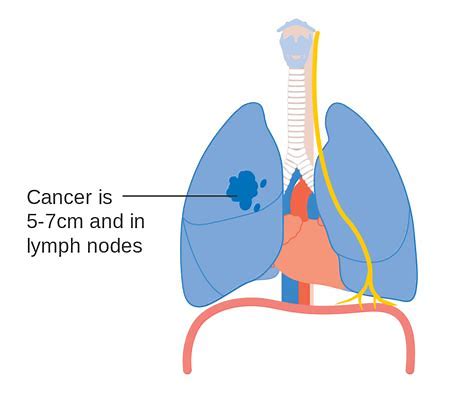
AZ的Tagrisso对肺癌的治疗具有持续作用
阿斯利康公司表示,Tagrisso作为一线治疗肺癌的"前所未有的无进展生存获益"通过后续的治疗方案得以延续。根据对全球III期FLAURA试验的数据进行的新分析,该试验评估Tagrisso(osimertinib)作为局部晚期或转移性表皮生长因子受体(EGFR)突变阳性患者的第一线发作的有效性和安全性 (EGFR
MedSci原创 - Tagrisso,肺癌 - 2018-04-16
FDA对阿斯利康肿瘤治疗的Tagrisso进行优先审查
美国FDA已经开始对阿斯利康公司的一线非小细胞肺癌(NSCLC)的Tagrisso进行优先审查,并于2018年上半年获得批准。第三代EGFR抑制剂Tagrisso(osimertinib)已经被批准作为该类药物的后续治疗,包括AZ的易瑞沙(gefitinib)和罗氏的Tarceva(erlotinib),但扩大到一线使用可以显着提高其销售潜力
MedSci原创 - Tagrisso - 2017-12-19
AZ的Tagrisso作为肺癌一线用药在美国获批
阿斯利康的Tagrisso已经在美国获得批准,作为对转移性非小细胞肺癌患者的一线治疗,用于肿瘤有表皮生长因子受体(EGFR)突变患者。扩大的批准基于来自III期FLAURA试验的数据,其中Tagrisso(osimertinib)与目前的一线EGFR-TKIs,
MedSci原创 - AZ的Tagrisso,肺癌一线用药 - 2018-04-20
NMPA授予Tagrisso(osimertinib)上市许可,治疗EGFR突变的非小细胞肺癌
国家医疗产品管理局(NMPA)已授予Tagrisso(osimertinib)作为一线治疗的上市许可。
MedSci原创 - NMPA,Tagrisso,EGFR突变,非小细胞肺癌 - 2019-09-05
AZ的肺癌药物Tagrisso在欧洲获准作为一线用药
欧洲的监管顾问支持阿斯利康公司的肺癌药物Tagrisso作为一线用药的批准。该研究的首席医疗官Sean Bohen指出:"该积极的建议承认Tagrisso的osimertinib具有欧洲EGFR突变NSCLC患者的一线治疗新标准的潜力。
MedSci原创 - Tagrisso,肺癌,AZ - 2018-05-01
阿斯利康的Tagrisso在美国被批准作为NSCLC的辅助疗法
FDA允许Tagrisso(osimertinib)治疗EGFR外显子19缺失或外显子21 L858R突变的非小细胞肺癌(NSCLC)患者。
MedSci原创 - NSCLC,阿斯利康,非小细胞肺癌(NSCLC),Tagrisso - 2020-12-19
欧洲药品管理局已经接受了Tagrisso(osimertinib)营销授权申请
阿斯利康宣布,欧洲药品管理局已经接受了Tagrisso(osimertinib)营销授权申请(MAAv)。Tagrisso是一种具有抗中枢神经系统(CNS)转移活性的第三代不可逆表皮生长因子受体(EGFR)酪氨酸激酶抑制剂(TKI),用于EGFR突变(外显子19缺失或外显子21(L858R)替换突变)局部晚期或转移性非小细胞肺癌
MedSci原创 - Tagrisso - 2017-12-02
阿斯利康第三代靶向肺癌药物Tagrisso获中国CFDA批准
英国制药巨头阿斯利康(AstraZeneca)近日宣布,中国食品和药品监督管理总局(CFDA)已批准抗癌药Tagrisso(omisertinib,AZD9291)40mg和80mg片剂,作为一种每日口服一次的药物
生物谷 - 阿斯利康,非小细胞肺癌,Tagrisso,EGFR-TKI,omisertinib,T790M,耐药突变 - 2017-03-30
WCLC 2020:Tagrisso可显著延长EGFR突变非小细胞肺患者的无病生存期
在接受过辅助化疗的患者中,Tagrisso辅助剂可将疾病复发或死亡的风险降低84%(危险比[HR]为0.16、95%置信区间0.10-0.26)。
MedSci原创 - 非小细胞肺癌,EGFR突变,Tagrisso - 2021-01-31
中国监管机构批准阿斯利康的Tagrisso作为EGFR突变型NSCLC的一线治疗药物
阿斯利康近日表示,中国国家医疗产品管理局(NMPA)已经批准其Tagrisso(osimertinib),用于一线治疗局部晚期或转移性非小细胞肺癌(NSCLC)的成人患者,这些患者的肿瘤细胞具有EGFR
MedSci原创 - Tagrisso,EGFR,NMPA,一线治疗药物 - 2019-09-04
III期ADAURA试验:Tagrisso在EGFR突变型肺癌患者的辅助治疗中具有压倒性疗效
III期ADAURA临床试验显示,Tagrisso(osimertinib)在辅助治疗IB、II和IIIA期表皮生长因子受体突变(EGFRm)非小细胞肺癌(NSCLC)且肿瘤完整切除的患者具有显著疗效
MedSci原创 - EGFR突变型非小细胞肺癌,Tagrisso - 2020-04-11
阿斯利康的EGFR抑制剂Tagrisso在III期临床试验中显著改善NSCLC的总体存活率
阿斯利康公布III期FLAURA试验中Tagrisso(osimertinib)在既往未治疗的、具有表皮生长因子受体(EGFR)突变的局部晚期或转移性非小细胞肺癌(NSCLC)患者中延长了总生存率(OS
MedSci原创 - 阿斯利康,EGFR抑制剂,Tagrisso,NSCLC,总体存活率 - 2019-08-10
阿斯利康非小细胞肺癌口服新药Tagrisso获FDA批准上市
11月13日,阿斯利康抗非小细胞肺癌口服新药Tagrisso获FDA快速批准(Accelerated approval)上市,Tagriss适用于表皮细胞生长因子受体(EGFR)T790M突变型和对其他
MedSci原创 - 2015-11-19
ELCC 2016:Tagrisso一线治疗EGFR T790M突变NSCLC患者,PFS长达19.3个月
FDA在去年11月13日以加速批准的方式提前3个月批准了阿斯利康的Tagrisso(osimertinib,奥希替尼),用于二线治疗携带EGFR T790M突变的非小细胞肺癌(NSCLC)患者。FDA的批准依据是AURA项目中两项II期研究的结果,显示Tagrisso对接受EGFR抑制剂治疗后疾病恶化NSCLC患者的客观应答率(ORR)分别为57%和61%。
MedSci原创 - ELCC,Tagrisso,奥希替尼,NSCLC - 2016-04-15
为您找到相关结果约51个