NAT NEUROSCI :中科院彭勃团队成功破解再殖小胶质细胞起源之谜
2018-02-27 BioArt BioArt
2018年2月22日和2月27日,Nature Neuroscience和Cell Discovery 在线刊发来自中国科学院深圳先进技术研究院彭勃团队主导的系列研究论文,分别揭示了脑与视网膜内小胶质细胞再殖现象(microglialrepopulation)的不同细胞起源,解决了成年哺乳动物中枢神经系统内是否存在小胶质细胞前体细胞的重要争议,并对中枢神经系统再生研究和小胶质细胞稳态维持有着重大科
2018年2月22日和2月27日,Nature Neuroscience和Cell Discovery 在线刊发来自中国科学院深圳先进技术研究院彭勃团队主导的系列研究论文,分别揭示了脑与视网膜内小胶质细胞再殖现象(microglialrepopulation)的不同细胞起源,解决了成年哺乳动物中枢神经系统内是否存在小胶质细胞前体细胞的重要争议,并对中枢神经系统再生研究和小胶质细胞稳态维持有着重大科学价值。
惊人的小胶质细胞再殖现象与重大争议
成年哺乳动物中枢神经系统(包括脑、视网膜和脊髓)的再生能力极其有限,曾在相当长的时间内认为其中枢神经系统受损的中枢神经系统无法修复。研究表明,在脑内只存在两类干细胞(或前体细胞):神经干细胞(neuralstem cell, NSC)以及少突胶质细胞前体细胞(oligodendrocyte precursor cell, OPC)。前者可分化成神经细胞和星形胶质细胞(astrocyte),后者可分化为少突胶质细胞(oligodendrocyte)。但是由于受到中枢神经系统细胞内在特性和外部环境的制约,其分化能力有限,无法在神经退行性病变(如脑外伤,老年痴呆和帕金森疾病等)时分化出足够的细胞以修复受损的中枢神经系统。因此,成年哺乳动物的脑损伤被认为是无法修复的。
然而,2014年来自加州大学欧文分校的研究人员在小鼠脑内发现了惊人的细胞再生现象,改写了脑内细胞再生的认知。KimGreen团队通过特异性抑制集落刺激因子1受体(colony-stimulatingfactor 1 receptor, CSF1R)的方式几乎完全消除脑内的小胶质细胞(>99%)。而当停止抑制并经过短暂恢复期后,脑内出现新生的小胶质细胞。这些再生的小胶质细胞可迅速定殖至全脑,并在一周左右完全恢复至原有状态(如密度、分布和形态)。这是人类首次在成年哺乳动物的中枢神经系统内发现的大规模细胞再生现象,该过程被称为小胶质细胞再殖。该研究团队通过组织学免疫染色的方式推测再殖小胶质细胞可能由脑内的一类瞬时表达Nestin的细胞分化而来。这被认为是继神经干细胞和少突胶质细胞前体细胞之外,在成年哺乳动物中枢神经系统内发现的第三类干细胞。在发育过程中,原生小胶质细胞起源于胚胎期的卵黄囊,而中枢神经系统内的其他细胞均起源于外胚层。Nestin细胞被认为是具有外胚层谱系干细胞的特征,提示该类干细胞具有跨谱系方向分化高分化潜能。由于其具有高度的分化潜能和惊人的分化速度,科学家认为有望通过调控该类细胞使其定向分化为脑内的其他细胞类型,这对于中枢神经系统损伤修复和再生医学具有重要意义。因此,该发现一经发表即得到了广泛关注,论文的年引用率逾100次。
然而着重大发现的背后,伴随的是关于再殖小胶质细胞起源的极大争议:首先,成熟的中枢神经系统中是否可能存在跨谱系分化现象。若再殖小胶质细胞由Nestin阳性细胞分化而来,即提示外胚层起源细胞可向其他谱系方向分化,而这种跨谱系细胞分化现象在成年哺乳动物的中枢神经系统内的发生概率极低。其次,再殖小胶质细胞是否起源于血液细胞的分化。在神经炎症反应中,会有极少量的血液细胞穿过血脑屏障并分化成小胶质细胞样细胞(microglia-likecell)。而既往关于再殖小胶质细胞起源的研究未充分排除该途径。第三,再殖小胶质细胞亦有可能来源于残存的小胶质细胞。依据KimGreen团队的研究,脑内仍残存少量的小胶质细胞(约1%),残存的小胶质细胞可能通过增殖的方式形成再殖小胶质细胞,而该途径的可能性亦未能完全排除。因此,关于脑内再殖小胶质细胞的起源问题,学术界存在重大争议。
多种谱系追踪技术锁定再殖小胶质细胞起源
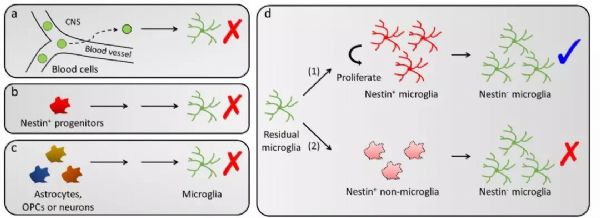
在Nature Neuroscience刊发的题为"Repopulated microglia are solely derived from the proliferation of residual microglia after acute depletion"的研究论文中,彭勃教授团队首次通过严谨的多种谱系追踪(fate mapping或lineagetracing)技术,系统性阐述再殖小胶质细胞的起源问题。首先,彭勃教授团队利用连体结合手术(parabiosis),将野生型小鼠与携带GFP绿色荧光蛋白小鼠的血液进行交换,以研究再殖小胶质细胞可能的血液起源途径。该团队发现,在其探索过的所有脑区内,均未发现有起源于血液的再殖小胶质细胞,排除了再殖小胶质细胞的血液起源假说(图2a)。
随后,该研究团队利用诱导型谱系追踪转基因小鼠Nestin-CreERT2::Ai14标记所有的Nestin细胞。在该类实验中,重组酶CreER会在他莫昔芬的诱导下切除Nestin细胞中报告基因tdTomato前的停止信号。于是该类细胞和其分化而成的后代细胞均会永久表达tdTomato报告蛋白。但令人意外的是,再殖小胶质细胞中未发现携带有tdTomato报告蛋白,说明该类细胞并非起源于前人所推测的Nestin阳性细胞(图2b)。
紧接着,该团队利用多个转基因小鼠工具对脑内主要的外胚层谱系细胞(包括星形胶质细胞、神经干细胞、少突胶质细胞前体细胞和多种神经细胞)进行谱系追踪,发现这些细胞均不是再殖小胶质细胞的前体细胞(图2c)。相反,通过巧妙设计的Cx3cr1-CreER::Ai14谱系追踪技术发现,所有的再殖小胶质细胞是由中枢神经系统内残存的原生小胶质细胞(<0.9%)经过直接的细胞增殖而来。在此过程中,新生的小胶质会瞬时性表达Nestin蛋白,但其细胞命运(cellfate)未发生改变(图2d)。于是,彭勃团队通过多种谱系追踪技术推翻了前人关于再殖小胶质细胞起源于Nestin阳性前体细胞分化的结论,并发现其再殖小胶质细胞完全起源于残存的小胶质细胞增殖。该现象是迄今为止在成年哺乳动物中枢神经系统内发现的最快的细胞增殖现象。此外,彭勃团队还通过单细胞RNA测序技术阐述了其细胞再殖的可能机理,并通过全脑RNA测序,发现了再殖小胶质细胞与原生小胶质细胞在功能学上的高度相似性。
Nature Neuroscience的两位匿名审稿人非常罕见地同时在审稿意见中对该论文给予非常高的评价。一位审稿人评价道:
“In their very elegant study the authors used a plethora of state-of-the-art fate mapping studies, parabiosis and sophisticated confocal immunofluorescence examinations for their thorough characterizations of microglia repopulation upon deletion… The topic tackled by the authors is of great relevance and some of their findings are of big importance. Overall, the manuscript is clearly structured, plausibly written and several high-end methods are used. The experiments were performed on a high technical standard and the conclusions drawn are justified.(在他们非常优雅的研究中,作者通过大量的现有最高水平的谱系追踪、联体结合手术和复杂的荧光共聚焦测试方法,详尽解析了小胶质细胞再殖现象。……作者的主题具有极大的相关性,他们的部分发现非常重要。总的来说,该论文结构清晰,撰写合理,并使用了具有高技术含量的研究方法。实验在高技术标准下进行,并得出了合理的结论。)”
同时,另外一位匿名审稿人则评价说:
“This is an excellent paper that addresses a number of controversial issues recently raised about microglia dynamics. Each conclusion brought forward is supported by multiple experiments using various approaches, including extensive lineage tracing for multiple CNS lineages. The conclusions appear amply justified by the data presented.(这是一篇卓越的论文,解决了近期一系列关于小胶质细胞动态的争议问题。作者的每一条结论都通过了多个不同的实验手段得出。所提供的数据得出的结论非常合理。)”
据了解,由于彭勃团队出色的回答了领域内关于小胶质细胞起源的重要问题,该论文在仅经一次修改的情况下被Nature Neuroscience原则接收。
视网膜研究意外发现全新小胶质细胞起源途径
视网膜是中枢神经系统内特殊的部分。在成年哺乳动物中,未有确凿证据表明视网膜内存在具有分化潜能的干细胞(只存在有零星报道的细胞再生现象,且存在争议)。因此,视网膜被认为无再生能力,一旦受损将无法修复。
彭勃教授团队发现当通过药物特异性抑制CSF1R时,视网膜内的小胶质细胞会完全被杀死(100%)。假如视网膜小胶质细胞遵循和脑小胶质细胞同样的再殖途径(图2),那么由于视网膜内无小胶质细胞残留,因此研究人员推测视网膜内不会发生小胶质细胞再殖现象。然而,彭勃团队非常惊讶的发现视网膜内的小胶质细胞依然能够再殖。于是,彭勃团队通过一系列的谱系追踪和视网膜离体培养(ex vivoculture)等技术,探索视网膜内小胶质细胞的起源。研究团队发现与脑小胶质细胞不同的是,视网膜内再殖小胶质细胞具有两条不同的视网膜外起源途径:大部分再殖小胶质细胞起源于视神经处残存的小胶质细胞向外迁移,而小部分再殖小胶质细胞来源于视网膜外侧睫状体和/或虹膜的巨噬细胞向内迁移(图3)。两种不同起源的再殖小胶质细胞呈现出不同的细胞形态,暗示其内在特性和功能的不同。综上,彭勃团队利用小胶质细胞消除-再殖模型,首次在成年哺乳动物视网膜上观察到了大规模的细胞再生现象,并阐明了其细胞起源。
长期以来,不论是在稳态和疾病状态下,视网膜内小胶质细胞被认为主要由内源性小胶质细胞维持。而该研究这是首次在成年哺乳动物的视网膜内观察到了外源性的小胶质细胞起源,这个发现对视网膜退行性病变的病理机制和治疗具有了重要的科学价值。该研究成果发表于Cell Discovery杂志上,标题为"Dualextra-retinal origins of microglia in the model of retinal microgliarepopulation"。
彭勃团队通过在脑和视网膜上关于小胶质细胞再殖的系列工作,全面阐述了其在中枢神经系统内的起源和功能,构成了有机的整体。该系列工作主要是彭勃团队与香港大学饶艳霞医生和上海精神卫生中心袁逖飞教授合作完成。彭勃教授团队的博士后黄玉斌和徐臻为该系列工作的共同第一作者。
原始出处:
[1]Huang, Y., Xu, Z., Xiong, S., Sun, F., Qin, G., Hu, G., Wang, J., Zhao,L., Liang, Y.-X., Wu, T., et al. (2018). Repopulated microglia are solelyderived from the proliferation of residual microglia after acute depletion.Nature neuroscience. https://www.nature.com/articles/s41593-018-0090-8
[2]Huang Y., Xu Z., Xiong S., Qin, G., Sun F., Yang J., Yuan T.F., ZhaoL., Wang K., Liang Y.X., Fu L., Wu T., So K.F., Rao Y. and Peng B., Dualextra-retinal origins of microglia in the model of retinal microglialrepopulation, 2018 (Cell Discovery) https://doi.org/10.1038/s41421-018-0011-8
小提示:本篇资讯需要登录阅读,点击跳转登录
版权声明:
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#中科院#
23
#Nat#
23
#ROS#
34
#胶质细胞#
36
一起学习学习
91