讲堂:临床试验报告的统一标准(CONSORT)
2018-12-13 佚名 复旦循证护理中心
一随机对照试验及其报告现状随机对照试验(RCT)通常是评估干预效果的最佳研究设计,但低质量的临床试验可能会错误地估计疗效。自2000年以来,每年都有25000篇随机或对照试验的文章被发表,但庞大的数量并不意味着决策者很容易找到可信的证据进行临床和保健决策,中国发表的随机对照试验文章质量亦令人堪忧。解决这些问题,一方面需从源头抓起,注重顶层设计和实施过程的质量控制;另一方面,完整、准确地报告研究论文
一
随机对照试验及其报告现状
随机对照试验(RCT)通常是评估干预效果的最佳研究设计,但低质量的临床试验可能会错误地估计疗效。自2000年以来,每年都有25000篇随机或对照试验的文章被发表,但庞大的数量并不意味着决策者很容易找到可信的证据进行临床和保健决策,中国发表的随机对照试验文章质量亦令人堪忧。解决这些问题,一方面需从源头抓起,注重顶层设计和实施过程的质量控制;另一方面,完整、准确地报告研究论文也有助于读者判断临床试验的内外部真实性(或称有效性)和应用价值。
本次讲堂旨在对近年来国际上提出的随机对照试验相关报告规范即临床试验报告的统一标准(Consolidated standards of reporting trials,CONSORT)及其扩展版进行简介。1995年,为了提高随机对照试验报告质量,一个由临床试验学者、统计学家、流行病学家和生物医学编辑组成的国际小组制定了CONSORT。1999年,CONSORT制定组织对CONSORT进行了修订,成为一个由22个条目组成的清单,见表1。
二 CONSORT清单
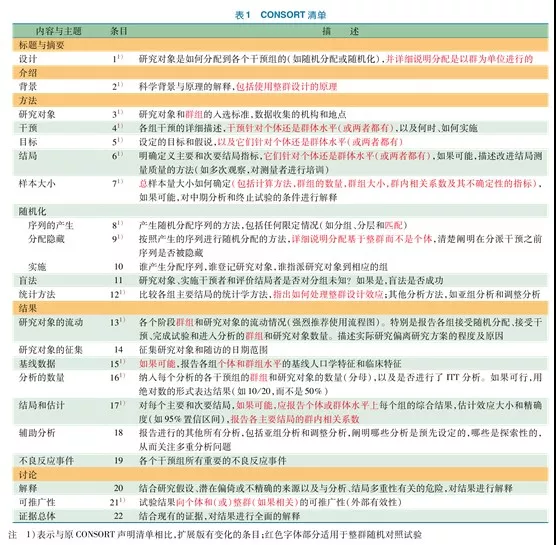
三参考文献
詹思延.第二讲:如何报告随机对照试验——国际报告规范CONSORT及其扩展版解读[J].中国循证儿科杂志,2010,5(02):146-150.
小提示:本篇资讯需要登录阅读,点击跳转登录
版权声明:
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







马住了
48
#统一标准#
36
#CONSORT#
34
#CONSORT#
33
好
56
学习学习学习
44