颅内肿瘤围术期突发Tako-tsubo综合征1例
2019-10-14 刘蓓 王公明 李伟 麻醉安全与质控
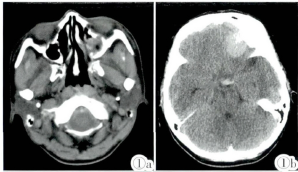
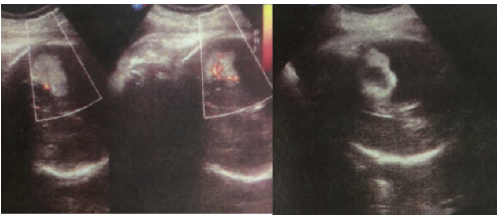
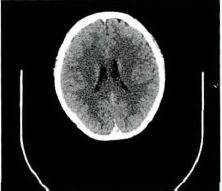
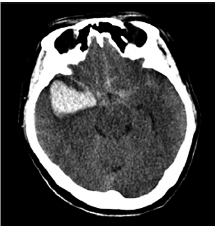
Tako-tusbo综合征(Tako-tusbo syndrome,TTS),又名应激性心肌病,由日本学者于1990年首次报道,其特征表现为短暂性可逆性心室局部收缩功能障碍,且不能用冠状动脉粥样硬化性疾病来解释所观察的一过性心室功能障碍。已知多种中枢神经系统疾病可能会引起一系列心功能异常,其中包括TTS。本文描述了1例罕见的颅内肿瘤患者围术期突发恶性心律失常,其最终诊断为TTS。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#Tako-tsubo综合征#
34
#围术期#
47
#综合征#
42