FDA延长了对Opdivo/Yervoy联合治疗方案的审查
2018-10-21 MedSci MedSci原创
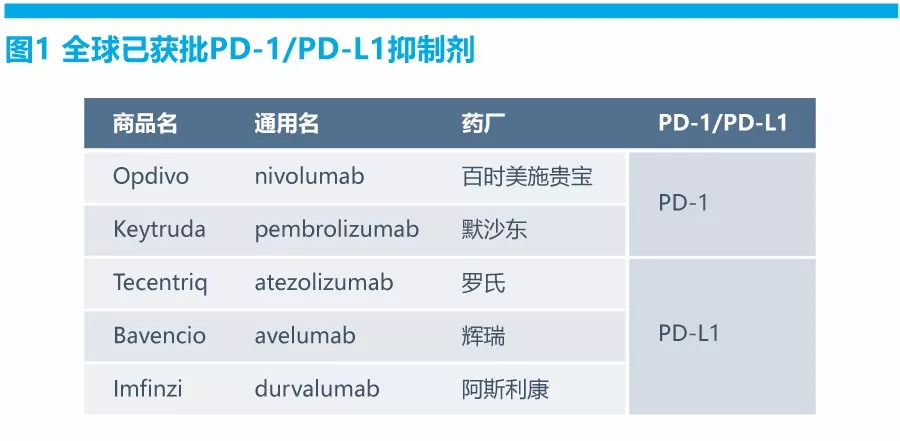
百时美施贵宝近日表示,FDA延长了对Opdivo(nivolumab)联合低剂量Yervoy(ipilimumab)一线治疗晚期非小细胞肺癌(NSCLC)申请的审查,预计延长三个月,FDA表示要着重考虑每兆碱基(mut / Mb)至少10个突变的肿瘤突变负荷(TMB)。
百时美施贵宝近日表示,FDA延长了对Opdivo(nivolumab)联合低剂量Yervoy(ipilimumab)一线治疗晚期非小细胞肺癌(NSCLC)申请的审查,预计延长三个月,FDA表示要着重考虑每兆碱基(mut / Mb)至少10个突变的肿瘤突变负荷(TMB)。FDA在2018年6月份接受了这份申请,同时百时美施贵宝此前宣布,相关临床试验符合其无进展生存期(PFS)的主要终点,后来在美国癌症研究协会(AACR)年会上详细说明了试验结果,与化疗相比,Opdivo和Yervoy的组合降低了疾病进展及死亡率的风险。当时,百时美施贵宝指出,对于TMB至少10 mut / Mb的患者,Opdivo联合Yervoy方案与化疗相比,总体存活率“令人鼓舞”。
该公司表示,在欧洲药品管理局人用药品委员会要求TMB作为其申请审查的一部分后,该公司随后向FDA提交了至少10 mut / Mb的TMB患者的OS分析。百时美施贵宝表示,FDA确定新信息构成了一项重大修订,从而延长了其审查范围与审查时间。
原始出处:
http://www.firstwordpharma.com/node/1598764?tsid=4#axzz5UWRvhj3l
本文系梅斯医学(MedSci)原创编译整理,转载需授权!
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#治疗方案#
29
#Opdivo#
32
#联合治疗#
23
#Yervoy#
40