ASCO2019 |新型融合抗PD-L1抗体试用在中国晚期实体瘤患者中的应用
2019-06-02 小M MedSci原创
第55届美国临床肿瘤学会(ASCO)年会于2019年5月31日至6月4日在美国芝加哥召开。本次会议吸引世界3万8千名肿瘤专家参与。
第55届美国临床肿瘤学会(ASCO)年会于2019年5月31日至6月4日在美国芝加哥召开。本次会议吸引世界3万8千名肿瘤专家参与。
KN035是人源化抗PD-L1单结构域抗体和人IgG1 Fc的新型融合蛋白,配制用于皮下(SC)注射。我们KN035的差异于其他同类药物的主要是皮下注射的剂型,对于癌症病人很方便,而且节省整个医疗的费用。
KN035分别在中国和日本进行了一期临床试验。在中国晚期恶性肿瘤患者中表现出良好的安全性和有希望的初步抗肿瘤活性。17名患者参加了临床试验,包括肝细胞癌,肝内胆管细胞癌,胸腺癌,结直肠癌,肾细胞癌,鳞状细胞肺癌和卵巢癌患者。

大多数受试者具有晚期疾病阶段,IV期和III期。共有7名受试者接受了放射治疗,16名受试者接受了手术,13名受试者接受了先前治疗的系统性抗癌治疗。没有人接受过先前的免疫检查点抑制剂治疗。只有一人3级药物相关的治疗突发不良事件(TEAE)发生在0.3 mg / kg剂量水平,这是免疫相关的皮炎,后来解决。
所有其他药物相关的TEAE均为1级或2级,最常见的事件是ALT升高(5/17)和AST升高(4/17)。在所有登记的受试者中,三名受试者已确认PR,包括一名2.5mg / kg的RCC受试者和一名5mg / kg的肝内胆管癌受试者,以及一名10mg / kg的胆管癌受试者。
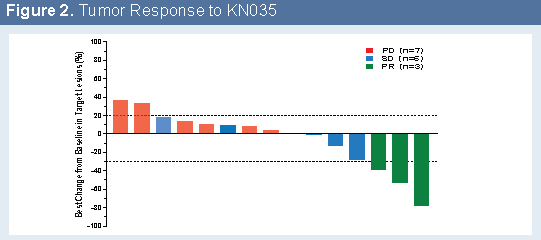
在日本患者中进行了I期安全性和药代动力学(PK)研究。在5mg / kg QW的最高剂量水平下未观察到DLT。没有达到最大耐受剂量(MTD)。在有基线和至少22周疗效检查的病人中,有两个确认的部分反应在晚期恶性肿瘤患者中表现出良好的安全性,初步结果显示出令人鼓舞的抗肿瘤活性。基于来自Q2W时间表的PK数据,目前正在评估每4周具有较少频率给药方案的固定剂量。
KN035在I 期临床试验很成功,药效和安全 性均与其它公司同类产品结果一致甚至更好,药效强,维持时间长。但我们的产品由于高水溶性可直接皮下注射给病人,免去了医生预约在医院IV注射的繁琐程序,大大方便了治疗流程。
会上我们采访了3DMed (思路迪)公司的CMO David,并问了几个简单的问题。

1. Q:能简单介绍一下思路迪3D Medicine 公司吗?
David:公司在中国已建立8年多,现在已经开始全球扩展业务。公司的主要业务和产品包括新药研发和临床诊断。
2. Q:这次参加2019ASCO年会,3D Medicine 有多少口头报告和海报?
David:2019年思路迪共有35项与临床专家合作的科研成果入选ASCO,其中10项成果将在会议期间以Poster形式进行展示。
3. Q:今后有无临床II期、III期计划?
David:我们正在中国进行临床II期、III期试验,II期主要集中在结直肠癌,III期主要集中在胆管癌,数据还未成熟 ,期待在明年的ASCO会有正式的报道。今年也将展开全球的III期试验。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#抗PD-L1抗体#
41
#ASC#
28
#PD-L1#
26
#晚期实体瘤#
33
#融合#
32