美敦力康辉骨科集团集结多款新品亮相2019 COA
2019-11-19 不详 美通社
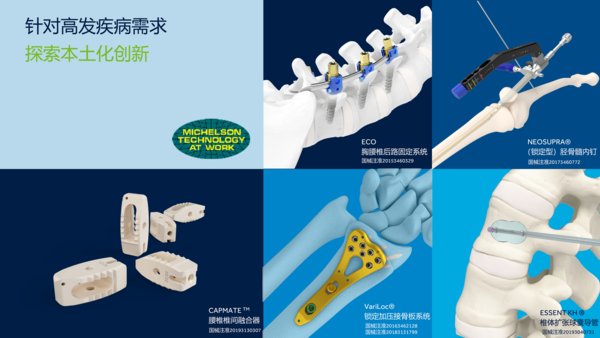
美敦力康辉骨科集团,全球领先的骨科企业,集结多款创伤及脊柱新品和解决方案,参展第十四届COA国际学术大会,向国内外骨科医生呈现更多适合于中国乃至全球其他市场需求的治疗选择。本次参展新品,包括NEOSUPRA®(锁定型)胫骨髓内钉、CAPMATETM腰椎椎间融合器、ECO胸腰椎后路固定系统、ESSENT KH®椎体扩张球囊导管以及VARILOC®锁定加压接骨板系统。 美敦力康辉骨科展台
美敦力康辉骨科集团,全球领先的骨科企业,集结多款创伤及脊柱新品和解决方案,参展第十四届COA国际学术大会,向国内外骨科医生呈现更多适合于中国乃至全球其他市场需求的治疗选择。本次参展新品,包括NEOSUPRA®(锁定型)胫骨髓内钉、CAPMATETM腰椎椎间融合器、ECO胸腰椎后路固定系统、ESSENT KH®椎体扩张球囊导管以及VARILOC®锁定加压接骨板系统。
“我非常期待即将上市的多款脊柱和创伤新品。这些新产品都已经蓄势待发,将致力于为医生和患者提供更好的术中体验和术后康复。”新上任的美敦力康辉骨科总经理魏璇博士谈道,“好的产品从来都不是一蹴而就。在过去几年里,我们一直在把前沿的技术和疗法,与临床需求相结合,研发设计更适合于中国市场的骨科产品。通过对新产品的反复验证和收集临床反馈,真正实现了把值得信赖的产品带给更多的医生和患者。”
新品齐聚,为医生赋能
美敦力康辉骨科集团,全球领先的骨科企业,集结多款创伤及脊柱新品和解决方案,参展第十四届COA国际学术大会,向国内外骨科医生呈现更多适合于中国乃至全球其他市场需求的治疗选择。
美敦力康辉骨科集团即将上市的NEOSUPRA®(锁定型)胫骨髓内钉,可多平面交锁实现各截骨面最大持骨量,拓展适应证范围;操作工具简化易用,一键旋转,实现近端锁定;采用轻便碳纤维远瞄支架,可简易高效地实现远端锁定,减少手术时长和辐射量;提供髌上髌下工具用于不同适应证选择。
在此次展会上,最新推出的CAPMATETM腰椎椎间融合器,在传承美敦力经典设计的基础上,结合中国市场需求,进行设计优化升级,使其成为医生得力助手,让腰椎融合手术更可靠。
此外,ECO胸腰椎后路固定系统,充分借助美敦力全球研发技术和资源,以高效、经典、优化为核心,立足本土化应用,旨在提高术中体验和临床效果。
ESSENT KH®椎体球囊产品,可应用于老年骨质疏松性椎体压缩性骨折的治疗。该产品传承美敦力Kyphon球囊技术与设计,其优势在于对伤后疼痛、生活质量、功能活动的明显改善。
品质护航,缔造新起点
康辉即将推出的多款新品,在过去几年的时间里,都在被反复讨论和验证,以确保其性能的合理性和有效性。经历过机械实验、力学实验,使这些新产品和配套工具都在极限、失效和使用寿命的不同测试下完成了蜕变。
同时,为了确保产品和工具在实际临床使用中的效果,携手临床主任以及美敦力资深研发技术支持,进行了多次模拟临床操作验证。
“中国速度享誉世界,中国品质服务全球。我们希望以更快的速度把优质的产品带到中国更多需要的地区和市场,扩大医疗可及性,使更多患者从中受益。同时,我们也在加大对专业教育方面的投入,携手众多医疗机构开展多元化专业教育课程和学术交流项目,提高医生临床及手术操作技巧,帮助患者获得更佳的医疗服务及治疗效果。”美敦力大中华区康辉业务高级总监李从真谈道。
作为全球领先的骨科品牌,康辉将不断为医生、患者以及合作伙伴带来创新的疗法和全面的骨科解决方案,帮助他们提高医疗效率和可及性,创造并实现真正有价值的医疗。
关于美敦力康辉骨科
美敦力康辉骨科,全球领先的骨科企业,隶属于美敦力公司恢复性疗法业务集团下的业务单元,致力于为医疗专业人士提供创新且具有经济价值的产品和解决方案。于2012年11月,美敦力公司宣布完成对康辉(中国)控股公司的收购,使其成为首个总部在美国之外独立运营的业务部门。美敦力康辉骨科在中国有两个生产基地,包括常州市康辉医疗器械有限公司,以及北京理贝尔生物工程研究所有限公司。公司员工超过1000名,业务遍布中国及其他50多个国家。借助美敦力品牌优势和健全的业务网络,助力美敦力康辉在全球新兴市场加速拓展业务版图,提供全面可靠的产品组合。
关于美敦力
美敦力的总部设在爱尔兰都柏林,是一家全球化的医疗科技、服务和解决方案提供者,致力于为全球千百万人减轻病痛、恢复健康、延长寿命。美敦力有超过90000名员工,在全球150多个国家和地区为医生、医院和患者提供服务。与全球的合作伙伴携手,共同推动医疗事业的发展。Further, Together。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













#COA#
41
很好的学习机会
73
#美敦力#
38
学习了很有用不錯
76