

背景
套细胞淋巴瘤(MCL)是一种B细胞恶性肿瘤,具有独特的生物学、病理学和临床特征,占所有非霍奇金淋巴瘤(NHL)的3%-10%。其分子特征为染色体t(11;14)(q13.3;q32.33),进而导致细胞周期蛋白D1(cyclin D1)的过表达。MCL主要发生在老年人(中位年龄60-65岁),以男性居多,男女比例为2:1。自然病程表现为侵袭性和惰性,患者常常最终出现耐药和复发,属于不可治愈性疾病。MCL患者中位生存期为4-5年,但对于能够忍受强化疗方案的年轻健康患者来说,中位生存期为8-12年。
大多数(>90%)MCL患者确诊时已为晚期,临床表现为淋巴结肿大、脾大、骨髓受浸;外周血及结外受累也很常见,常累及胃肠道和肝脏,也可累及乳房、肺、皮肤、软组织、唾液腺和眼眶;巨大肿块和B症状相对少见;有30%-50%的患者可伴有两个以上的结外部位受累;中枢神经系统(CNS)受累较为罕见。
MCL的临床进程具有异质性。临床表现与病理亚型相关,有些病例表现为侵袭性的临床进程,对治疗不敏感,生存期短。与此相反,有些病例表现为惰性的临床进程,以脾大、外周血淋巴细胞增多、很少或没有淋巴结累及为特征,生存期可达到5-12年。目前已认识到原位套细胞淋巴瘤的本质,惰性而局限,临床进展表现为低风险。
一、MCL的一线治疗
大多数MCL患者在诊断时即需要接受治疗,治疗指证包括:有症状的巨大淋巴结病;B症状;有症状的器官肿大;包括出血在内的胃肠道症状;骨髓衰竭。在开始治疗前,方案的选择应取决于患者年龄、合并症、PS评分和治疗目标,特别是应该对适合自体造血干细胞移植(ASCT)的年轻患者和那些不适合ASCT的患者作出区分,BSH认为,ASCT的适合与否是决定治疗方案的关键 (见Fig 1)。
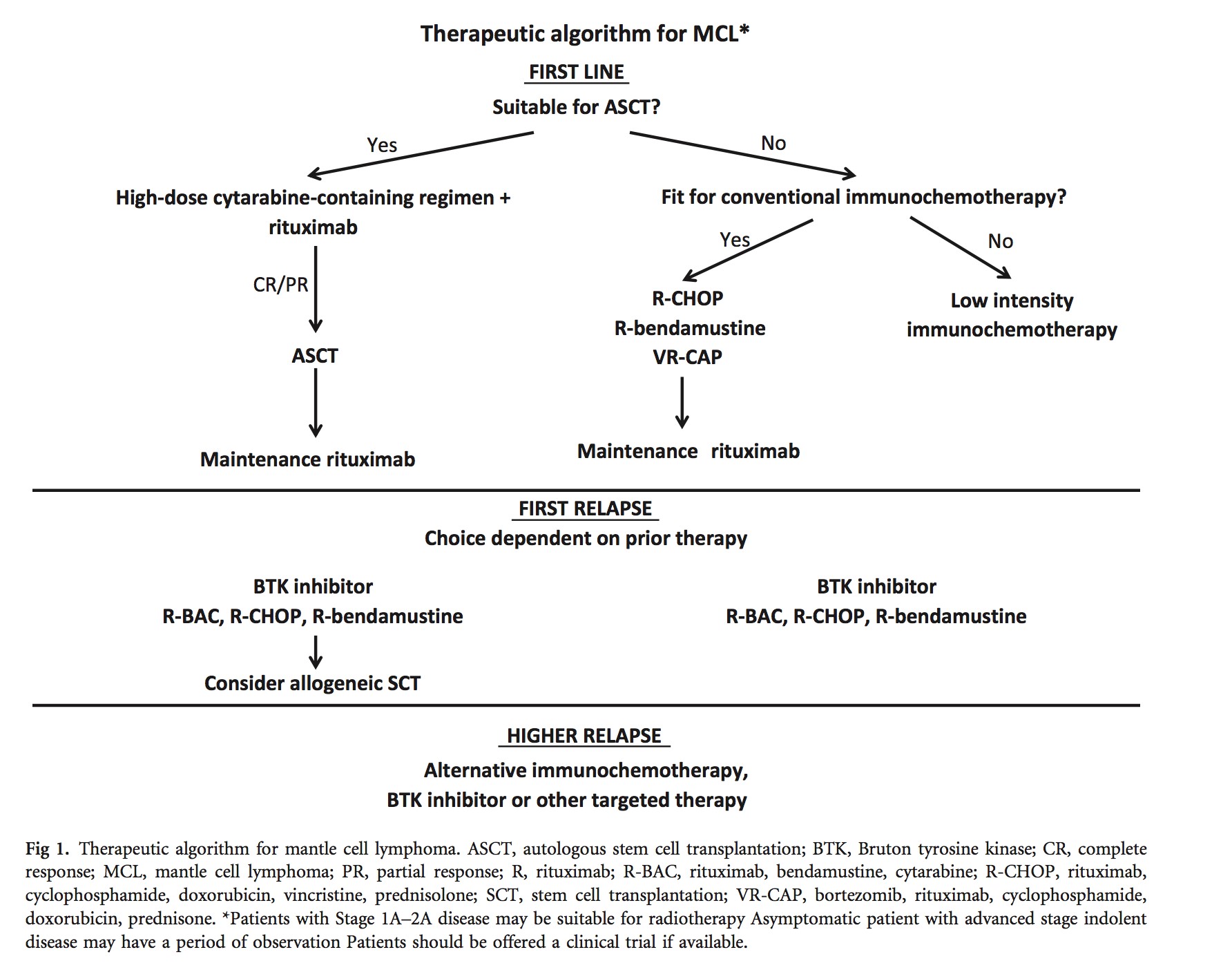
1、治疗前应考虑的因素
患者的年龄、合并症、PS评分和治疗目标
2、惰性MCL的治疗选择
对惰性MCL的研究较少。有研究表明,累及部位的局部放射治疗可能会产生良好的疗效,64%-80%的患者可达完全缓解(CR)和长期缓解,甚至有些患者可以被治愈。
3、侵袭性MCL一线治疗(适合ASCT)
——阿糖胞苷的优势
CHOP(环磷酰胺,多柔比星,长春新碱,泼尼松龙)及R-CHOP(利妥昔单抗+CHOP)方案已经广泛应用于ASCT前,以使患者获得完全缓解(CR)或部分缓解(PR)。近年来,阿糖胞苷(cytarabine)的疗效越来越受到人们的重视,当其应用于一线治疗时,疗效优异,大多数研究显示其总反应率ORR> 90%,CR> 50%。
2016年 “MCL Younger” 研究评估了R-DHAP(利妥昔单抗+地塞米松,高剂量阿糖胞苷,顺铂)与R-CHOP的差异,中位随访6.1年后,含阿糖胞苷组的治疗失败时间明显延长(9.1年vs 3.9年)。同样,2016年另一项II期临床研究表明,3个周期的R-苯达莫司汀+3个周期的R-高剂量阿糖胞苷治疗, CR/ CRu为96%,中位随访13个月时,PFS为96%。因此, 2018版BSH指南强烈推荐高剂量阿糖胞苷,用于适合ASCT患者的一线治疗方案中。
—— R-hyperCVAD方案已被摒弃
两项多中心临床试验研究得出结论,认为虽然R-hyperCVAD(环磷酰胺、长春新碱、多柔比星、地塞米松,与利妥昔单抗联合高剂量的甲氨喋呤和阿糖胞苷交替应用)曾经是MCL一线治疗的积极方案,但几乎40%的患者由于急性骨髓毒性和感染性并发症等原因无法完成治疗计划。因此,2018版BSH指南不再推荐R-hyperCVAD作为一线方案。
4、侵袭性MCL一线治疗(不适合ASCT)
——FC方案已被摒弃
大多数MCL患者是老年人,因此高剂量化疗方案是不可行的。对于这一部分患者,目前无标准疗法。在以往,MCL在临床研究中被认为是低级别淋巴瘤,治疗方案包括CVP(环磷酰胺、长春新碱、泼尼松)联合氟达拉滨和CHOP,但疗效均不佳。尽管FC(氟达拉滨,环磷酰胺)方案曾经取得过积极的治疗效果,但最新的研究显示,虽然R-FC和R-CHOP在完全缓解率上相似(R-FC 40%,R-CHOP 34%),但R-FC与更频繁的疾病进展相关(R-FC 14%,R-CHOP 5%),4年OS缩短幅度更加明显(R-FC 47%,R-CHOP 62%),且 R-FC方案的不良反应发生率更高。因此2018版BSH指南不再推荐FC及R-FC方案作为老年MCL患者的一线治疗方案。
——苯达莫司汀备受青睐
苯达莫司汀(Bendamustin)在MCL治疗中,兼具高有效性及低毒性特征,随着研究的深入,苯达莫司汀可能在MCL治疗中的作用越来越大。2005年,苯达莫司汀和利妥昔单抗(BR)联合应用的ORR为75%(CR 50%)。2014年,在BRIGHT研究中,BR无劣于R-CHOP或R-CVP,BR的ORR高达97%(CR 31%),R-CHOP/R-CVP的ORR为91%(CR 25%)。
二、MCL一线治疗总结
• 在考虑如何治疗套细胞淋巴瘤(MCL)时,临床表现、增殖指数、临床风险评分(简化MCL国际预后指数[sMIPI]和MCL国际预后指数[MIPI-c])以及身体状况,应纳入考量。(1B)
• 早期MCL(1A或2A期)患者,建议局部放疗。(1B)
• 临床表现为惰性进程的患者,可以考虑观察等待。(2B)
• 利妥昔单抗(R)联合化疗可提高疗效。因此,利妥昔单抗应纳入一线化疗方案。(1B) 但不建议利妥昔单抗单药治疗。(1A)
• 不适合自体干细胞移植(ASCT)的患者应接受R-化疗方案。R-CHOP(环磷酰胺、多柔比星、长春新碱、泼尼松)序贯利妥昔单抗维持治疗疗效最好,而R-苯达莫司汀也是有效的,而且副作用更小。(1B)
• 年轻、健康的患者应接受利妥昔单抗联合含高剂量阿糖胞苷的方案,以期在首次缓解期间进行ASCT。(1B)
• 未能行ASCT治疗的患者,R-化疗有反应后(完全或者部分缓解),推荐进行利妥昔单抗维持治疗。(1B)
• 疗效的评价应使用CT。除非进行临床试验,否则不推荐FDG-PET和微小残留病灶(MRD)状态评估。(1B)
三、MCL的二线及以上治疗
对于复发MCL,目前尚无标准的二线治疗方案。比起初始治疗,二线治疗后的CRs通常更低,反应持续时间更短。由于许多复发性MCL的治疗方案是单臂研究,且其纳入/排除标准不同,因此很难对这些研究的结论进行横向比较。尽管如此,随着新的靶向药物,特别是口服型BTK抑制剂伊布替尼的上市,复发难治性MCL的治疗获得了巨大的突破。
1、MCL二线治疗——伊布替尼正式登上历史舞台
在二线治疗中,2018版同样推荐R-BAC,R-CHOP及R-bendamustin方案。但尤其值得注意的是,靶向BTK抑制剂已在2012年后上市,且BTK抑制剂对复发难治MCL显示出了卓越的疗效(图1)。纵观全球,目前共有4种药物获批用于复发/难治MCL:硼替佐米(bortezomib),来那度胺(lenalidomide),西罗莫司(temsirolimus)和伊布替尼(ibrutinib)。横向比较这4种药物的有效性发现,伊布替尼具有最佳的ORR、CR、DOR、PFS及OS(表1)。2016年发表于《柳叶刀》的一项涉及这些药物的随机试验表明,与西罗莫司相比,伊布替尼治疗组的PFS显著改善(14.6个月vs 6.2个月),且治疗相关毒性较低。与一线治疗情况类似的是,利妥昔单抗在加入新药治疗方案后,患者的反应率和缓解深度均有一定程度的改善(表1)(利妥昔单抗+伊布替尼:ORR增加至87%,CR增加至38%),并可能改善PFS。更为重要的是,伊布替尼可以穿过血脑屏障并对治疗CNS复发有效,且越早使用伊布替尼有效性就越高。伊布替尼的作用显然不会局限于二线治疗,伊布替尼作为一线治疗药物的临床试验也正在进行中。
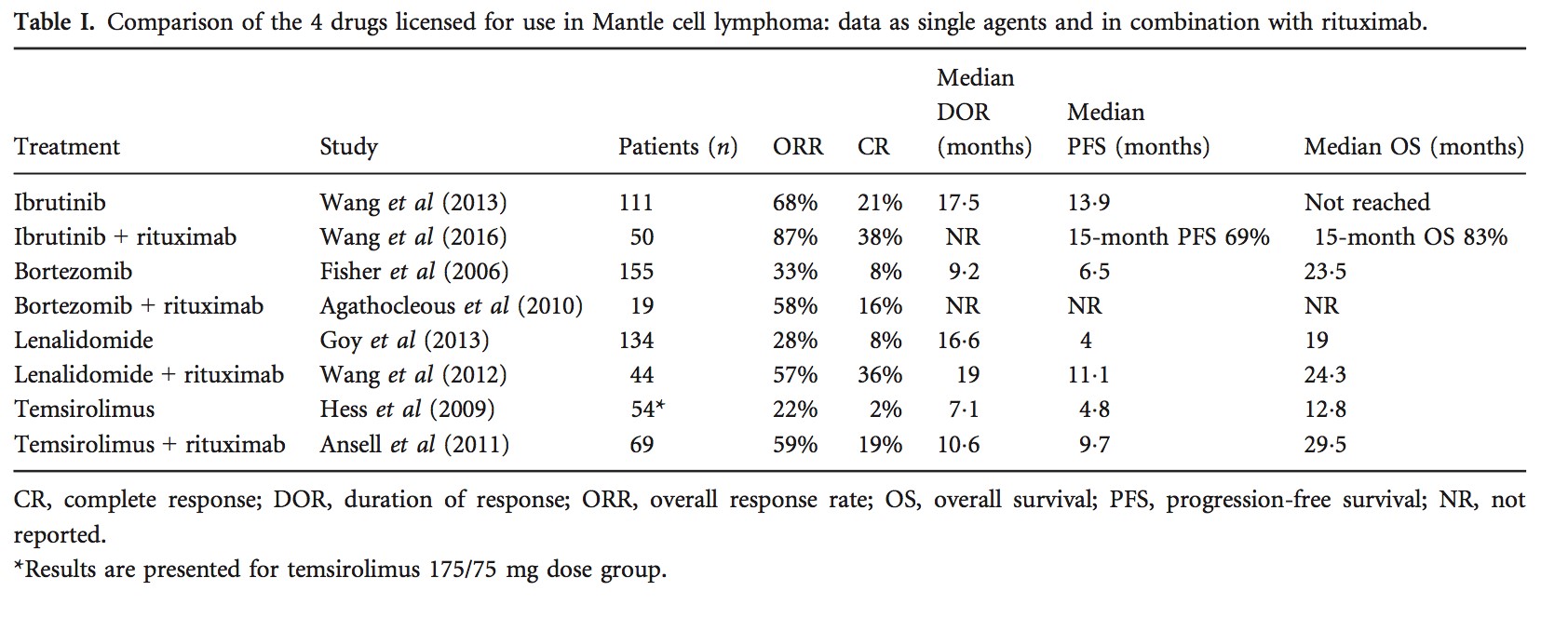
2、MCL二线治疗——其他药物
硼替佐米:关于硼替佐米联合标准CHOP方案、联合地塞米松和利妥昔单抗、联合苯达莫司汀和利妥昔单抗、联合高剂量阿糖胞苷、联合吉西他滨和联合放射免疫疗法等的研究表明,反应率超过50%,但因入组患者数很少,不具有代表性。2015年的一项关于硼替佐米联合来那度胺的研究,ORR为39.5%(CR 15%),但中位PFS仅为7个月。
来那度胺:是一种口服免疫调节剂,对血液系统恶性肿瘤治疗有效,单药来那度胺在MCL中活性约为30%。但与伊布替尼一样,反应可能是持久的。通过与利妥昔单抗或地塞米松或硼替佐米联合治疗可提高反应率。PFS在所有联合用药方案中均有改善。
西罗莫司:是一种mTOR抑制剂,注册研究的ORR为22%(2%CR)。联合利妥昔单抗可提高疗效,尤其是CR率(59%ORR,19%CR),但关于进一步联合治疗的报道有限。
Idelalisib:PI3K抑制剂,单药ORR为40%(CR 5%)。反应持续时间很短,中位持续时间为2.7个月,PFS为3.7个月。
Venetoclax :BCL2抑制剂。一项I期试验显示,ORR为75%(21%CR),中位PFS为14个月,几乎与单药伊布替尼的结果一致。
3、MCL二线治疗总结
• 复发性MCL没有标准的治疗方案。应根据年龄、合并症、临床状况以及先前治疗的反应和毒性采取个体化疗法。(1B)
• 伊布替尼是治疗复发性MCL的最佳选择。(1A)
• 一线治疗复发后,应给予替代化疗方案。(1A)
• 推荐以利妥昔单抗为基础的免疫化疗方案(1A),推荐利妥昔单抗与新的靶向药物联合使用(1B)。但复发后利妥昔单抗维持治疗的作用不明。
四、MCL的干细胞移植
1、自体造血干细胞移植(ASCT)
针对TBI预处理方案在治疗中的作用的研究,只有回顾性分析,有假说认为,TBI预处理方案可以使ASCT治疗前已经达PR的患者受益。然而,目前还没有适合MCL患者的最佳ASCT预处理方案。多项研究表明,一线治疗行ASCT结果会更好。ASCT治疗相关副作用与年龄相关。60岁以上接受ASCT治疗的患者发生与移植相关的死亡率为10%,而60岁以下为3%。因此,当考虑对60岁以上的患者行ASCT治疗时,应对病人进行仔细评估。一项研究表明,ASCT一线治疗后序贯利妥昔单抗维持治疗3年,改善了PFS和OS。另一项大型前瞻性随机试验表明,接受利妥昔单抗维持治疗组的4年PFS和OS分别为83%和89%,对照组分别为64%和80%。因此,我们建议在ASCT后进行利妥昔单抗的维持治疗。
2、异基因造血干细胞移植(AlloSCT)
AlloSCT理论上具备干细胞移植的优势,既不受淋巴瘤细胞的污染,也不受诱导药物的破坏,并可能具有移植物抗淋巴瘤的效应。但是,有关一线AlloSCT治疗的数据很少,所以在高危患者中,AlloSCT疗效是否比ASCT更好仍有待确定。因此,一线AlloSCT治疗仅应用于临床研究中。
在复发及接受过ASCT治疗的患者中,应用AlloSCT的数据相对较多。结果表明,在疾病晚期进行AlloSCT治疗的结果不如早期好。然而,经ASCT治疗后复发的患者,甚至那些难治性患者,AlloSCT可能会延长PFS,这意味着少数高危患者可能会被治愈。目前无标准的预处理方案。AlloSCT治疗的时机也需要进一步的评估。
3、MCL干细胞移植推荐
• 所有适合强化治疗的患者,推荐ASCT作为一线治疗。应对60岁以上的患者进行彻底地评估。 (1A)
• 达到CR的患者行ASCT巩固治疗获益可能性更大。(1A)
• 虽然目前没有足够的证据表明ASCT能够明显改善总生存率,但确实可以显著延长疾病反应的持续时间。(1A)
• 建议ASCT后序贯利妥昔单抗维持治疗。(1A)
• 对于有合适供体的健康患者,可以考虑在第二次缓解期内进行AlloSCT。预处理方案的强度应根据患者的情况进行选择。(1C)
• AlloSCT对ASCT后复发的患者有效。(1B)
• AlloSCT仅在高危患者和临床试验的情况下作为一线治疗。(1C)
如需了解更多淋巴瘤的前沿信息
请扫描二维码访问 “淋巴瘤亿刻 ”网站。

 热门推荐
MORE
热门推荐
MORE

专家“亿”周谈——直击伊布替尼,纵观CLL治疗从免疫化疗到个体化靶向疗法的革新
07-09
J HEMATOL ONCOL:前瞻性研究预测伊布替尼治疗过程中房颤的发生
07-19
CANCER CHEMOTH PHARM :PH调节剂奥美拉唑对伊布替尼影响几何?
08-08
以数据为准绳,中国新药亟需更多原始创新!——首创BTK抑制剂伊布替尼原研专家潘峥婴专访
09-30
欧洲血液学杂志:TEC与BTK抑制剂出血副作用无关
10-22
2018年IWWM 会议现场直达:伊布替尼治疗华氏巨球蛋白血症突破性进展!
11-02
专家“亿”周谈—— J CLIN ONCOL:伊布替尼单药治疗症状型/初治型华氏巨球蛋白血症的最新突破
04-09
BLOOD:基于伊布替尼的联合方案治疗复发/难治CNS淋巴瘤效果显著
05-14
专家“亿”周谈——NEJM:伊布替尼联合维奈托克一线治疗慢性淋巴细胞白血病
06-12
【2019 ICML】黄慧强教授点评:IR联合短疗程R-HYPERCVAD / MTX在初治年轻MCL患者中有效性显著
06-20
【2019 EHA】纵览伊布替尼联合用药进一步提升CLL疗效
06-24
【2019 ICML】邱录贵教授点评:伊布替尼治疗华氏巨球蛋白血症的最新进展
06-25
【2019 ICML】张会来教授点评:伊布替尼联合利妥昔单抗治疗MCL疗效显著
06-25
【2019 ICML & EHA 回顾】中外专家畅谈伊布替尼治疗淋巴瘤的前沿进展
07-09Copyright 2008-2019 梅斯(MedSci)备案号 沪ICP备14018916号-1
