FDA:如何规范考虑植物药的开发(上)
2017年国家药品改革政策“流星雨”,不仅个大还很炫,已经波及到中药品种,目前已经降生的中药注射剂剂再评价仅仅只是个开端。
药渡 - 植物药,FDA,药物开发 - 2017-11-14
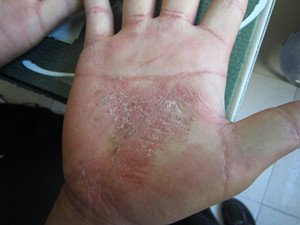
FDA批准银屑病治疗药Taltz
美国FDA批准Eli Lilly的Taltz (ixekizumab) 来治疗中度至重度斑块状银屑病。银屑病是一种皮肤发红和剥落的皮肤状况。FDA 的药物评价和研究中心办公室主任医学博士Julie Bei
睿医 - FDA,银屑病 - 2016-03-24
KL1333获FDA孤儿药认定
NeuroVive制药公司的实验性药物KL1333近日获得了FDA孤儿药物认定资格,用于治疗遗传性线粒体呼吸链疾病(MRCD),线粒体病是遗传缺损引起线粒体代谢酶缺陷,致使ATP合成障碍、能量来源不足导致的一组异质性病变
MedSci原创 - FDA,KL1333,线粒体呼吸链疾病 - 2018-04-23
瑞德西韦获得FDA孤儿药认定
根据美国《金融邮报》的报道,FDA已授予吉列德科学(Gilead)公司的实验性药物瑞德西韦(remdesivir)孤儿药认定,以作为COVID-19的潜在治疗药物。
MedSci原创 - 瑞德西韦,Covid-19,COVID-19肺炎,孤儿药 - 2020-03-24
辉瑞抗癌药Xalkori获FDA正式批准
辉瑞(Pfizer)11月21日宣布,抗癌药物Xalkori(crizotinib)获得了FDA的正式批准,用于经FDA批准的一款检测试剂盒证实其肿瘤为间变性淋巴瘤激酶(ALK)阳性的转移性非小细胞肺癌出于ALK阳性NSCLC患者对新药迫切需求的考虑,FDA于2011年8月授予了Xalkori加速批准(accelerated approval)。 肺癌是癌症致死
生物谷 - 新药,FDA - 2013-11-26
FDA拒绝Mylan的Advair Diskus非专利药
该公司透露,它收到了美国食品和药物管理局(fda)的一份最新报告,指出申请中存在"小缺陷",并将在本月晚些时候发出完整的回复信。有关缺陷的进一步细节没有透露。
MedSci原创 - Mylan,Advair,Diskus - 2018-06-14
FDA群体药代动力学
本指南旨在帮助新药申请 (NDA)、生物制品许可申请 (BLA)、简化新药申请 (ANDA) 和研究性新药 (IND) 申请的申办者和申请人在群体药代动力学 (PK) 分析中的应用 . 群体 PK 分
FDA - 药代动力学 - 2022-03-16
FDA批准降糖药empagliflozin上市
8月1日,美国食品与药物管理局(FDA)批准了empagliflozin片剂用于辅助改善饮食和运动控制不佳的2型糖尿病成人患者的血糖水平。FDA相关人员表示,该药可单独或作为整体降糖方案中的补充治疗。 Empagliflozin是钠葡萄糖共同转运蛋白2(SGLT2)抑制剂。FDA相关通告写道,该药不应用于以下类型患者:1型糖尿病、血或尿酮体升高(糖尿病酮症酸中毒)、严重肾脏损害、终末期肾病或
医学论坛网 - FDA,降糖药,empagliflozin - 2014-08-05
2016年创新中药及植物药国际峰会即将盛大开幕
不详 - 美通社 - 2016-11-10
FDA批准首个治疗耐多药结核病药上市
2012年12月28日,美国食品与药物管理局(FDA)通过加速审批程序批准了Sirturo(bedaquiline,双芳基喹啉类抗结核药)在无其它替代药物可用时作为成人多重耐药的结核(TB)联合治疗的组成部分该药通过抑制人体内结核杆菌复制和播散所需的酶而发挥作用。 Sirturo的说明书和标签中带有加框
医学论坛网 - 多重耐药结核,TB,bedaquiline - 2013-01-04
APASL 2014:中国植物药—肝纤维化治疗的新方法
John Vierling教授于3月14日在APASL 2014上就中药制剂“扶正化瘀片”对减少大多数患者肝脏纤维化程度的能力所进行的II期临床试验进行汇报,研究发现该药能改善患者的恢复,减缓肝脏纤维化进展
dxy - 植物药,肝纤维化 - 2014-03-24
盘点:2014年FDA批准的孤儿药
1982年,美国的罕见病家庭和支持团体成立了一个“非正式联盟”,呼吁立法支持孤儿药和治疗罕见病的药物研发,1983年,这个组织成功使美国国会通过了“孤儿药法案”,该法案制定了发展孤儿药的诸多激励性措施30多年过去了,FDA共认证近3000个孤儿药,获批的有400多个,涉及447种罕见病的治疗。在其2013年批准的27个新药中,也有10个是孤儿药。下面就让我们细数2014年1月至今FDA批
咸达数据 - 孤儿药,罕见病 - 2014-09-26
FDA批准新抗孕吐药Diclegis上市
2013年4月8日,美国食品与药物管理局(FDA)批准了Diclegis缓释片【有效成分为琥珀酸多西拉敏(doxylamine succinate)和维生素B6】用于治疗妊娠女性的恶心和呕吐。 该药预期用于那些经保守治疗(如饮食和生活方式调整)无效的妊娠期女性恶心和呕吐。
MedSci原创 - 抗孕吐药,Diclegis,恶心,呕吐 - 2013-04-10
中国肝癌治疗药物获FDA孤儿药资质
小编提示:这仅仅是获得YS-ON-001取得肝癌治疗的孤儿药资质,并不是批准上市。能否正式上市成功,还要看后期的临床试验结果。10月24日,依生生物制药有限公司宣布,美国食品和药物管理局(FDA)已经正式批准其主打产品YS-ON-001取得肝癌治疗的孤儿药资质。
科学网 www.sciencenet.c - 生物,制药 - 2016-10-25
FDA 顾问小组建议批准减肥药Qnexa
FDA的内分泌恩和代谢药物委员会建议批准VIVUS公司的减肥药Qnexa上市,委员会以20票赞成,2票反对建议品准其上市。“对于专家们的结果支持Qnexa的安全性和有效性的建议批准,我们很高兴”,VIVUS公司总裁Peter Tam说道, “我们期待与FDA的进一步工作以完成他们对该药的评价。
MedSci原创 - FDA,减肥药,Qnexa - 2012-02-26
为您找到相关结果约500个