临床前研究验证性研究发表难题
临床前研究结果可重复性差,但是对这些研究进行重复似乎缺乏动力,只有一些比较重大的突破性研究,如那些发表在重要学术期刊上的,有潜在应用价值的研究,会受到医药公司的重视和重复。但是医学临床前研究的结果重复发表难问题已经
科学网博客园 - 临床研究 - 2016-02-05
Neurology:临床前和前驱认知障碍阶段的临床相关变化
MCIDs可应用于临床实践或临床试验,以确定是否发生了临床相关的变化
MedSci原创 - 老年痴呆症,轻度认知障碍 - 2022-09-14
Moderna正在临床前阶段研究mRNA猴痘疫苗
周一,又有五个国家报告了首例猴痘确诊病例,使今年报告猴痘疫情的国家总数达到17个。截至上周六,世界卫生组织(WHO)报告了12个国家5月13日至21日至少92例实验室确诊病例。另有28例疑似病例正在接
网络 - 猴痘疫苗 - 2022-05-25
Aspetar临床实践指南:前交叉韧带重建术后康复
本指南是为指导前交叉韧带重建术(ACLR)后的临床康复实践而制定的,根据研究与评估指南II(Agree II)的评估工具执行,并使用建议分级、评估、发展和评估(GRADE)方法。指南制定小组利用随机临
Br J Sports Med - 前交叉韧带损伤,前交叉韧带重建术 - 2023-02-07
学者热议如何提高临床前研究的重现性
科学具有自我纠错能力,但这一原理在动物实验研究方面遭受打击,这一问题已受到科学家和民众的广泛关注,促使NIH为纠正这一问题建立新的指导原则。学术不端肯定是导致这一问题的一个因素,估计有大量造假论文在海量论文掩护下顺利发表。自从去年NIH倡议采取各种措施解决这个问题以来,尤其是发布“NIH重复研究指南”,是否有成效不清楚,有一些学术期刊支持,也有一些学术期刊认为这个指南增加了工作的复杂性,而
科学网 - 重复研究,实验研究 - 2015-04-22
2018 ASHM临床指南:HIV暴露前预防(更新版)
2018年4月,澳大利亚艾滋病医学会(ASHM)更新发布了HIV暴露前预防指南,HIV感染高危人群日常联合应用替诺福韦和恩曲他滨进行暴露前预防在美国,欧洲以及澳大利亚和WHO指南中均有推荐。本文是对2017版指南的更新,针对每日用药和按需用药进行HIV暴露前预防的建议进行修订。
J Virus Erad. 2018 A - HIV暴露前预防 - 2018-04-30
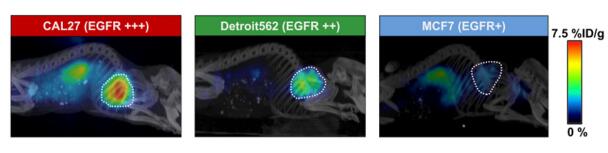
多模PET成像为临床前肿瘤学提供新见解
为患者提供更个性化的癌症治疗的需求,正推动着临床前PET肿瘤研究的发展。众多的肿瘤类型及其对不同治疗手段的反应不一,使得对有效治疗癌症方法的探求变得极具挑战。
医谷 - 肿瘤,PET成像 - 2019-09-02
2022 AAOS临床实践指南:前交叉韧带损伤的管理(概要)
本临床实践指南基于循证对已发表的治疗骨骼成熟和未成熟患者前交叉韧带受伤的研究进行系统综述,提出前交叉韧带损伤的处理的8项建议和7选项,以帮助整形外科医生和所有医生根据现有最佳证据管理前交叉韧带损伤患者
J Am Acad Orthop Surg - 前交叉韧带损伤 - 2023-02-07
前交叉韧带损伤处理相关国际指南解读及其临床应用
前交叉韧带损伤是一种常见的膝关节运动损伤。前交叉韧带损伤后的病人往往需要及时、有效的医学干预。但是目前临床医生在前交叉韧带损伤诊断、手术指征选择、手术方式、移植物类型、术后康复方案以及重返运动评估方面
中华关节外科杂志(电子版) - 关节,前交叉韧带损伤,前交叉韧带 - 2022-02-28
2016 循证临床实践指南:前交叉韧带康复
2016年8月,荷兰皇家物理治疗学会(KNGF)指示前交叉韧带多学科专家组制订发布了前交叉韧带重建后康复共识,主要内容涉及前交叉韧带术前康复,术后康复,返回治疗标准。
Br J Sports Med. 2016 Aug 18. - 前交叉韧带,康复 - 2016-08-24
2018 ASHM临床指南:HIV暴露前预防(更新版)
2018年4月,澳大利亚艾滋病医学会(ASHM)更新发布了HIV暴露前预防指南,HIV感染高危人群日常联合应用替诺福韦和恩曲他滨进行暴露前预防在美国,欧洲以及澳大利亚和WHO指南中均有推荐。本文是对2017版指南的更新,针对每日用药和按需用药进行HIV暴露前预防的建议进行修订。
J Virus Erad. 2018 Apr 1;4(2):143-159. - HIV暴露前预防 - 2018-04-30
神经精神数据认同临床前阿尔茨海默病
亚利桑那州斯科特市梅奥医院的Caselli医生说:“在过去的一两年间,临床前阿尔茨海默病的概念备受关注,脑脊液内生物标记物和淀粉样抗原水平等检测的发展进一步推动了这一观念我们已经认识到,临床
网络 - 临床前阿尔茨海默病 - 2012-08-13
抗体偶联药物质量控制和临床前评价专家共识
本专家共识对人用抗体偶联药物(ADC)的生产制造、质量控制和临床前评价提出指导性意见,旨在为ADC研发者提供技术参考。ADC作为创新性抗体药物,应按照国内外对于创新药研发及申报的相关技术要求,在保证临床基本安全性的前提下分阶段、有步骤地开展研究;企业应根据ADC研发生命周期的规律在不同研发阶段到上市批准的过程中采用基于科学和风险评估的开发策略
中国药事.2018,32(7):993-1004. - :,抗体偶联药物,质量控制,临床前评价 - 2018-08-10
为您找到相关结果约500个