鉴于感染风险及肾毒性:FDA拒绝golodirsen治疗杜兴氏肌肉营养不良症
Sarepta Therapeutics宣布,FDA发布了一份完整的回复函,拒绝了golodirsen治疗杜兴氏肌肉营养不良症(DMD)的申请。
MedSci原创 - golodirsen,感染风险,肾毒性 - 2019-08-21
10月这3家生物公司面临着FDA的重大决定
生物制药行业事件的催化作用很大。例如,近日Axovant公司(AXON)宣布旗下阿尔茨海默病治疗药物intepirdine的三期试验未达其主要终点,受此利空消息影响,公司股票下跌了近75%。本文汇总了10月份面临着美国食品和药物管理局重大决定的三家公司,同样地,FDA给出的最终结果将会对公司股价和未来的发展起到很强的影响作用。
新浪医药新闻 - 生物公司,FDA,重大决定 - 2017-10-10
外显子跳跃疗法Vyondys 53治疗Duchenne肌营养不良症
FDA近日批准了Sarepta Therapeutics的Vyondys 53(golodirsen)的加速审批,用于治疗Duchenne肌营养不良症(DMD)且存在肌营养不良蛋白基因突变的患者。
MedSci原创 - Vyondys,53,外显子跳跃疗法,Duchenne肌营养不良症 - 2019-12-13
Sarepta公司第3款反义寡核苷酸疗法获FDA批准上市
2月25日,罕见病精准基因治疗领域领导者Sarepta公司宣布,FDA已批准反义寡核苷酸药物AMONDYS 45 (casimersen)上市,用于45外显子跳跃突变杜氏肌营养不良症(DMD)患者治疗
医药魔方 - 罕见病 - 2021-02-28
基因疗法为攻克罕见病DMD带来新希望?礼来砸下1.35亿美元进场
礼来与基因编辑公司Precision BioSciences达成一项合作,开启了对杜氏肌营养不良(DMD)基因疗法的布局。
网络 - 基因疗法,礼来,DMD - 2020-12-05
2019年上半年获批新药中的“首例”
根据FDA药物评估和研究中心(CDER)的数据统计,2019年上半年,FDA总计批准了13款创新药。这一统计并不包括基因和细胞疗法。而FDA生物制剂评估和研究中心(CBER)的数据表明,2019年上半年,FDA还批准了一款基因疗法和一款疫苗。今年获批的新药中有多个“首例”。今天药明康德内容团队将从这些“首例”中,与读者分享药物开发和审评的一些趋势。▲2019年上半年获批新药和疫苗(数据来源:F
药明康德 - 新药,FDA - 2019-07-03
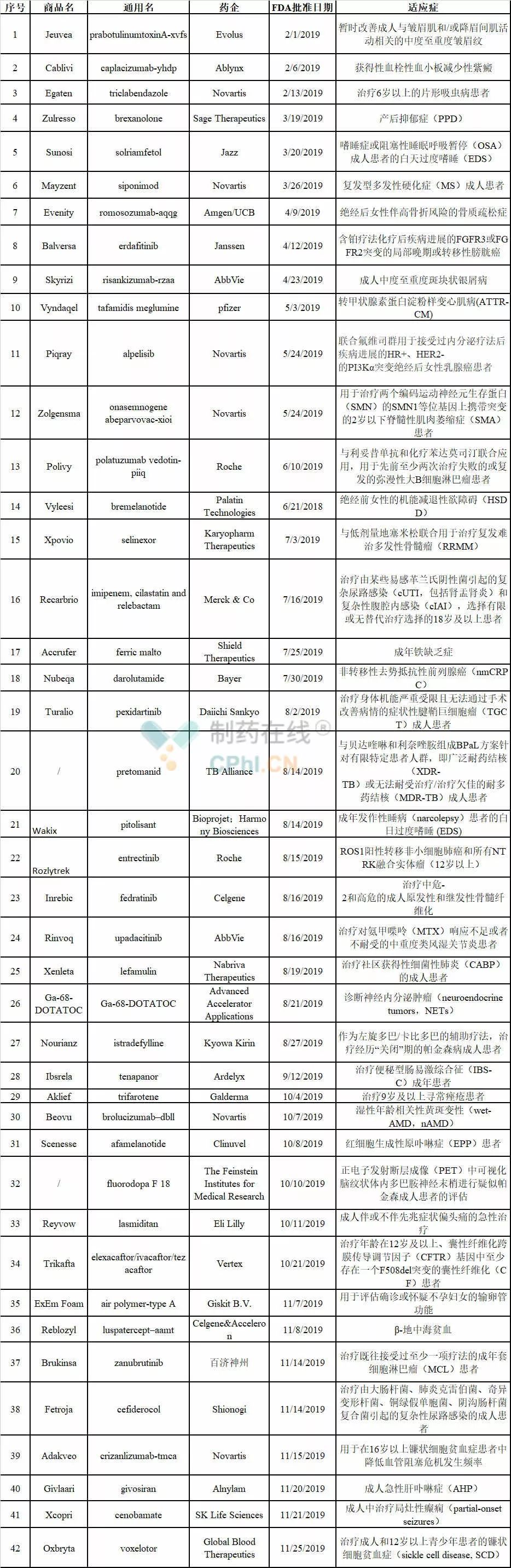
FDA 2019:批准45款新药,9款生物类似药
美国FDA的药物评估与研究中心(CDER)已经批准42款新药,9款生物类似药,3款在路上,而生物制品评估与研究中心(CBER)也批准了诺华公司的基因疗法Zolgensma和首款登革热疫苗。另外还有3款新药的PDUFA时间在12月,预计2019年将有45款新药获得FDA批准。相较于2017年和2018年,2019年会是FDA批准新药数量最低的一年,但质量不差,比如Skyrizi、Zolgensm
MedSci - FDA,新药 - 2019-12-24
FDA:2021年共批准49个新药
2021年以来,美国食品药品监督管理局(FDA)下设的药审中心(Center for Drug Evaluation and Research, CDER)批准了49个新药(New Molecular
美柏医健 - FDA - 2021-12-29
为您找到相关结果约8个