血管内超声指导腔内治疗肾动脉夹层一例
2019-07-11 韩林 吴小燕 干学东 影像诊断与介入放射学
患者,女,36岁,因“突发咯血4h”入院。患者于4h前突发咯血,为鲜血夹带少量血凝块,总量约50ml,伴心慌、胸闷,无腹痛、腰痛、发热。否认高血压、结缔组织疾病及血管炎病史,无腹部创伤史及血管介入治疗史。无吸烟、饮酒史。查体:心率120次/分,血压199/132mmHg(1mmHg≈0.133kPa),腹平软,无压痛及反跳痛,双肾区无叩痛。
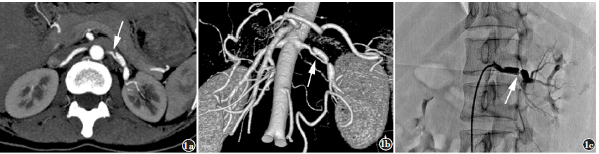
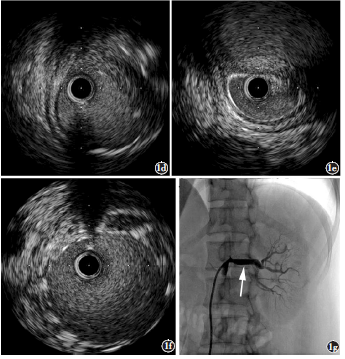
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#肾动脉#
44
#肾动脉夹层#
37
#动脉夹层#
44
#腔内治疗#
47