Nature Aging:南京大学丁利军/孙海翔/李朝军等合作发现卵母细胞减数分裂缺陷和非整倍体的调控新机制
2023-05-18 iNature iNature 发表于上海
该研究证明了GCs中的MVA通路是卵母细胞减数分裂成熟和整倍性的关键调节因子,而年龄相关的MVA通路异常导致卵母细胞的减数分裂缺陷和非整倍性。
随着年龄的增长,卵母细胞减数分裂过程中的异常现象变得更加普遍。然而,与衰老相关的卵母细胞非整倍体的机制尚不完全清楚。
2023年5月15日,南京大学丁利军、孙海翔、李朝军及上海交通大学卞迁共同通讯在Nature Aging在线发表题为“Granulosa cell mevalonate pathway abnormalities contribute to oocyte meiotic defects and aneuploidy”的研究论文,该研究表明颗粒细胞的甲羟戊酸途径异常会导致卵母细胞减数分裂缺陷和非整倍体。该研究揭示了来自老年小鼠的中期I卵母细胞中染色体凝聚减少和减数分裂相关基因表达中断。转录组学分析表明,年轻卵母细胞的减数分裂成熟与卵母细胞周围颗粒细胞(GCs)中甲羟戊酸(MVA)通路基因表达的显著增加有关,而老年颗粒细胞中甲羟丙酸通路基因表达在很大程度上下调。
他汀类药物对GCs中MVA代谢的抑制导致年轻卵丘-卵母细胞复合体中明显的减数分裂缺陷和非整倍体。相应地,补充MVA类异戊二烯香叶醇可以改善衰老小鼠的卵母细胞减数分裂缺陷和非整倍体。从机制上讲,作者发现香叶醇激活了衰老GCs中的LHR/EGF信号传导,并增强了卵母细胞中减数分裂相关基因的表达。总之,该研究证明了GCs中的MVA通路是卵母细胞减数分裂成熟和整倍性的关键调节因子,而年龄相关的MVA通路异常导致卵母细胞的减数分裂缺陷和非整倍性。

卵巢是生殖器官,在产生成熟卵母细胞和分泌性激素方面具有关键功能。近几十年来,首次怀孕的年龄不断增加。然而,35岁以上的人卵巢功能显著下降 ,表现为卵巢储备减少和卵母细胞质量下降。这些变化主要是由减数分裂缺陷引起的,尤其是非整倍体。33岁后,非整倍体中期II(MII)卵母细胞的比例从23.6%迅速增加到53.5% 。然而,卵母细胞中与衰老相关的减数分裂缺陷和非整倍体的机制仍有待阐明,目前还没有有效的方法来保持卵母细胞减数分裂随年龄的保真度。
正常卵母细胞生长是一个复杂的生物过程,其特征是卵母细胞和邻近颗粒细胞(GCs)的动态转录调节。GCs为卵母细胞的生长和成熟提供糖酵解和胆固醇生物合成的产物以及氨基酸。表皮生长因子(EGF)信号传导通过将黄体生成素(LH)信号从GCs传递到卵母细胞,在卵母细胞减数分裂恢复中发挥关键作用。以前的一些研究表明,卵巢衰老与卵母细胞-GCs相互作用的破坏有关,从而导致卵母细胞减数分裂过程紊乱。
单细胞转录组学和全基因组染色质构象捕获(Hi-C)技术的最新进展为在系统水平上探索卵巢衰老过程中转录和染色质结构的变化提供了前所未有的机会。尽管先前的研究已经对不同年龄的卵母细胞和GCs的转录组进行了表征,但在整个减数分裂过程中,与衰老相关的转录组变化与配对卵母细胞或GCs的信号传输之间的关系尚未得到明确的研究。
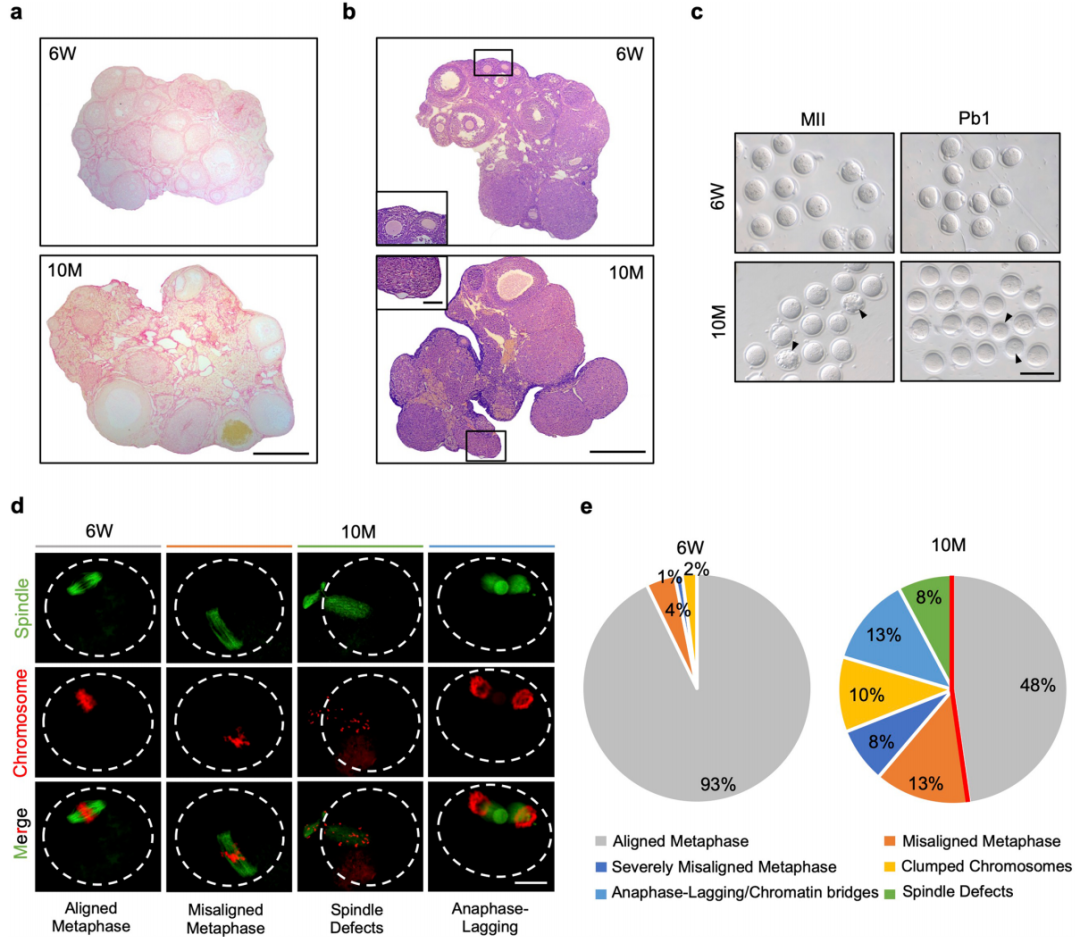
衰老卵巢中卵泡储备减少和减数分裂缺陷(Nature Aging )
该研究通过年轻和老年小鼠卵母细胞和周围GCs在不同减数分裂阶段的转录组景观揭示了GCs中MVA通路在诱导卵母细胞减数分裂成熟中的作用。衰老GCs中MVA通路的下调导致MI处减数分裂相关基因表达受到抑制,这解释了卵巢衰老过程中卵母细胞的染色体异常、减数分裂缺陷和非整倍性。卵巢衰老过程中卵母细胞和GCs之间的MVA代谢偶联和信号转导为衰老卵母细胞非整倍体的机制提供了见解,为临床卵母细胞质量评估和卵巢衰老诊断提供了潜在的生物标志物,并为临床提高卵母细胞的质量提出了新的靶点。
原文链接:
https://www.nature.com/articles/s43587-023-00419-9
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














签到学习
38
好
29