施一公团队发现APOE4受体,揭示阿尔茨海默病最强风险因子致病原因
2023-01-02 生物世界 生物世界 发表于上海
首次在结构上阐明APOE结合受体复合物,揭示了关于APOE亚型特异性和受体介导信号的线索。
载脂蛋白E是主要的脂质载体之一,负责将脂质运送到细胞和组织中,以调节血脂水平。而这种APOE亚型依赖的潜在机制仍然是谜。

APOE的免疫调节作用最初是作为血浆脂蛋白对T细胞增殖抑制作用的一部分被发现的。APOE蛋白抑制T细胞增殖和中性粒细胞激活,调节巨噬细胞功能,促进脂质抗原呈递,调节炎症和氧化。例如,多发性硬化症(MS)患者的APOE4会加速脑组织功能丧失,导致早期认知障碍。
此外,APOE不同亚型在神经学和神经退行性疾病如阿尔茨海默病(AD)中也发挥着重要作用。例如,APOE4能够显著增加阿尔茨海默病发病风险,是阿尔茨海默病最强的遗传风险因子,40%-50%的阿尔茨海默病患者都存在APOE4。当有一个拷贝的APOE4时,阿尔茨海默病患病风险将增加3倍,当两个拷贝都是APOE4时,患病风险将提高8-12倍。而APOE2则能够显著降低阿尔茨海默病风险。
之前的研究表明APOE在β-淀粉样蛋白(Aβ)沉积中发挥作用,此外,许多研究证据显示免疫系统功能障碍在阿尔茨海默病病理中发挥关键作用。特别是小胶质细胞的异常激活,导致神经毒性细胞因子释放和突触修剪,与记忆丧失和阿尔茨海默病的发展有关。在Tau蛋白病小鼠模型中,与APOE2相比,敲入APOE4基因会导致小胶质细胞明显更强的激活。
在这项研究中,研究团队确定LilrB3(白细胞免疫球蛋白样受体B3)是APOE4的候选免疫细胞表面受体,而不是APOE2。该研究解析了LilrB3-APOE4二元复合物的平均分辨率为3.0Å的冷冻电镜结构,为LilrB3特异性识别APOE4提供了结构基础。
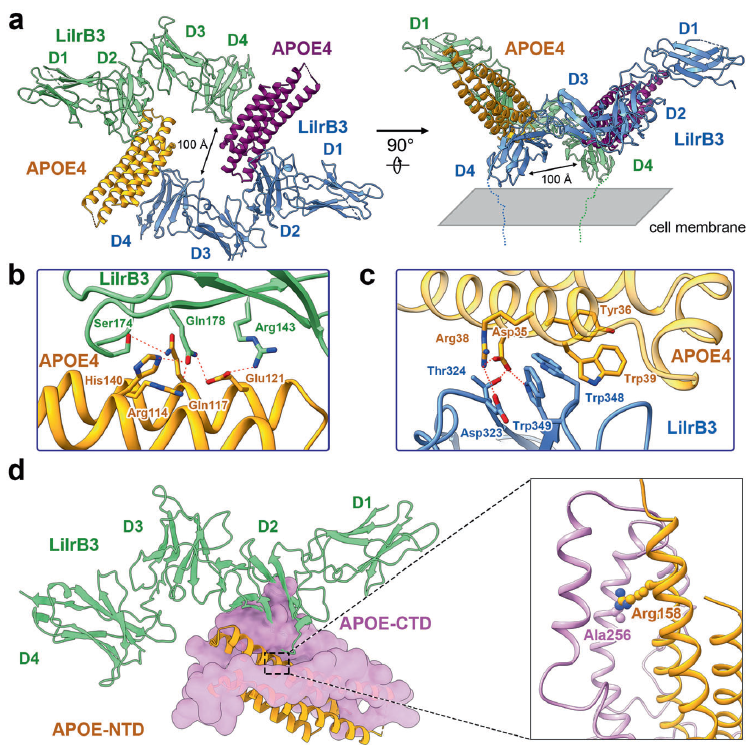
LilrB3识别APOE4的结构基础
这也是首次在结构上阐明APOE结合受体复合物,揭示了关于APOE亚型特异性和受体介导信号的线索。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#施一公#团队发现#APOE4#受体,揭示#阿尔茨海默病#最强风险因子致病原因
68