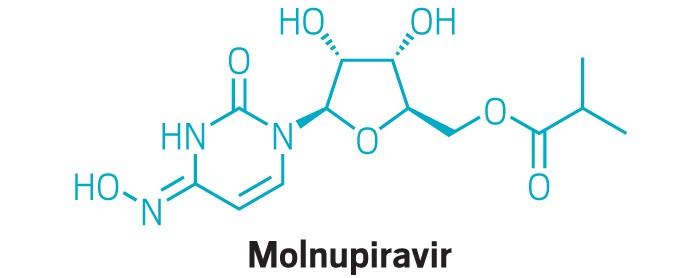
FDA将召开咨询委员会会议,以讨论默克和Ridgeback的COVID-19口服疗法molnupiravir
2021-10-17 Allan MedSci原创
近日,美国食品和药品监督管理局宣布其抗菌药物咨询委员会 (AMDAC) 即将召开会议,以讨论默克和Ridgeback对molnupiravir的紧急使用授权 (EUA) 的申请。
近日,美国食品和药品监督管理局宣布其抗菌药物咨询委员会 (AMDAC) 即将召开会议,以讨论默克和Ridgeback对molnupiravir的紧急使用授权 (EUA) 的申请,molnupiravir是一种用于治疗COVID-19 的研究性抗病毒药物。
11月30日,咨询委员会将召开会议,讨论支持使用molnupiravir治疗COVID-19轻中度患者的决议。
FDA 的药物评价和研究中心,医学博士 Patrizia Cavazzoni 说:“ FDA 正在评估默克和 Ridgeback 在其紧急使用授权请求中提交的安全性和有效性数据,molnupiravir是一种针对新诊断出的COVID-19 感染的高危人群的新型口服治疗药物。我们认为,在这种情况下,与 FDA 咨询委员会对这些数据进行公开讨论将有助于确保清楚了解 FDA 正在评估的科学数据和信息,以决定是否批准该药物的EUA”。
根据 FDA 的判断,该机构可以召集一个咨询委员会,就各种复杂的科学、技术和政策问题征求独立的外部专家的建议。FDA 并不总是召集与 EUA 审查相关的咨询委员会会议,但在某些情况下可能会召开咨询委员会会议,因为与咨询委员会的讨论将有助于为机构决策提供信息。
会议是在公司提交 EUA 请求后尽快安排的。该时间表允许 FDA 在会议之前彻底评估 EUA 请求中提交的数据和信息。在会议期间,委员会将听取公司关于抗病毒药物数据的介绍。在此举行公开听证会期间,公众将有机会发表意见。
FDA 打算在不迟于会议前两个工作日向公众提供 AMDAC 会议的背景材料,包括会议议程和委员会名册。
原始出处:
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言















#默克#
39
溶酶生成后迅速与a2纤溶酶抑制剂1:1结
54