Cancer Discov:过表达BCL-2的CAR-T细胞治疗,“抗癌利器”疗效再提升!
2022-09-25 生物探索 生物探索
作为近几年中抗癌免疫疗法的新宠,CAR-T的有效性陆续得到验证,越来越多的产品开始从临床走向商业化。但是,就目前来说,CAR-T疗法的抗肿瘤效果仍然有待提升。
自2017年首款CAR-T细胞疗法上市以来,细胞治疗时代正式开启,在多种肿瘤治疗中取得了很好的临床效果,B细胞淋巴瘤就是其中一种。但是,需要注意的是,并不是所有患者都能获得良好的治疗效果。超过60%的复发难治性B细胞淋巴瘤患者要么对CAR-T疗法不响应,要么治疗后产生耐受,导致疾病复发。因此,CAR-T疗法的抗肿瘤效果亟待提升。
近日,来自宾夕法尼亚大学的研究团队展开了CAR-T疗法抗肿瘤效果提升的探索,他们发现,抗凋亡蛋白BCL-2抑制剂能够与CAR-T疗法产生协同作用,进而对B细胞淋巴瘤产生更加有效的治疗效果(单独CAR-T治疗对肿瘤的杀伤力在47%-63%,而BCL-2抑制剂与CAR-T联用对肿瘤的杀伤力在75%-88%)。同时,他们也设计制造了过表达BCL-2或者BCL-2(F104L)突变的CAR-T细胞,发现过表达BCL-2不仅可以提升CAR-T细胞对BCL-2抑制剂毒性的抵抗能力,还能增强其抗肿瘤能力。相关研究成果以“Modulation of BCL-2 in both T Cells and Tumor Cells to Enhance Chimeric Antigen Receptor T cell Immunotherapy against Cancer”为题,发表在权威期刊Cancer Discovery上。

图1 研究成果(图源:[1])
在这项研究中,研究人员通过在B细胞前体白血病细胞系(NALM6)中对29个促凋亡药物进行定向筛查,他们发现BCL-2抑制剂是CAR-T细胞疗法的毒性增强剂,能够显著提升CAR-T细胞的肿瘤杀伤功能。在这其中,美国FDA批准的药物venetoclax提升CAR-T细胞肿瘤杀伤能力的作用最强,单独CAR-T对肿瘤的杀伤力在47%-63%,而BCL-2抑制剂与CAR-T联用对肿瘤的杀伤力在75%-88%[1]。
为了研究给药是否会增强CAR-T细胞介导的肿瘤杀伤能力,研究人员使用了两种不同的B细胞淋巴瘤细胞系和一种白血病细胞系OCI-Ly18,这些细胞对venetoclax有不同的敏感性。将CAR-T细胞与DMSO或venetoclax共培养,并在48小时检测细胞毒性,结果表明,venetoclax联合CAR-T治疗导致了肿瘤杀伤能力的大幅提升。
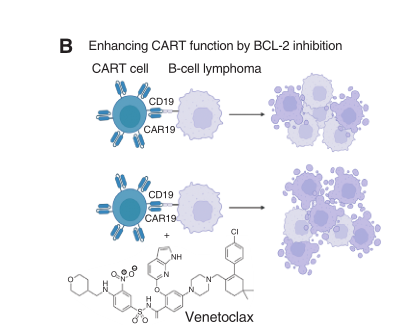
图2 venetoclax与CAR-T联合治疗增强了CAR-T介导的肿瘤杀伤能力(图源:[1])
通过对比接受CAR-T和接受CAR-T/venetoclax联合治疗的动物肿瘤细胞的转录组,研究数据表明,联合治疗通过促进肿瘤细胞凋亡和抑制癌细胞周期来增强CAR-T介导的肿瘤杀伤能力。对此,研究人员表示,联合使用venetoclax和CAR-T细胞可能是改善CAR-T 19治疗venetoclax敏感淋巴瘤的临床结果的一种有希望的策略。
在实验中,研究人员发现高剂量venetoclax的使用会导致对CAR-T细胞的毒性,导致CAR-T细胞抗肿瘤能力不断下降直至消失。为了改变这种情况,研究人员设计出了过表达BCL-2或者BCL-2(F104L)突变的CAR-T细胞,调节CAR-T细胞对venetoclax的耐受力,结果表明过表达BCL-2或者BCL-2(F104L)突变的CAR-T细胞比CAR-T细胞对venetoclax引起的细胞毒性具有更显著的抗性。
在不使用venetoclax的情况下,单独使用过表达BCL-2的CAR-T细胞比常规的CAR-T细胞能产生更强的肿瘤杀伤作用,但是效果不如venetoclax和CAR-T联用的效果明显。在后续实验中,研究人员发现除了降低venetoclax的毒性外,BCL-2(F104L)在CAR-T细胞中的过表达固有地增强了它们在没有venetoclax的情况下控制肿瘤的能力。
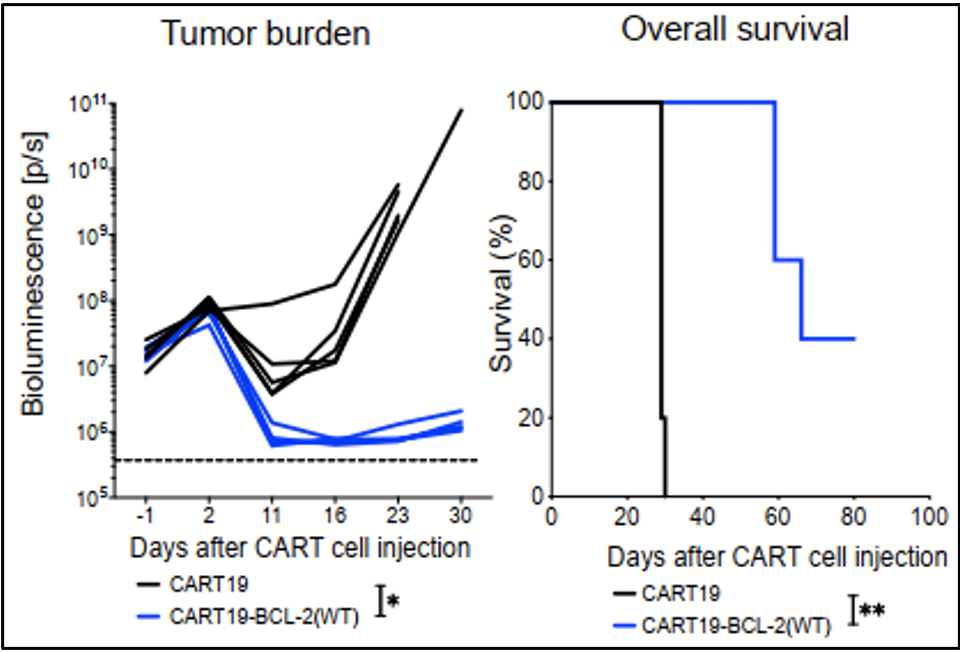
图3 单独使用过表达BCL-2的CAR-T细胞也能控制肿瘤发展(图源:[1])
为了弄清楚BCL-2过表达可能提高CAR-T细胞抗肿瘤活性的机制,研究人员进行了体外和体内CAR-T细胞的功能研究。研究人员发现,BCL-2过表达可以在缺乏细胞因子产生的生存信号的情况下保护CAR-T细胞,可能是通过增强的JAK-STAT生存信号通路。也即,BCL-2介导的细胞凋亡通路,对CAR-T细胞疗法的抗肿瘤能力具有非常重要的调节作用。
此外,研究人员表示,尽管BCL-2过表达使得CAR-T细胞抗淋巴瘤活性的显著提升,但这种方法的关键问题在于其长期安全性。为了解决安全性问题,研究人员设计了一种带有基于抗体介导的自杀基因控制元件的BCL-2过表达CAR-T细胞,同时也证明了其有效性。
综上所述,研究人员提出并证实了通过调节CAR-T细胞和肿瘤细胞的BCL-2信号通路,来提高CAR-T细胞抗肿瘤效果这一新的治疗思路。
参考资料:
[1]Lee YG, Guruprasad P, Ghilardi G, et al. Modulation of BCL-2 in both T Cells and Tumor Cells to Enhance Chimeric Antigen Receptor T cell Immunotherapy against Cancer. Cancer Discov. 2022 Jul 29:CD-21-1026. doi: 10.1158/2159-8290.CD-21-1026. Epub ahead of print. PMID: 35904479.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言