PNAS:浙江大学张海涛团队揭示人胃泌素释放肽受体结合拮抗剂和激动剂结构
2023-02-07 iNature iNature 发表于上海
胃泌素释放肽受体( GRPR )是蛙皮素( BBN ) G蛋白偶联受体中的一员,在多种恶性肿瘤中异常高表达,包括乳腺、前列腺、胰腺、肺和中枢神经系统。此外,它还介导小鼠的非组胺性瘙痒和病理性瘙痒。
胃泌素释放肽受体( GRPR )是蛙皮素( BBN ) G蛋白偶联受体中的一员,在多种恶性肿瘤中异常高表达,包括乳腺、前列腺、胰腺、肺和中枢神经系统。此外,它还介导小鼠的非组胺性瘙痒和病理性瘙痒。因此,GRPR可能是癌症和瘙痒治疗的一个潜在靶点。
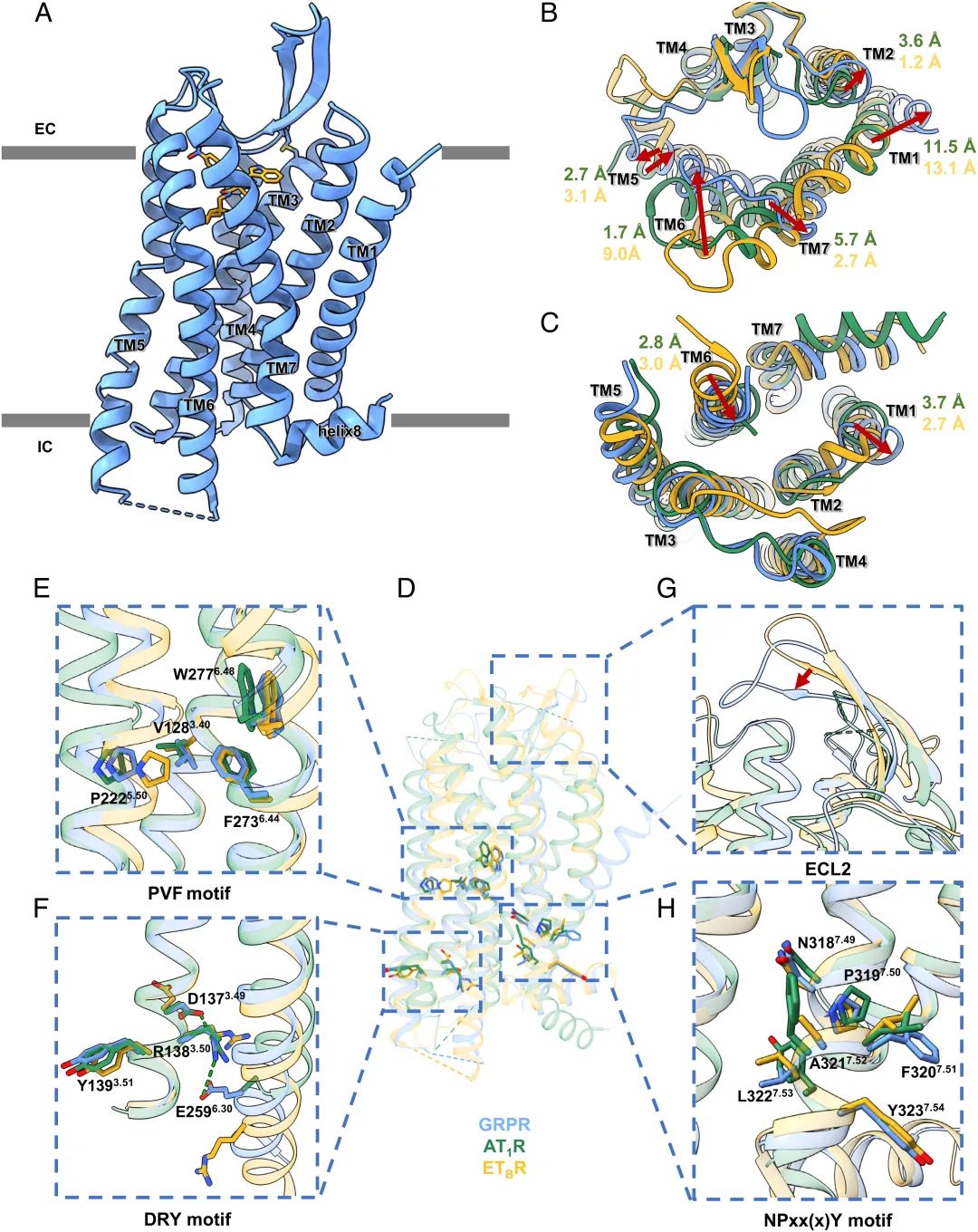
2023年2月1日,浙江大学张海涛团队在PNAS 上在线发表题为“Structures of human gastrin-releasing peptide receptors bound to antagonist and agonist for cancer and itch therapy”的研究论文,该研究报道了人GRPR与非肽类拮抗剂PD176252复合物的非活性状态晶体结构,以及GRPR与内源性肽类激动剂胃泌素释放肽和人工合成的BBN类似物[ D-Phe6 , β-Ala11 , Phe13 , Nle14]Bn ( 6-14 )结合后与Gq异三聚体复合物的两种活性状态冷冻电镜结构。
总之,这些结构揭示了GRPR的配体结合、受体激活和Gq蛋白信号传导的分子机制,有望加速基于结构的GRPR拮抗剂和激动剂的设计,用于癌症和瘙痒的治疗。

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言