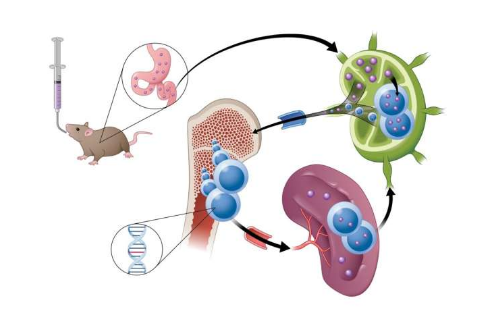
Science:分解蛋白质供能,饥饿的癌细胞是如何转换“食物”来源的?
2022-09-18 网络 网络
这项研究结果揭示了 LYSET 和 M6P 途径对依赖溶酶体分解代谢产生营养素的细胞基本功能,并证明该途径对癌细胞特别重要。因此,这一途径有望成为攻击癌症主要代谢瓶颈的分子切入点。
众所周知,营养素是不可或缺的资源,为满足哺乳动物细胞生长和存活提供了能量。在营养丰富的情况下,细胞会通过质膜转运氨基酸来优先满足自身对外源氨基酸的需求。但大多数循环中的细胞外都是蛋白质,它们会通过巨胞饮和溶酶体分解代谢在细胞内分解为氨基酸。利用胞外这些丰富的蛋白质储备,细胞可以在饥饿期间维持生命。
与正常细胞相比,癌细胞通常会在营养匮乏的环境中生长。为此,它们必须改变代谢以支持其更多的能量需求。最显着的变化是肿瘤糖酵解增加,进而导致葡萄糖摄取和利用增加。这也是一个世纪以来 Warburg 效应的核心概念。
然而,越来越多的研究发现,如氨基酸、乳酸、乙酸和大分子等非葡萄糖营养素也在被癌细胞用作替代能量。这些恶性细胞中与巨胞饮和溶酶体分解代谢相关的信号途径都会上调。由此产生的胞外蛋白质摄取和溶酶体分解增加构成了另一种氨基酸来源,使癌细胞能在营养缺乏的肿瘤环境中生长。这意味着,癌细胞也如同正常细胞一样,在饥饿期间确保自身不会缺乏“食物”。然而,使它们发生这种转变的机制在很大程度上仍是未知的。
2022年9月8日,德国癌症研究中心的 Wilhelm Palm 和奥地利维也纳分子病理研究所 Johannes Zuber 领导的国际研究团队在国际顶尖学术期刊 Science 上发表了题为:Lysosomal enzyme trafficking factor LYSET enables nutritional usage of extracellular proteins 的研究论文。
癌细胞通常在营养含量低的环境中生长,它们通过将新陈代谢转变为使用蛋白质作为“食物”来源来应对这一挑战。这项最新研究表明,一种名为 LYSET 的蛋白质是允许癌细胞进行这种代谢转换的关键。这项研究也为癌症治疗提供了一个新靶点。

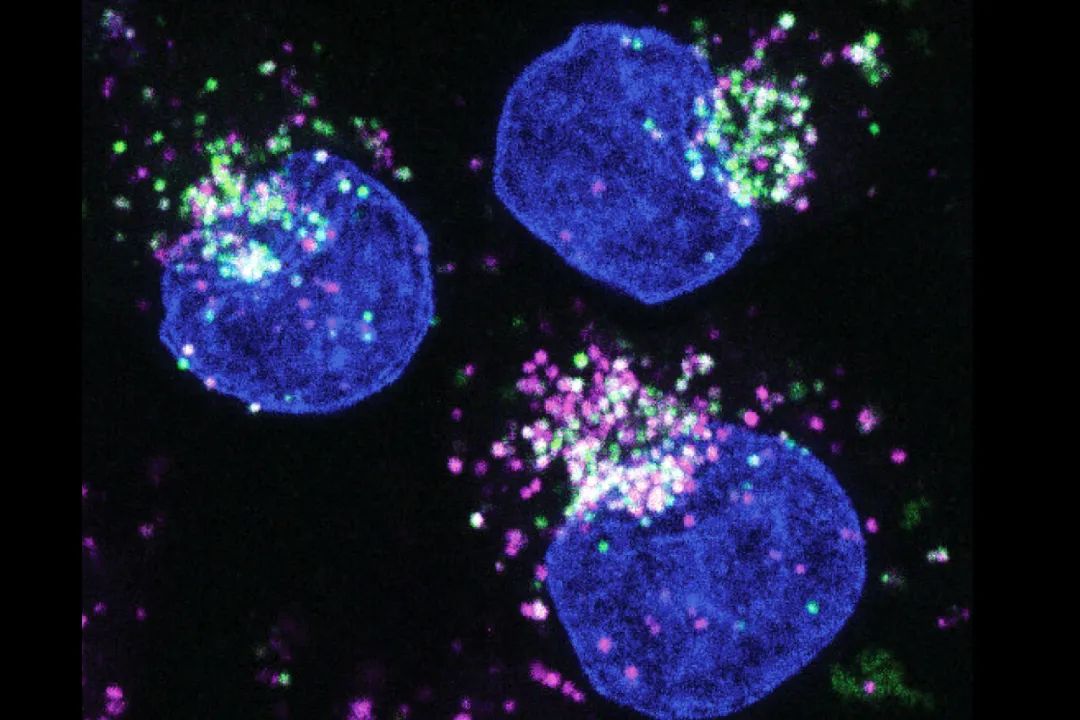
以蛋白质(绿色标记)为食的人类癌细胞(蓝色为癌细胞的细胞核),蛋白质在溶酶体中被消化并分解成氨基酸(洋红色)
氨基酸是蛋白质的组成部分,也是细胞生长和增殖的关键营养素。了解细胞如何在不同环境中利用氨基酸是基础生物学和癌症研究的一个核心问题。
Wilhelm Palm 实验室是最早描述癌细胞具有以细胞外蛋白质为食的能力的实验室之一。在这项新研究中,为了更好地理解癌症中营养转换的分子途径,研究团队建立了筛选条件,在该条件下细胞生长可以摄取单体氨基酸,或通过细胞外蛋白质的巨胞饮作用和溶酶体分解代谢得到支持。为了有选择地强化任何一种营养获取途径,必需氨基酸亮氨酸以其单体形式提供或包含在白蛋白中。

然后,他们选择了一种营养缺乏的肿瘤类型,细胞外蛋白是重要的氨基酸来源。实验显示,当白蛋白添加到生理水平(3-4%)时,肿瘤模型中的细胞可以通过溶酶体白蛋白分解代谢在缺乏亮氨酸的培养基中维持增殖。
接下来,他们使用 CRISPR-Cas9 筛选技术以确定与营养转换有关的几种途径。
研究团队发现,当细胞以白蛋白为食时,一个重要的选择性关键基因是跨膜蛋白 TMEM251,该团队将其命名为 LYSET(溶酶体酶转运因子)。
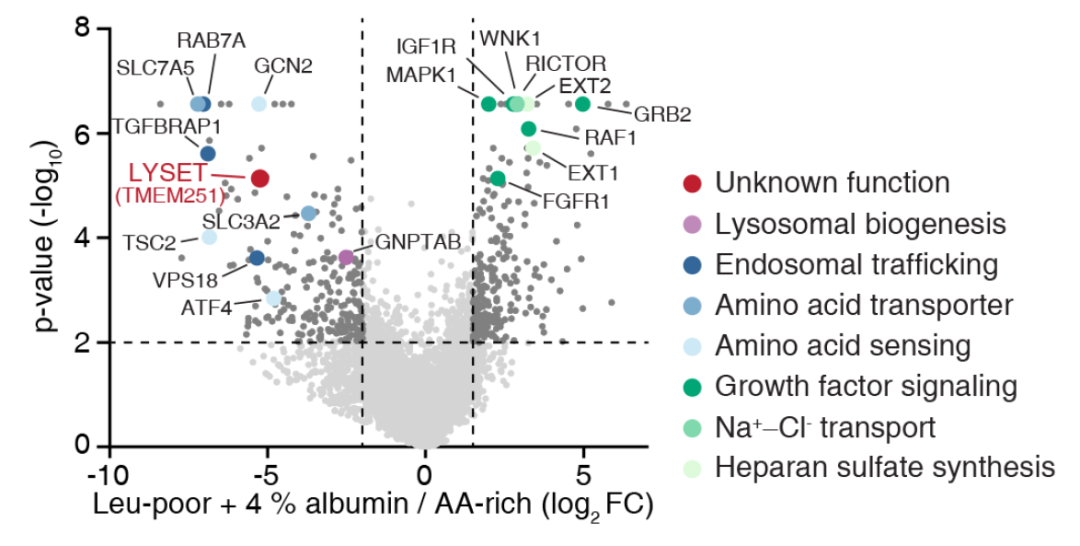
LYSET 是一种含有131个氨基酸残基的小型跨膜蛋白,与其他蛋白缺乏明显的同源性。
在营养丰富的条件下,LYSET 对于细胞活力和生长是非必需基因;但在添加3%白蛋白的缺乏亮氨酸的培养基中,LYSET 的缺失强烈抑制了所有癌细胞系、小鼠胚胎成纤维细胞和肾细胞的增殖和活力。这表明,在细胞外蛋白是必需营养素时、在体外氨基酸耗尽条件下,以及在体内肿瘤生长期间,LYSET 是必需基因。
对 LYSET 功能的进一步实验表明,该基因是甘露糖-6-磷酸(M6P)途径的核心成分,该途径是溶酶体酶转运所必需的,因此也是溶酶体营养素生成所必需的。溶酶体是一种小细胞器,作为细胞的胃,蛋白质在溶酶体中被消化;但在 LYSET 缺失的情况下,癌细胞的溶酶体中缺乏酶,因此不再能消化蛋白质。
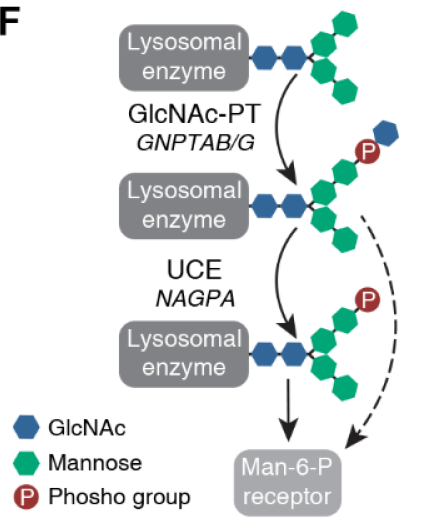
最后,研究人员使用小鼠模型研究了 LYSET 在真实肿瘤中的功能。他们发现,LYSET 缺失在几种类型的癌症中强烈抑制了肿瘤的发展;但在正常的营养条件下,LYSET 的耐受性良好。

Johannes Zuber(左),Wilhelm Palm(右)
Wilhelm Palm 表示,通过鉴定出 LYSET,发现了一个能适应不同营养代谢途径的核心成分。该途径对溶酶体生理学、细胞外蛋白质的营养利用和癌症的代谢适应至关重要。这是癌细胞在恶劣的肿瘤环境中生存和生长的关键能力。”
Johannes Zuber 表示,这项研究结果揭示了 LYSET 和 M6P 途径对依赖溶酶体分解代谢产生营养素的细胞基本功能,并证明该途径对癌细胞特别重要。因此,这一途径有望成为攻击癌症主要代谢瓶颈的分子切入点。”
原始出处:
Lysosomal enzyme trafficking factor LYSET enables nutritional usage of extracellular proteins. Science, 2022.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言