Nat Commun:AP-1和TGFβ协同介导非经典Hedgehog信号转导通路诱导基底细胞癌的耐药性
2020-10-19 xiaozeng MedSci原创
尽管目前靶向癌基因的癌症疗法已取得长足的进步,但由于肿瘤的异质性等特点限制了单一疗法的疗效。皮肤基底细胞癌(BCC)是美国最常见的癌症之一,由于其反复暴露于紫外线以及高突变负担,以及临床样品方便获取,
尽管目前靶向癌基因的癌症疗法已取得长足的进步,但由于肿瘤的异质性等特点限制了单一疗法的疗效。皮肤基底细胞癌(BCC)是美国最常见的癌症之一,由于其反复暴露于紫外线以及高突变负担,以及临床样品方便获取,BCC成为肿瘤进化和异质性研究的极佳模型。
既往研究显示,BCC的发生是由Hedgehog(Hh)信号通路的过度激活所引起的,因此该其成为靶向疗法的有希望的候选者。然而,使用SMO抑制剂疗法的初始应答率仅有令人失望的40%,且第一年的复发率为20%。
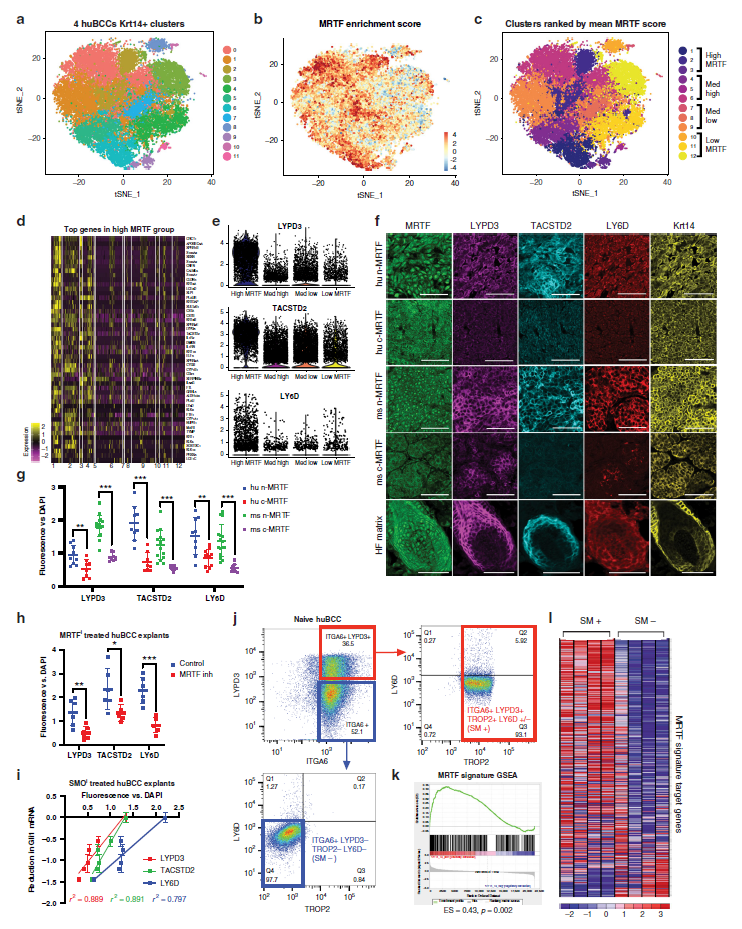
LYPD3/TACSTD2/LY6D标记BCCs患者的nMRTF亚群
研究人员先前发现了一个心肌核蛋白相关转录因子(nMRTF)耐药通路,其可以放大非典型的Gli1活性,但nMRTF细胞状态的特征和驱动因素仍然未知。
AP-1和Smad3诱导RhoGEFs的转录
在该研究中,研究人员通过对患者肿瘤组织的单细胞RNA测序,鉴定了与nMRTF和SMO抑制剂耐药性相关的三个预后表面标志物(LYPD3、TACSTD2和LY6D)。研究发现,nMRTF的细胞状态类似于毛囊基质的传递-放大细胞,在这些细胞中AP-1和TGFβ能够协同驱动nMRTF的激活。JNK/AP-1信号能够通过染色质开放性和Smad3对DNA结合,诱导RhoGEFs的转录,最终促进nMRTF的激活。
重要的是,小分子AP-1抑制剂能够选择性的靶向人基底细胞癌的LYPD3+/TACSTD2+/LY6D+nMRTF通路,为改善该疾病的组合疗法开辟了道路。
原始出处:
Yao, C.D., Haensel, D., Gaddam, S. et al. AP-1 and TGFβ cooperativity drives non-canonical Hedgehog signaling in resistant basal cell carcinoma. Nat Commun 11, 5079 (08 October 2020).
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#TGFβ#
22
#Nat#
33
#细胞癌#
31
#TGF#
0
#Hedgehog#
31
#COMMUN#
32
#基底细胞#
23
这个很有意义,让我眼界大开
78
靶向癌基因疗法突破在即。
98
来学习
93