因为安全性问题,今年的PARP抑制剂可以“一蹶不振”到什么程度?
11月11日,GSK第二次宣布撤回PARP抑制剂Zejula的部分适应症,以后二线治疗中将仅用于有害以及疑似有害的生殖系BRCA突变的卵巢癌患者人群。
这个决定基于一项ENGOT-OV16/NOVA III期试验最终总生存期(OS)分析的审查结果。在最终结果中,非BRCA突变患者(non-gBRCA)队列的OS次要终点的风险比(HR)为1.06(95% CI: 0.81-1.37)。与安慰剂相比,Zejula在两轮化疗后并不能帮助非BRCA突变患者获得更长的生存期。于是,GSK撤回了Zejula在二线化疗后病情稳定的卵巢癌患者的治疗。
除此之外,Zejula在美国一线适应症保持不变,用于对铂类药物化疗有完全或部分反应的晚期上皮性卵巢癌、输卵管癌或原发性腹膜癌的成人患者的维持治疗。
据悉,GSK在2018年以51亿美元收购Tesaro时获得Zejula。BIOPHARMA pE数据表明,Zejula在2021年的销售额约为5.43亿美元,但今年第三季度的销售额约下降至4.18亿美元。
就连此前最畅销的PARP抑制剂Lynparza的销售额,最近也呈下降趋势。阿斯利康迫于Lynparza有可能增加患者死亡的潜在风险,经与FDA协商,也撤销了Lynparza用于治疗已接受过三种或多种先前化疗方案的有害或疑似有害gBRCAm晚期卵巢癌的成年患者的适应症后,今年Lynparza第三季度的业绩低于市场普遍预期。
更有甚者,6月,FDA对Clovis Oncology和ARIEL4试验的总体生存数据进行审查后,同样因为死亡风险的增加,Rubraca惨遭适应症撤回,EMA也在4月启动对该适应症的审查,随后CHMP建议限制Rubraca的使用。在撤回适应症后今年第三季度,Rubraca剩余的前列腺癌与复发性卵巢上皮、输卵管或原发性腹膜癌的维持治疗两大适应症支撑的销售额仅为3070万美元,低于第二季度的3210万美元。
支柱产品的负面消息不但直接影响了Rubraca的创收能力,也影响了Clovis现金流周转,Clovis甚至放出了即将破产的消息。
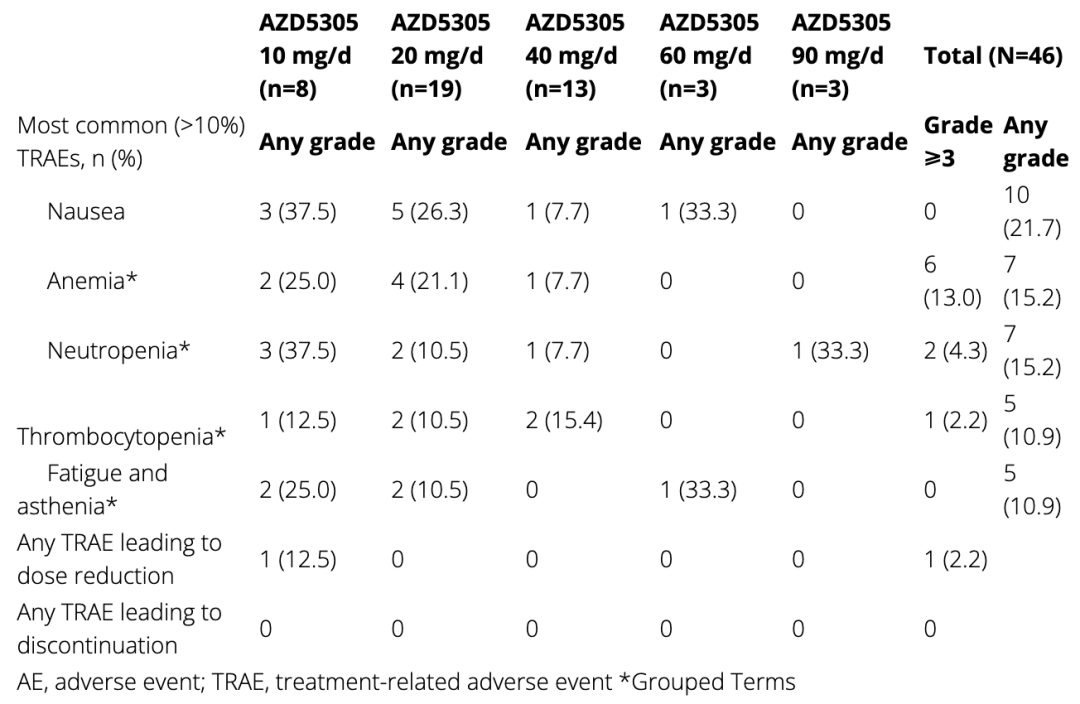
安全性成为了PARP抑制剂绕不开的问题。PARP抑制剂与化疗的联用中,限制在于毒副作用叠加,尤其是血液毒性,比如淋巴细胞减少等。以分子机制来看,血液毒性来自对PARP2的抑制,但目前已上市的PARP抑制剂对PARP1和PARP2没有选择性,是增加死亡率风险的根本原因。
从临床角度说,2022年的NCCN指南已经更新了五次,细究其因,其中关于卵巢癌的临床指导有很多变化,或有可能就是因为其强大的毒副作用与制药公司PARP抑制剂适应症的接连撤市所导致。

尽管每家公司都强调,撤回一项适应症并不会影响药物的其他适应症,但FDA对于PARP抑制剂审查的加强,以及现阶段没有解决的安全性问题,可能会导致一些医生在临床中减少PARP抑制剂的使用。
这势必直接影响着PARP抑制剂市场的增长。SVB Securities分析师Andrew Berens在11月10日的一份报告中写道:“PARP类对卵巢癌后线治疗的BRCA患者以外的总生存率的影响,是监管部门重点关心对象,会对该药物的销售额产生消极作用。虽然PARP抑制剂药物已经在研究转向卵巢癌患者的早期治疗线,但对其安全性问题的担忧,可能会影响药物的广泛使用。”
参考文献:
1.Under FDA pressure, GSK limits use of ovarian cancer drug;BIOPHARMA pE
2.三种 PARP 抑制剂如此使用增加卵巢癌患者死亡风险!该适应症均已撤回!;丁香园肿瘤时间
3.PARP抑制剂不香了?概念股Clovis裁员,行将破产;同写意
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言