Nature:肿瘤微环境也能诊断癌症了
2017-04-19 佚名 癌症123
肿瘤早期诊断无疑对于治疗和预后都有很大的影响,越早作出诊断,就能越早开始治疗,疗效往往更好。早期诊断的手段主要有两种,一种是检测血液中是否有肿瘤特征的生物标记物,另一种是使用分子成像技术希望能够找到肿瘤的确切位置和大小。不过,目前这两种技术均面临一些困难,还没有真正达到早期准确诊断肿瘤的目的。对于这两种技术来说,现有的手段对肿瘤的敏感度都还欠缺。这两种技术的“信噪比”,在这里称为肿瘤 / 正常组织

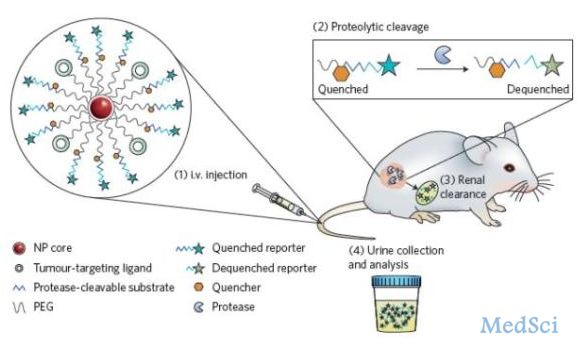
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#Nat#
37
#诊断癌症#
36
牛
59