Science子刊:中山大学王铭辉/黄炳培发现Src重新激活焦亡以逆转肺癌和胰腺癌模型中的化学耐药性
2023-01-14 iNature iNature 发表于威斯康星
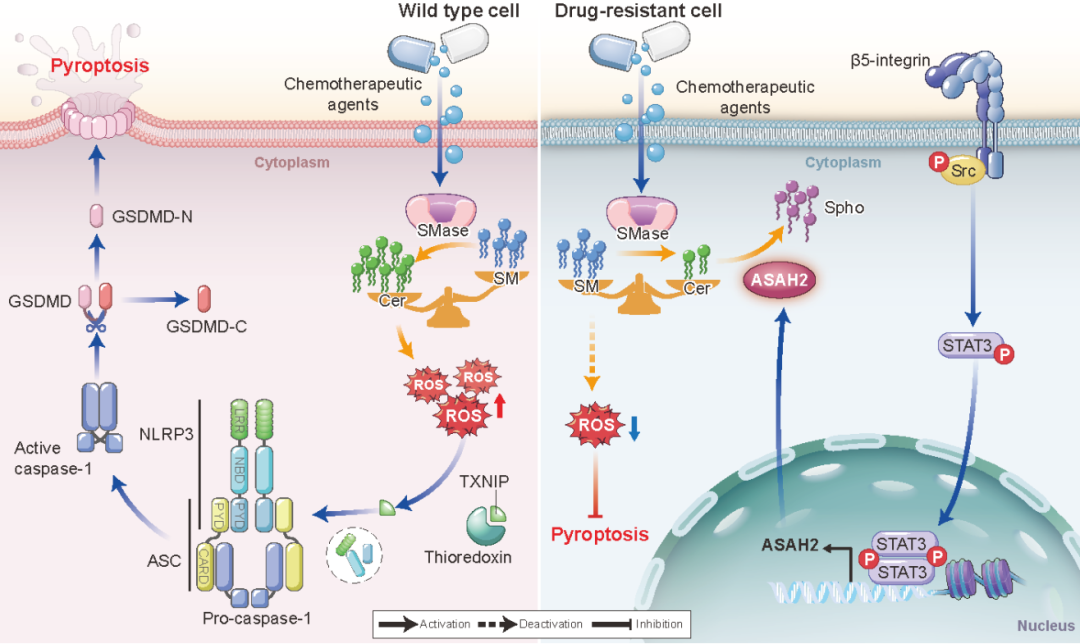
该研究发现整合素β5-Src-STAT3-ASAH2驱动的鞘脂代谢轴通过灭活典型焦亡而赋予癌症耐药性。
焦亡是一种由焦孔素驱动的溶解性程序性细胞死亡,由炎症性半胱天冬酶触发,由典型或非典型途径启动,最近被视为癌症治疗的潜在治疗靶点。然而,通过调节焦亡来克服癌症的化疗耐药还没有被探索。
2023年1月11日,中山大学王铭辉及黄炳培共同通讯在Science Translational Medicine(IF=19)在线发表题为“Targeting Src reactivates pyroptosis to reverse chemoresistance in lung and pancreatic cancer models”的研究论文,该研究表明靶向Src可以重新激活焦亡以逆转肺癌和胰腺癌模型中的化学耐药性。该研究证明了整合素β5通过ASAH2驱动的鞘脂代谢重编程抑制化疗诱导的典型焦亡,从而赋予癌症化疗耐药。临床上,整合素β5高表达与癌症患者不良预后和化疗反应有关。此外,体外化疗耐药细胞不能发生化疗诱导的焦亡,这是由整合素β5控制的。
蛋白质组学和脂质组学分析表明,整合素β5通过Src信号转导器和转录激活因子3 (STAT3)信号上调鞘脂代谢酶神经酰胺酶(ASAH2)的表达,进而降低代谢物神经酰胺浓度和随后的ROS生成,从而阻止化疗诱导的典型焦亡。利用癌细胞系、患者来源的肿瘤类器官和原位肺和胰腺动物模型,作者表明,Src或神经酰胺酶抑制剂通过在体外和体内重新激活焦亡来挽救耐药胰腺癌和肺癌细胞对化疗的反应。总的来说,研究结果表明细胞焦亡疗法是改善癌症治疗的一种手段,值得进一步研究。

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言