The Lancet Gastroenterology & Hepatology发表Early detection of pancreatic cancer,文章指出,临床诊断出PDAC通常已到晚期,这限制了治疗选择,并导患者5年生存率仅有3–15%。尽管胰腺导管腺癌相对不常见,目前的方法不建议筛查无症状的成年人口。但是,建议对高危人群进行筛查。
PDAC的病情发展与特定基因的种系和种系突变有关,因此有较高的遗传风险。因此家族史是PDAC高危人群指征之一。而且相关研究发现,分子和临床标志物组合检测比单独使用当前的临床特征对需要手术或常规监测或不需要监测的患者进行分类更为准确。胰腺导管腺癌与糖尿病之间有多方面关系。与一般人群相比,长期存在的2型糖尿病(超过5年)的人患胰腺导管腺癌的风险增加了1-1.5-倍。国际指南和有关胰腺导管腺癌早期发现的白皮书建议对有发展为胰腺导管腺癌的终生风险高于5%的个体进行有针对性的筛查。还确定了其他高危人群,例如患有新发糖尿病的个体,可改变的危险因素(例如吸烟,肥胖),不可改变的危险因素(例如年龄),特定的合并症(例如肥胖,慢性胰腺炎)或早期症状(其中一些症状在诊断前已存在1年以上)。
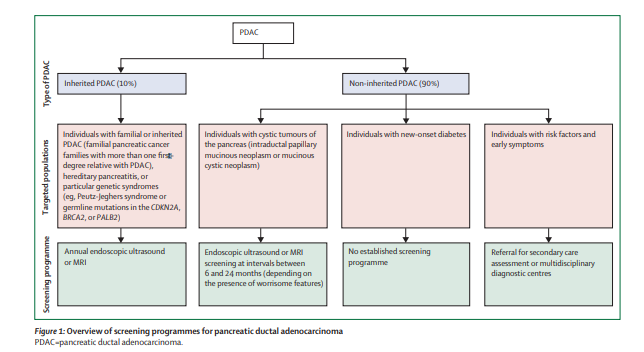
生物标记物可以在胰腺导管腺癌的早期检测中发挥重要作用,它可以筛选高危人群中的个体,这些个体具有最高的癌症诊断机会,从而帮助临床医生优先筛选个体。
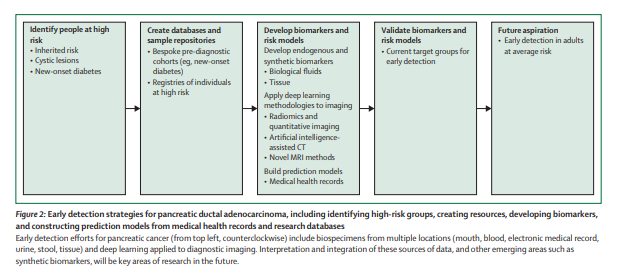
通过对PDAC确诊患者的样本进行生物标志物研究,可能会发现指示有症状疾病的生物标志物。相关实验是在生物标志物开发中使用小鼠模型,通过该过程生成的标记代表了在遗传,转录组,代谢组学和蛋白质组学水平上与胰腺导管腺癌发展的最早组织学阶段相关的异常变化。
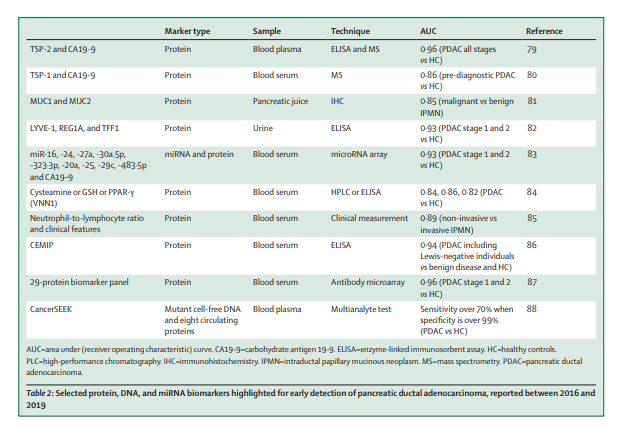
毫无疑问,早期诊断将在改善疾病治疗方面发挥重要作用,正如我们所指出的那样,相关研究已经取得了进展。新的参加实验的的患者人群(患有新发糖尿病或有症状的个体)的建立为生物学和流行病学标志物的发现和验证提供了独特的诊断前资源。无论是通过社交媒体还是通过电子健康记录,对现有数据的谨慎和合乎道德的使用都具有促进预测模型的功能,而应用于成像的人工智能提供了发现较早病变的可能性。早期检测的进展将与治疗方法的改进相结合,以延长PDAC患者的生存期。
原始出处:
Pereira SP, Oldfield L, Ney A, Hart PA, Keane MG, Pandol SJ, Li D, Greenhalf W, Jeon CY, Koay EJ, Almario CV, Halloran C, Lennon AM, Costello E. Early detection of pancreatic cancer. Lancet Gastroenterol Hepatol. 2020 Mar 2. pii: S2468-1253(19)30416-9
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#Lancet#
24