Cell Death Dis:BRD9激活TUFT1/AKT通路促进肝细胞癌的生长和转移
2020-09-10 QQY MedSci原创
肝细胞癌(HCC)作为第六大最常见的恶性肿瘤,是癌症相关死亡的第三大诱因,每年约有780,000例新确诊病例和750,000例死亡病例。肝癌的发病机制是一个复杂的过程,包括持续的炎性损伤和纤维化沉积。
肝细胞癌(HCC)作为第六大最常见的恶性肿瘤,是癌症相关死亡的第三大诱因,每年约有780,000例新确诊病例和750,000例死亡病例。肝癌的发病机制是一个复杂的过程,包括持续的炎性损伤和纤维化沉积。尽管近年来影像学诊断、手术、化疗和靶向治疗等手段已取得显著进展,但由于肿瘤的快速生长、复发以及高转移率,HCC的5年生存率仍低于20%。因此,更好地了解肝癌发生发展的分子机制有利于新型靶向药物的开发以及该疾病总体预后的改善。
既往研究显示,在人鳞状细胞肺癌、急性髓性白血病和恶性横纹肌瘤中BRD9(Bromodomain-containing protein 9)均起着至关重要的作用。然而在HCC中BRD9的表达水平和生物学功能仍有待研究。
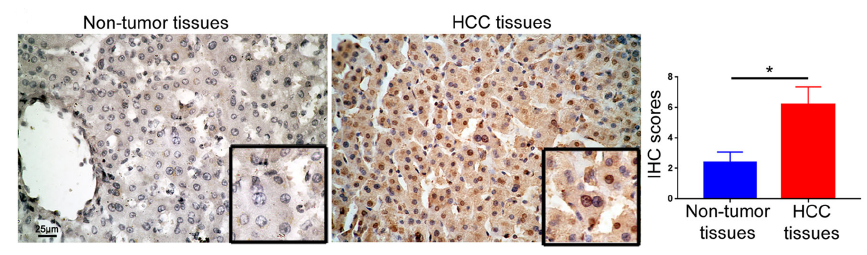
该研究前期通过公共数据库分析,发现在肝癌中BRD9的表达水平上调。研究人员进一步验证了,相比于邻近非癌组织,BRD9在肝癌组织中的表达升高。与LO2细胞相比,在HCC细胞中也同样观察到BRD9表达水平的上调。而升高的BRD9与患者不良的临床病理特征相关。高表达水平的BRD9对应着较低的HCC患者整体生存率和无病生存率。
功能研究显示,过表达BRD9能够促进Hep3B细胞的增殖、迁移、侵袭和上皮-间质转化(EMT)作用。相反的,敲除BRD9或药理学抑制其表达均会导致HCCLM3细胞增殖和侵袭能力的降低。此外,敲低BRD9会抑制HCCLM3细胞的生长和转移。
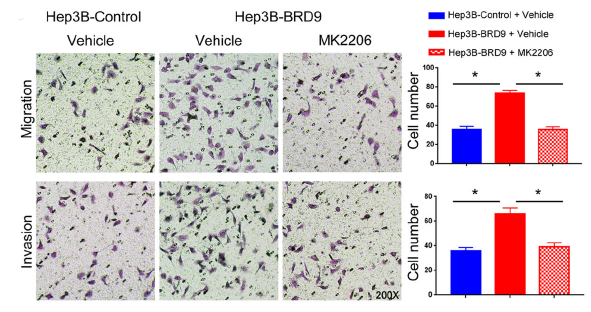
机制研究显示,BRD9能够调控HCC细胞中TUFT1的表达和AKT的激活。 ChIP-qPCR结果显示,BRD9通过促进P300乙酰转移酶与TUFT1启动子区域结合,提高启动子区域的H3K27Ac修饰水平,从而在表观遗传学层面调控TUFT1的表达。值得注意的是,敲低TUFT1或给予AKT抑制剂(MK2206)均阻断了BRD9对Hep3B细胞增殖、迁移、侵袭和EMT的促进作用。而强制表达TUFT1则能够消除上述敲低BRD9对HCCLM3细胞生长和转移的影响。
总而言之,该研究显示BRD9能够通过激活TUFT1/AKT通路来促进肝癌细胞的生长和转移,其可能是HCC的一个潜在的生物标志物和治疗靶标。
原始出处:
Dou, C., Sun, L., Wang, L. et al. Bromodomain-containing protein 9 promotes the growth and metastasis of human hepatocellular carcinoma by activating the TUFT1/AKT pathway. Cell Death Dis 11, 730 (09 September 2020).
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#肝细胞#
0
#细胞癌#
27
#Cell#
18
#CEL#
25
#Dis#
22
#Akt#
31
#Death#
25