告别注射,MIT团队开发口服机器人胶囊,实现蛋白质药物高效缓释递送
2022-10-04 生物世界 生物世界
生物大分子药物通常需要更繁琐且昂贵的方法给药,例如皮下注射、静脉注射,甚至是住院治疗。正如在胰岛素递送的案例中显示的那样,RoboCap 让口服生物大分子药物的吸收达到治疗水平成为可能。
口服给药是最常见、最经济,且最实用的给药方式,然而,包括核酸(DNA、RNA)和蛋白质在内的生物大分子药物虽然可以有效治疗多种疾病,但它们却受到了胃肠道降解和吸收不良的限制,因此,难以口服给药。
早在1922年,班廷就开始通过胰岛素来治疗糖尿病,这一方法拯救了无数糖尿病患者,班廷也因此获得了诺贝尔奖。但胰岛素作为一种蛋白质大分子,其口服的生物利用度不足1%,因此必须通过注射的方式给药,这对于数以百万计的2型糖尿病患者来说,每天打针是一件很麻烦且痛苦的事情。
近日,麻省理工学院的 Giovanni Traverso、Robert Langer 等人在 Science 子刊 Science Robotics 上发表了题为:RoboCap: Robotic mucus-clearing capsule for enhanced drug delivery in the gastrointestinal tract 的研究论文【1】。
研究团队开发了一种机器人药物胶囊——RoboCap,口服该机器人药物胶囊后,胶囊的凝胶涂层首先在胃中溶解,然后,小肠的环境会激活 RoboCap,其携带的机器帽会振动和旋转并穿过黏液屏障,将胶囊中携带的药物沉积在小肠,促进肠内壁细胞对药物的吸收。
研究团队还在临床前模型中测试了 RoboCap 递送胰岛素和万古霉素的效果(万古霉素是一种治疗严重耐药菌感染的抗生素,通常需要静脉注射给药)。在猪模型实验中,RoboCap 将胰岛素和万古霉素的药物渗透性提高了10倍以上,生物利用度提高了20-40倍。因此,RoboCap 可以克服胃肠道环境的许多挑战,有望实现多种生物大分子药物的口服给药。
麻省理工学院(MIT)的 Robert Langer、Giovanni Traverso 团队一直致力于开发生物大分子药物的口服给药方法。

Robert Langer(左)、Giovanni Traverso(右)
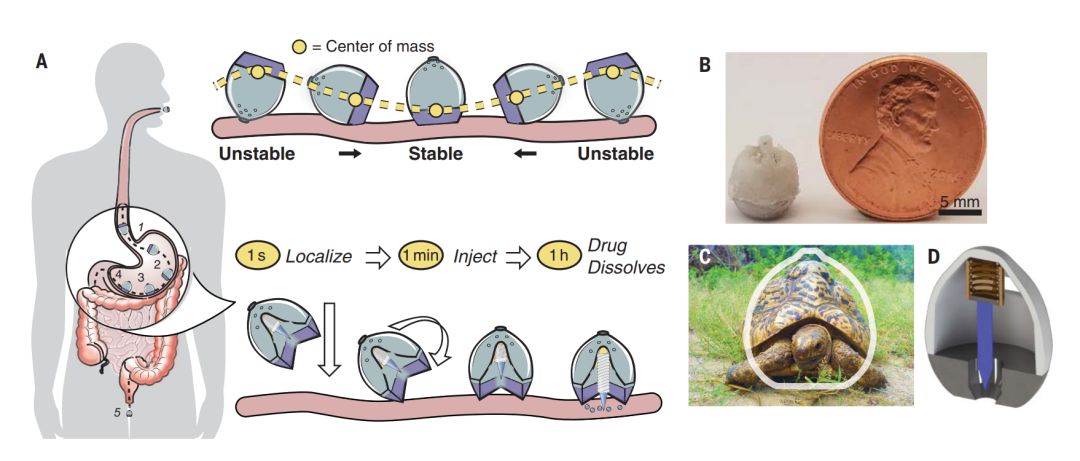
早在2019年2月,他们就在 Science 发表论文【2】,开发了一种小型机器胶囊,这种胶囊能够通过口服到达胃部后向胃壁注射胰岛素,从而降低血糖。这种胶囊以豹龟的外形为灵感,能够自我纠正方向,保证将药物准确注射到胃壁。
在胶囊内,针头连接到压缩弹簧上,压缩弹簧由糖制成的圆盘固定就位。当吞咽胶囊时,胃中的水溶解糖圆盘,释放弹簧并将针注射到胃壁中。由于胃壁没有疼痛感受器,因此患者无法感受到注射带来的疼痛。
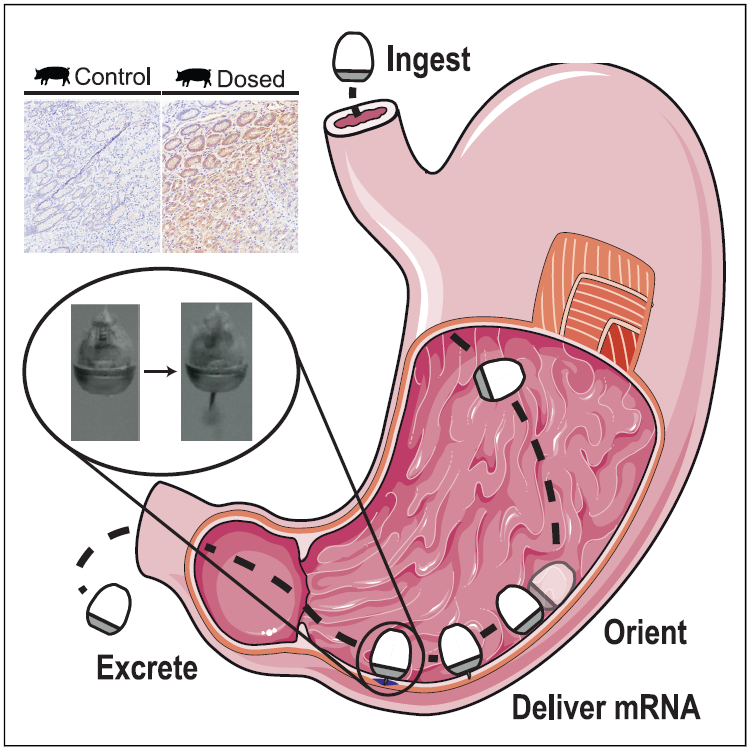
2022年1月,Robert Langer、Giovanni Traverso 团队在 Matter 期刊发表论文【3】。将这种胶囊用来递送 mRNA 疫苗,实现了核酸大分子的口服给药。
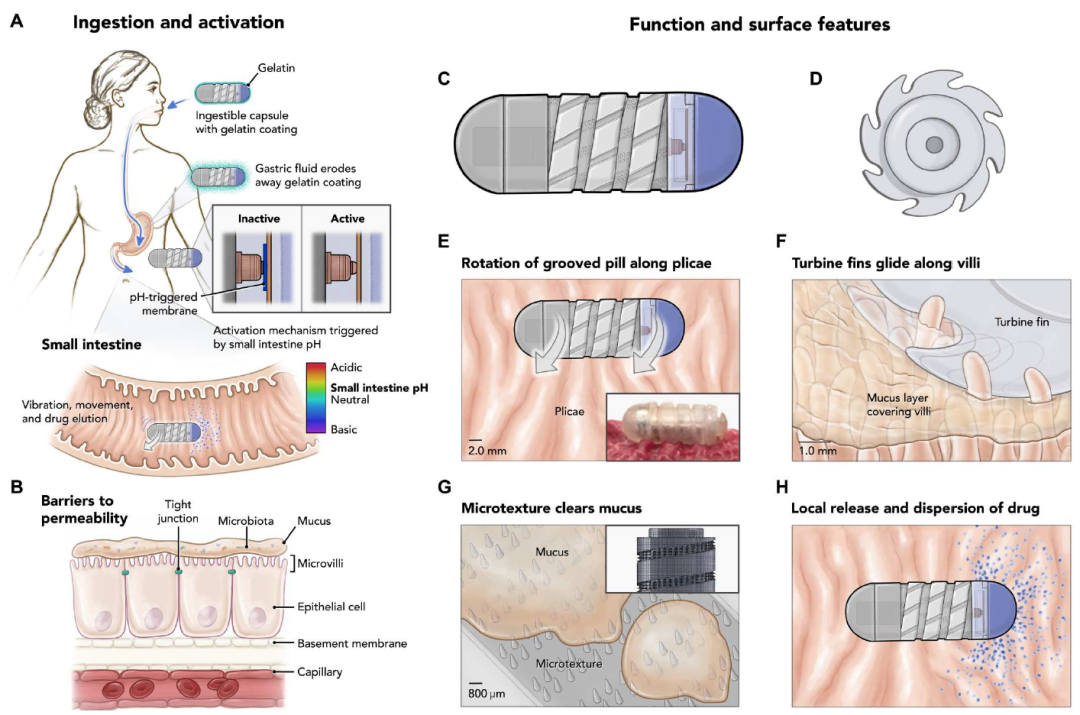
在这篇 Science Robotics 论文 ,Robert Langer、Giovanni Traverso 团队想到了创造一种保护性胶囊的方法,这种胶囊的外层在消化道中溶解,然后可以在胃肠道粘液中旋转前进,将携带的药物直接沉积在上皮细胞。


研究团队最终开发出了这款名为 RoboCap 的机器人药物胶囊,约为复合维生素片的大小,胶囊表面涂有明胶,可调节其在特定pH值下溶解,还能防止口服时的磨损或不适感。该胶囊一端的小储药库中携带药物,当表面涂层溶解时,pH值的变化会触发胶囊内的一个微型马达开始旋转。这种旋转运动既有助于前进,还能刷掉粘液。
研究团队在临床前模型中测试了 RoboCap 递送胰岛素和万古霉素的效果。全世界数以百万计的2型糖尿病患者需要每天使用胰岛素治疗,其口服的生物利用度不足1%,因此必须通过注射给药。万古霉素是一种糖肽类抗生素,用于治疗严重耐药的革兰氏阳性细菌感染,其口服的生物利用度仅为0.069%-4%,必须通过静脉注射给药,还需要昂贵的住院费用。
实验结果显示,与标准口服给药相比,RoboCap 递送的万古霉素和胰岛素在体外和体内猪模型中的生物利用度提高了20-40倍。值得一提的是,与皮下注射或静脉注射相比,RoboCap 递送的胰岛素缓释效果更好,这对于一些需要逐步或持续释放的药物来说,是个很好的优势。
药物从 RoboCap 中释放出来后,RoboCap 本身可以自行通过消化道排出体外。体内研究显示,RoboCap 在通过消化道的过程中没有出现炎症或刺激的迹象,而且,RoboCap 影响的粘液层会在几个小时后恢复。
研究团队表示,RoboCap 与其他药物递送载体(例如脂质体、纳米颗粒)不同,RoboCap 不存在生物相容性的问题,因为整个胶囊保持封闭状态,并能够在药物递送后排出人体。他们在论文中总结道:生物大分子药物通常需要更繁琐且昂贵的方法给药,例如皮下注射、静脉注射,甚至是住院治疗。正如在胰岛素递送的案例中显示的那样,RoboCap 让口服生物大分子药物的吸收达到治疗水平成为可能。
论文的通讯作者 Giovanni Traverso 表示,肽类和蛋白质是重要的药物类型,但胃肠道的降解环境和不良吸收限制了这类药物的口服潜力。而 RoboCap 能够通过振动、旋转等方式清除和穿过胃肠道黏液屏障,帮助药物到达所需的位置,并最大限度地在局部区域分散药物,增强大分子或小分子药物的吸收。
该研究中使用的 RoboCap 是在小肠中释放药物,但需要指出的是,RoboCap 可以通过改变明胶涂层溶解的pH值来靶向胃或结肠等部位。研究团队还计划探索使用 RoboCap 递送其他蛋白质药物的可能性,例如用于治疗2型糖尿病的 GLP1 受体激动剂。此外,这种胶囊还可以用来实现治疗溃疡性结肠炎和其他炎症的局部给药,通过最大化组织中药物的局部浓度来帮助治疗炎症。
论文链接:
https://www.science.org/doi/10.1126/scirobotics.abp9066
http://science.sciencemag.org/content/363/6427/611
https://doi.org/10.1016/j.matt.2021.12.022
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








