ESH-ISH 2021|COVID-19相关研究热点速递与点评
2021-04-25 “心关注”公众号 “心关注”公众号
北京时间2021年4月12日21:00~22:00,欧洲高血压学会(European Society of Hypertension, ESH)与国际高血压学会(International Socie
北京时间2021年4月12日21:00~22:00,欧洲高血压学会(European Society of Hypertension, ESH)与国际高血压学会(International Society of Hypertension, ISH)联席学术会议举行了一场COVID-19相关研究的线上学术汇报,共对来自欧洲和南美的九项研究进行了云端分享和讨论。上述九项研究主要集中在COVID-19疫情封闭期间心血管疾病负担和危险因素的变化、COVID-19与肾素-血管紧张素系统(renin angiotensin system, RAS)、以及影响COVID-19患者院内转归的治疗方法和潜在治疗新靶点等三个领域。本文旨在对上述九项研究结果进行简要介绍,并与该领域的其他研究进行对比,以期对临床工作和相关科研工作的开展有所启发和借鉴。
一、COVID-19疫情封闭期间心血管疾病负担和危险因素的变化
意大利中部2020年初期COVID-19疫情期间属于低流行区域。Del Pinto等报道了2020年1月至3月期间意大利中部拉奎拉省五所医院全因住院、心血管疾病住院以及心血管疾病急性期治疗措施(冠状动脉成形术、溶栓、血管腔内治疗)和院内心血管死亡情况。结果显示,与2019年同期相比,全因住院和心血管住院人次下降~15%,心血管手术量下降~26%,与2019年3月相比,2020年3月发生的院内心血管死亡更多(6.1% vs.11.9%, P=0.048)。
总体而言,此研究的结果并不意外,与其他大多数报道一致,即COVID-19疫情封闭期间呈现住院人次减少的趋势,但由于就医习惯的改变,寻求住院治疗的心血管疾病患者病情往往较封闭前更为严重,导致院内心血管死亡增高。然而,另一项研究对COVID-19封闭期间心血管疾病住院减少的原因提出了新的见解。Girerd等对法国巴黎市区在COVID-19疫情封闭期间,2273名受试者采用基于移动互联网的可穿戴设备记录约30万次家庭血压和心率测量进行了分析。结果显示(图1),在实施封闭的前四周内,与2019年同期相比,整体血压水平开始逐渐降低,在封闭第4~7周时,收缩压下降3 mmHg(-2.4 ~ -3.9),舒张压下降1.5 mmHg (-1.4 ~ -2.2)。在经过年龄和性别调整后,仍然得出了类似的结果。此外,在封锁期间基线血压水平较高者的血压下降幅度更为明显。在此之前针对COVID-19期间心血管疾病负担的研究多认为患者在心血管症状出现之后对住院治疗相关的COVID-19感染风险的顾虑、以及封闭期间的交通受阻是引起住院减少的原因,但后续又有学者提出空气污染减轻和居家隔离后药物治疗依从性提高也可能是心血管疾病发病减少的可能解释。鉴于高血压是心血管疾病最为重要危险因素之一,这项基于COVID-19期间血压遥测技术的研究无疑对心血管疾病发病降低的潜在原因提出了新的解释。的确,COVID-19引起的全人类生活方式的改变,在一定程度上可能会对与传统危险因素相关疾病的发生和发展产生潜在的影响。而且这种基于COVID-19疫情封锁产生的自然实验(natural experiment)是研究心血管疾病的难能可贵的机会。比如,在2008年北京奥运会期间,由于城市限行引起空气质量的改善,可以显着降低很多与心血管疾病相关炎症因子的水平。
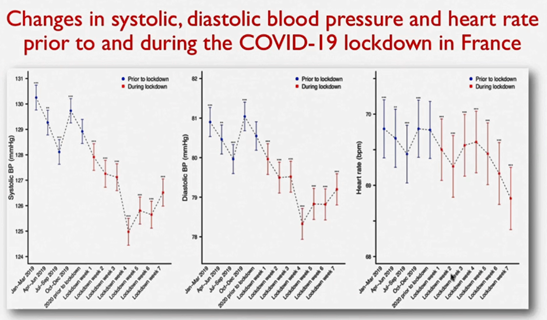
图1. 巴黎市区在COVID-19疫情封闭期间,2273名受试者采用基于移动互联网的可穿戴设备记录的血压和心率变化趋势
来自巴黎心血管中心的Bruno报道了法国和德国COVID-19疫情封闭前和封闭期间采用一种家用新型体成分智能电子秤测定的脉搏波传导速度(pulse wave velocity, PWV)的变化规律。作者选择的这两个国家具有代表性,其中法国实施了严格的封闭而德国仅实施部分封闭。在封闭期间,采用上述方法测定的总体人群的PWV、体重、血压和体力活动均显着降低,而法国的PWV降低明显大于德国,相当于血管硬化年龄降低了5.2个月(图2)。在法国人群中,PWV轨迹分为三组:下降型(21.1%)、稳定型(60.6%)和上升型(18.2%)。与稳定型PWV相比,PWV下降型轨迹和上升型轨迹的基线血管硬化年龄均高于稳定型(图3)。只有下降型PWV轨迹伴有显着的体重降低;此外,独居与上升型轨迹有关。
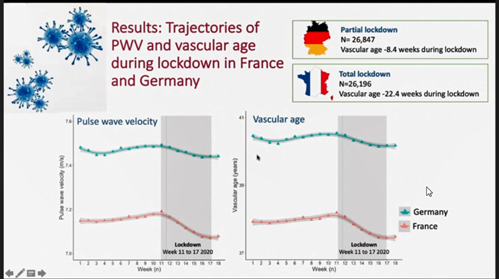
图2. 法国和德国在COVID-19疫情封闭前后,采用基于移动互联网技术测定的居家动脉波传导速度和血管硬化年龄的变化趋势
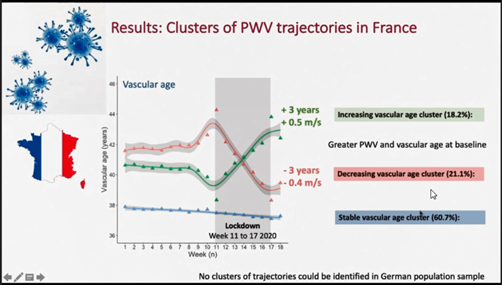
图3. 法国在COVID-19疫情封闭前后,采用基于移动互联网技术测定的居家动脉波传导速度群体轨迹
上述两项研究一致性的显示,COVID-19疫情封闭在整个人群中可引起心血管危险因素的变化,表现为血压降低,血管增龄性硬化的改善、体重降低等等。这些基于大样本人群的证据,再次提示COVID-19封闭期间心血管住院人次的降低很有可能源于心血管危险因素的改善。
二、COVID-19与肾素-血管紧张素系统
基于血管紧张素转化酶2(angiotensin converting enzyme 2, ACE2)是冠状病毒(包括SARS-CoV-2)的功能性受体的证据和RAS与COVID-19疾病进展之间的潜在联系,自COVID-19在全球大流行之初,众多学者都在积极探讨血管紧张素转化酶抑制剂(angiotensin-converting enzyme inhibitors,ACEI)和血管紧张素受体拮抗剂(angiotensin receptor blockers, ARB)对COVID-19患者不良预后的潜在影响。
当然,RAS相关研究也是此次ESH-ISH联合科学会议COVID-19专场的热点。以RAS为主题,共有四项研究发布,其中两项研究涉及RAS抑制剂对COVID-19患者预后的影响。Rodilla等分析了西班牙SEMI-COVID-19协作网中150家医院收治的12226名COVID-19患者(其中2630例患者死亡),发现高血压病史是全因死亡的独立预测因素,且在高血压患者中,ARB显示出比其他抗高血压药物更低的死亡风险。另一项研究中,Patoulias等对COVID-19大流行开始至2020年5月19日期间发表的观察性研究进行了荟萃分析,以评估ACEI/ARB的使用与COVID-19大流行期间成人患者主要临床终点(感染、住院、入住 ICU、死亡)风险之间的相关性[7]。该作者共纳入25项观察性研究,结果显示ACEI/ARB与SARS-CoV-2感染、入院、急危重症、ICU住院和SARS-CoV-2相关死亡的风险增加不相关;但存在显着的地区差异:在亚洲国家,使用ACEI/ARBs可降低急危重症(OR = 0.37,95% CI 0.16-0.89)和死亡(OR= 0.62,95% CI 0.39-0.99)的风险;但在北美,使用ACEI/ARB与ICU入院风险增加有关(OR = 1.75,95% CI 1.37-2.23),在欧洲与死亡风险增加(OR= 1.68,95% CI 1.05-2.70)。然而,这两项研究均无法避免观察性研究的固有局限性:在很多情况下,涉及临床决策的观察性研究在患者特征上均存在尚未控制的混杂因素。事实上,对于RAS抑制与COVID-19的关系,在2020年ESC年会上公布的BRACE CORONA(Angiotensin Receptor Blockers andAngiotensin-converting Enzyme Inhibitors and Adverse Outcomes in Patients WithCOVID19)研究已经提供了更具说服力的证据。
BRACECORONA研究是一项来自巴西的多中心、IV期、随机对照临床试验(randomized controlled trial, RCT),旨在比较继续或暂停ACEI/ARB治疗对COVID-19患者临床结局的影响。该研究共入选659名接受ACEI/ARB治疗且确诊为轻中度COVID-19的患者。入选患者按1:1随机分为继续ACEI/ARB治疗组及暂停ACEI/ARB治疗组。其主要研究终点是30天时存活及出院情况,次要终点为COVID-19的进展,包括全因死亡,心血管死亡,心肌梗死,卒中,短暂性脑缺血发作,新发或恶化性心力衰竭等复合终点。BRACE CORONA研究显示暂停使用和继续使用组在平均存活时间、中位存活时间上均无统计学差异;在出院30天时的存活率也无统计学差异。BRACE CORONA研究是第一项评价ACEI/ARB使用与否对COVID-19患者临床结局影响的RCT。该研究建议对于有ACEI/ARB适应症的COVID-19患者一般应继续使用该药物。另一项旨在评估ACEI/ARB在CVOVID-19患者中应用安全性的RCT是REPLACE COVID(The Randomized Elimination or ProLongationof ACEIs and ARBs in COronaVIrus Disease 2019 trial)研究。该研究从2020年3月31日至8月20日从全球7个国家20家医院共招募152名在住院前接受ACEI/ARB治疗的COVID-19患者,按1:1随机分为继续ACEI/ARB治疗组和停止ACEI/ARB组。该研究的终点是基于死亡、机械通气时间、肾功能恶化、多器官功能异常以及使用升压药物等临床症状恶化的综合评分。结果显示两组患者在此综合评分体系评价中没有统计学差异,两组患者的血压、血钾、肌酐水平和死亡均无无明显差异。虽然REPLACE COVID研究的样本例数较少,但也弥补了一部分BRACE CORONA研究未解决的问题:(1) REPLACE COVID研究人群的年龄高于BRACE CORONA研究(62岁 vs. 55岁);(2) REPLACE COVID研究的整体人群更为高危(病死率为14%;BRACE CORONA研究为3%)。因此,综合BRACE CORONA和REPLACE COVID两项RCT研究的结果,目前已经有充足的证据显示ACEI/ARB对于轻中症和重症COVID-19的病理转归没有影响,如果没有明确的禁忌证,正在服用ACEI/ARB的CVOVID-19患者应当继续ACEI/ARB治疗。鉴于ACE2与COVID-19的复杂联系已经由一个学术争论上升为公众热点,当COVID-19患者表达出了对于继续使用ACEI/ARB的担忧时,基于上述两项RCT研究的结果,临床医生应说服患者继续使用该药物,尤其是伴有心力衰竭的患者,ACEI/ARB的使用可以显着改善这种患者的预后。从另一方面,BRACE CORONA和REPLACE COVID研究也提示,ACEI/ARB使用与否对不同病情COVID-19患者病程进展无明显影响,在特殊情况下也可以安全的改变治疗方案。
RAS与COVID-19的另一个科学问题是ACE2作为SARS-CoV2的受体,具有保护作用还是会进一步加重感染。ACE2与肺部炎症损伤的研究始于2005年澳大利亚学者在Nature发表的一篇论文:此文首次报道ACE2和血管紧张素AT2受体对于吸入和败血症相关急性呼吸窘迫综合征模型具有保护作用;而RAS的其他组分,如ACE、血管紧张素II以及AT1R则具有恶化急性肺损伤的作用。遗憾的是,直至十五年后COVID-19全球流行时,尚无一种旨在提升ACE2保护作用的药物问世。我国学者在COVID-19全球大流行之前,就已经完成人源性ACE2过表达小鼠模型的构建工作,并通过直接感染SARS-CoV2病毒引起小鼠肺部的显着炎症反应。虽然这一模型证实了ACE2在介导COVID-19肺部病理改变中的重要作用,但并不能说明ACE2在COVID-19病理进展中是有害的。此次ESH-ISH会议上,英国曼彻斯特大学的一个研究组通过对436例人肾脏RNA测序的分析,发现无论是高血压还是包括ACEI/ARB在内的多种降压药物,均不会引起肾脏ACE2水平表达的变化;然而,在人类肺组织和肾脏中ACE2的表达呈现显着的增龄性表达上调。后一发现的意义目前尚不明确,作者认为可能与老年人感染风险增加有关。
ESH-ISH会议另一个涉及ACE2的相关研究观察了Gitelman综合征和Bartter综合征患者感染SARS-CoV-2的风险。ACE2存在糖基化和非糖基化两种不同的免疫反应形式,只有糖基化ACE2与病毒结合有关。ACE2糖基化过程需要细胞内溶酶体/高尔基体中的酸性环境;能够进入细胞中的碱性药物,如羟氯喹/氯喹,可通过增加溶酶体/高尔基体中的pH值,抑制ACE2的糖基化的过程,从而有可能“关闭”SARS-CoV-2进入细胞的“大门”。此外,Rho激酶能够下调ACE2的水平。Gitelman综合征和Bartter综合征均为罕见的遗传性肾小管病,患者具有RAS活性升高,Ang II水平升高但血压正常或低血压、代谢性碱中毒、ACE2及其产物Ang 1-7的水平升高和Rho激酶活性降低等特点,因此能为ACE2水平增加和Rho激酶抑制剂对COVID-19的保护作用提供佐证。研究者对意大利北部的COVID-19高发地区(威尼托、伦巴第亚、艾米利亚罗马涅)100多名Gitelman综合征和Bartter综合征患者进行了电话调查,结果均未报告COVID-19 的感染/症状。由于Gitelman综合征和Bartter综合征的发病率较低,与意大利高发地区普通人群COVID-19的患病率相比无显着性差异,但与高发地区一般人群的估计患病率相比有统计学意义。这一研究提示增高的ACE2水平并不增加COVID-19的风险,因此也不支持暂停使用增加ACE2表达的ACE抑制剂/ARBs治疗以减少感染风险。
三、影响COVID-19院内转归的药物治疗和新的干预靶点
高血压与重症COVID-19风险增加和死亡率增加有关。由于高血压患者经常需要使用利尿剂,Pengo等调查了意大利伦巴第地区两个转诊中心住院的COVID-19患者中利尿剂的使用情况及其与死亡率之间的关系。该研究从637例患者中,最终分析了502名数据完整的患者样本。在高血压患者中,64%在住院前或住院期间均未接受利尿剂治疗(对照组),15%仅在住院期间(A组)接受利尿治疗,9%仅在住院前(B组)接受利尿剂治疗,12%在住院前和住院期间均接受利尿治疗(C组)。在校正混杂因素(年龄、性别、入院呼吸频率、共病数量、住院期间服用的其他药物的数量、气管插管)后,仅在住院期间使用利尿剂与COVID-19患者的预后恶化之间存在相关性。然而,此项研究的结果需要审慎对待,住院期间首次使用利尿剂的患者显然可能具有更为明显的体液潴留和心功能不全,然而这两个因素并未进行校正,因此这项研究的结果不能排除反向因果关系。
COVID-19急性肺损伤的病理生理机制包括一系列局部和全身反应,激活了多种促炎细胞因子,如基质金属蛋白酶。此次ESH-ISH会议上,一项来自巴西的研究调查了ICU重症COVID-19患者血浆中基质金属蛋白酶-9(MMP-9)的变化。该研究对42例临床确诊为 SARS-CoV-2感染的 ICU 住院患者和15例健康对照者进行了流行病学调查和血液标本检测,采用明胶酶谱法检测 MMP-9血浆活性。与对照组相比,COVID-19组的MMP-9活性增高(0.38±0.072 UA;95% CI=0.23-0.52,P<0.0001)。MMP-9 活性升高与性别、年龄、体重指数和或高血压均无关。该研究提示MMP-9可能是COVID-19患者急性肺损伤治疗的潜在新靶点。目前四环素类抗生素(如多西环素)具有MMP-9抑制作用,对于一些MMPs系统活性增强相关的疾病,如腹主动脉瘤,显示出潜在的治疗价值。因此,有必要开展基于MMP-9活性抑制的临床研究,探讨其潜在治疗价值。
四、小结与展望
鉴于目前COVID-19的全球大流行趋势尚未缓解,且国内间断出现小范围聚集性爆发,使得以高血压为主的慢病管理受到不小的冲击。从本次ESC-ISH大会发布的COVID-19相关研究来看,COVID-19从某种程度上加速了基于移动互联网可穿戴设备和家用遥测设备的应用进程,从而使临床医生可在新形势下探索以高血压为主的慢病管理新模式,这也是未来慢病管理大数据化的必然趋势。在2019年底爆发至今的近一年半时间内,从结构生物学研究揭示SARS-CoV2经由ACE2触发细胞感染这一重要机制的发现开始,学术界提出了RAS阻断剂与COVID-19易感性以及病程演进的潜在利弊问题,并引发争议,尤其是ACEI/ARB使用上调ACE2是否会加重COVID-19病情的问题;然而全世界的临床工作者在资源短缺和医疗挤兑的背景下,仍然在短时间内开展了大量观察性研究,初步证实ACEI/ARB至少不会加重COVID-19感染风险和恶化病情。值得欣慰的是,在短时间内,两项RCT的迅速完成,为平息这一争议提供了令人信服的科学证据。因此,在临床实践中,高血压合并COVID-19时,如患者正在使用ACEI/ARB,应继续ACEI/ARB治疗;如遇病情变化,需要停用ACEI/ARB,切换为其他降压药物也不影响患者预后。此次ESC-ISH大会的研究报道中涉及人肾脏和肺组织ACE2表达的研究,进一步证实无论是高血压还是多种降压药物,不会显着影响ACE2的表达,因此临床医生不应在降压药物的选择问题上过度纠结。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#相关研究#
35
#ESH#
34