解读新辅助/辅助关键研究数据,选择围手术期免疫最佳策略
2023-03-14 找药宝典 网络 发表于上海
早期 NSCLC 的免疫治疗可能会遵循晚期 NSCLC 中建⽴的模式,使⼤多数患者的生存率得到显著改善
免疫检查点抑制剂 (ICI) 改善了转移性 NSCLC 患者的预后,最近在多项临床试验中的研究结果确定了它们在局部或区域疾病患者的新辅助或辅助治疗中的疗效。肺癌围手术期 ICI 的前景正在迅速发展,多项临床试验即将成熟。最近相关研究数据强调了 ICI 在提高肺癌早期缓解率和降低复发率方面的潜力。发表在《美国医学会杂志》(JAMA)子刊JAMA Oncology的一篇综述,详细回顾了在围手术期使用免疫疗法治疗早期 NSCLC 的各种方法,为新辅助与辅助疗法的后续探索指明了方向。

新辅助和辅助免疫疗法凭借关键的3 期研究 IMpower010、KEYNOTE‑091/PEARLS和 CheckMate -816以及正在进行的多项其他研究中令人⿎舞的数据,带领我们进入了早期 NSCLC 治疗的新时代。本综述侧重于使用免疫疗法改善可切除 NSCLC 患者预后的新数据。

新辅助免疫疗法

新辅助化学疗法和免疫疗法的组合
一、 新辅助阿替利珠单抗联合化疗
由于化学疗法有可能从垂死的肿瘤细胞中释放抗原,从而刺激和启动抗原特异性 T 细胞的扩增,因此在化疗的同时添加免疫检查点抑制剂 (ICI) 的前景令人充满期待。鉴于此,Shu 及其同事进行了一项单臂 2 期试验,其中 30 名患者接受了新辅助阿替利珠单抗联合铂类双药化疗(卡铂和白蛋白结合型紫杉醇),共 4个周期。主要终点是主要病理反应 (MPR),定义为手术时存在10% 或更少的残留活肿瘤,57%(30 名中的 17 名)患者出现这种反应,并未出现影响手术切除与治疗相关的不良反应,也没有与治疗相关的死亡。
二、 CheckMate -816 研究
在 3 期随机 CheckMate -816 试验中,358 名新诊断、可切除的 IB ⾄ IIIA 期患者(没有已知 EGFR 或 ALK 突变的非⼩细胞肺癌患者)⼊组,接受 3 个周期的新辅助纳武利尤单抗联合铂双药化疗或在根治性切除前单独化疗。研究的主要终点是病理学完全缓解 (pCR)(定义为切除的肺和淋巴结中 0%的活肿瘤)和⽆事件生存期 (EFS),关键的次要终点是 MPR、OS 和时间死亡或远处转移。
结果显示:纳武利尤单抗联合化疗组的中位 EFS 为 31.6 个月,而单独化疗组为 20.8 个月(HR=0.63;P=0.005)。此外,纳武利尤单抗联合化疗组中 24% 的患者达到 pCR,而对照组为 2.2%。
在所有分析的亚组中都观察到纳武利尤单抗带来的额外益处,尤其对于具有以下特征的患者更为明显:年龄小于 65 岁,女性,来自亚洲,ECOG体能评分为0,IIIA 期疾病,非鳞状细胞组织学,从不吸烟,PD‑L1> 50%,并接受卡铂治疗。
在接受新辅助化免联合疗法的患者中,后续进行微创手术更常见,而全肺切除术更少见,这些患者没有手术延迟或治疗相关不良事件的实质性差异。基于这些结果,FDA 批准了新辅助纳武利尤单抗加化疗用于治疗早期肺癌。试验报告了 OS 的中期分析,其中任一治疗组均未达到中位 OS;期待后续成熟的OS数据结果公布。

单药新辅助免疫疗法
一、 LCMC3 研究
2 期 LCMC3 研究对 181 名未经治疗的 IB ⾄ IIIB 期可切除 NSCLC 患者进行了最多 2 个周期的阿替利珠单抗术前治疗。在无已知EGFR 或 ALK 突变的队列中,20.4% 的患者实现了 MPR,6.8% 的患者实现了 pCR。
有趣的是,该研究发现未达到MPR患者中STK11/LKB1和KEAP1突变更常见。同样,在KRAS突变晚期的NSCLC较少发现携带STK11和KEAP1突变,这些异常与免疫反应基因的低表达相关,表明肿瘤免疫微环境较冷。最近,一项多机构回顾性队列研究还表明,STK11 和 KEAP1 癌症突变与在 KRAS 突变的晚期 NSCLC 患者中进行 ICI 治疗后更差的结果相关,但在具有野生型 KRAS 的肺腺癌患者中则不然。
二、 PRINCEPS 研究
单组 2 期 PRINCEPS 试验对30 名临床分期为 IA ⾄ IIIA 的非小细胞肺癌患者(仅限非 N2)给予单剂量的阿替利珠单抗治疗,未观察到MPR。作者的结论是,阿替利珠单抗治疗和手术之间的短暂间隔(发生在3-4周免疫治疗后)可能解释了这一特定研究中缺乏反应的原因。在新辅助治疗PEM-brolizumab的1期研究中也观察到了这一现象,其中所有达到MPR的患者在首次治疗和手术之间都有相对较长的间隔。
总体而言,单药新辅助免疫治疗的结果差异很⼤,MPR 在相对较小的研究中介于 14% 到 40% 之间,但这些提供了新辅助免疫治疗是安全的证据,并且可以与有意义的放射学和病理学反应相关联。
辅助免疫治疗
一、IMpower 010 试验
IMpower 010 试验是首个在完全切除的 IB ⾄ IIIA 期NSCLC 患者中测试铂类化疗后阿替利珠单抗辅助治疗获益的随机 3 期研究。共有1005 名患者随机接受每 3 周一次的阿替利珠单抗治疗,持续时间长达1 年(16 个周期)或最佳支持治疗;主要终点是研究者评估的DFS(对不同患者人群进行分层评估)。
在进行32.2个月的中位随访后,与最佳支持治疗相⽐,阿替利珠单抗可改善所有 II ⾄ IIIA 期患者的DFS (HR, 0.79; P = .02),在 PD-L1 表达≥1%的患者中DFS显著改善 (HR, 0.66; P = .004)。
值得注意的是,PD‑L1 > 50% 患者的 DFS 获益最⼤(HR = 0.43)。EGFR 突变阳性 NSCLC 患者 (n = 43) 的 DFS HR 为 0.57 (vs 0.67 EGFR 突变阴性 NSCLC [n = 248) ]),这表明 EGFR 突变阳性 NSCLC 患者可能会从辅助免疫治疗中获益,尽管这一发现是基于总研究人群的一小部分。ALK 阳性 NSCLC 患者的DFS(HR=1.05(95% CI,0.32‑3.45),表明这部分患者辅助免疫治疗没有获益。
第一次预先指定的 OS 中期分析显⽰,在 PD-L1 > 1% 的人群中有阿替利珠单抗的获益趋势(HR=0.71 [95% CI,0.49-1.03 ]),在 PD‑L1 > 50% 的队列中观察到最⼤的生存获益(HR,0.43 [95% CI,0.24‑0.78])。
在接受阿替利珠单抗治疗的 495 名患者中,有53 名 (11%) 患者发生免疫相关的 3 级和 4 级不良事件, 4 名 (1%)患者发生 5 级事件。总的来说,这些结果表明没有新的安全问题。基于这项研究的结果,美国FDA 批准在PD-L1表达≥1%的 II ⾄ IIIA 期 NSCLC 患者中使用阿替利珠单抗进行辅助治疗(在手术切除和铂类化疗后)。
二、 PEARLS 研究
3 期 PEARLS 研究入组了 1117 名确诊为 IB ⾄ IIIA 期 NSCLC 的患者,这些患者在完全手术切除且切缘阴性并提供肿瘤组织进行 PD‑L1 检测后被确诊。 最多允许进行 4 个周期的辅助化疗。患者被随机分组,每 3 周接受一次帕博利珠单抗或安慰剂,持续长达 1 年。该试验有双重主要终点(整体研究人群DFS和 PD-L1 ≥50% 人群的DFS)。
在中位随访 35.6 个月的情况下,总体人群的预估中位 DFS 为 58.6 个月,帕博利珠单抗为 42 个月(HR,0.76;P = .001),而PD-L1>50%的中位DFS在两组中均未达到。亚组分
析表明,帕博利珠单抗对当前吸烟者、非鳞状组织学患者和 EGFR 改变患者更有益。关于化疗的亚组分析显⽰,接受辅助化疗的患者 (n = 1010;HR=0.73) 与未接受辅助化疗的患者 (n = 167;HR=1.25 )相⽐,DFS 获益更⾼。在接受辅助化疗的患者中,DFS因周期数和化疗方案而异,在接受3 ⾄ 4 个周期化疗并接受卡铂加长春瑞滨的患者获益更⼤。
令人惊讶的是,PD-L1 1% 至49%患者的获益程度高于 PD-L1 ≥50%的患者。在不良事件方
面,34.1% 的帕博利珠单抗治疗患者发生3⾄5级治疗相关的不良事件,而安慰剂组为 25.8% .总体而言,这些数据表明,无论PD-L1 表达如何,帕博利珠单抗也可能作为 I ⾄ IIIA 期 NSCLC 患者在完全切除和辅助化疗后的另一种辅助治疗选择。
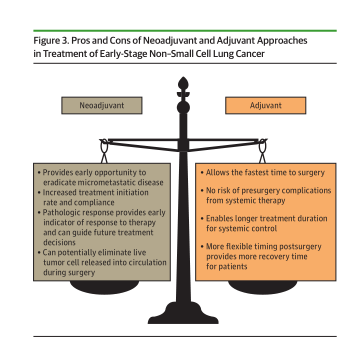
新辅助与辅助疗法的优缺点
目前有⼏项 3 期研究正在进行中,使用不同的 ICI 来确定序贯新辅助化学免疫疗法和辅助免疫疗法是否可以提⾼生存率。关于改善EFS和预测OS中EFS真实价值还有待进一步研究。

术前新辅助免疫治疗有望为患者带来独特的治疗益处,如早期根除微小转移灶、较高的治疗启始率/较高患者依从性、带来手术降期的可能、大范围手术(如肺切除术或开胸手术)需求潜在降低、提供评估病理学缓解程度的机会(病理学缓解程度可作为生存的预测因子并为未来治疗决策提供信息)。
辅助治疗可缩短手术时间,并降低术前全身治疗相关并发症的风险。此外,辅助治疗可延长全身治疗时间,在恢复期间,可以进行基因检测,可能有足够的标本来帮助指导辅助治疗的选择。
结论
虽然在过去 20 年的⼤部分时间里,可切除 NSCLC 辅助化疗的阳性试验模式已使辅助治疗成为早期 NSCLC 患者的标准治疗模式,但新辅助免疫治疗、辅助免疫治疗新数据的披露正在迅速改变默认的治疗标准。早期 NSCLC 的免疫治疗可能会遵循晚期 NSCLC 中建⽴的模式,使⼤多数患者的生存率得到显著改善。然而还需进一步确认免疫疗法与其他系统疗法的最佳时机、持续时间以及治疗顺序。
参考文献:
Desai AP, Adashek JJ, Reuss JE, West HJ, Mansfield AS. Perioperative Immune Checkpoint Inhibition in Early-Stage Non-Small Cell Lung Cancer: A Review. JAMA Oncol. 2023 Jan 1;9(1):135-142. doi: 10.1001/jamaoncol.2022.5389. Erratum in: JAMA Oncol. 2023 Jan 1;9(1):151. PMID: 36394834.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言