LAG3 能否掀起免疫治疗下一波热潮?
2022-12-02 找药宝典 找药宝典 发表于上海
免疫治疗单药的疗效具有一定的局限性,探索PD1/PDL1最佳治疗拍档成为临床研究的热点。今年3月,BMS靶向淋巴细胞活化基因 3(LAG3,CD223)的单抗药物Relatlimab联合 Nivolu
免疫治疗单药的疗效具有一定的局限性,探索PD1/PDL1最佳治疗拍档成为临床研究的热点。
今年3月,BMS靶向淋巴细胞活化基因 3(LAG3,CD223)的单抗药物Relatlimab联合 Nivolumab (O药)获批用于治疗转移性黑色素瘤。作为首款获得 FDA 批准的 LAG3 单抗组合疗法,LAG3 或将成为继 PD-1 和 CTLA-4 之后第三个应用于临床的热门流量免疫检查点!

早在2021年9月20日,FDA就授予百时美施贵宝公司的LAG-3抗体relatlimab和抗PD-1抗体Oppo(nivolumab,o药)构成的固定剂量组合的生物制品许可申请(BLA)优先审评资格,用于治疗患有不可切除/转移性黑色素瘤的成人和儿童患者。

该项审批结果是根据一项在2021年美国临床肿瘤学会(ASCO)上公布的2/3期一项名为RELATIVITY-047 Ⅲ期的全球双盲随机试验,旨在评估Relatlimab联合Nivolumab作为一种新型固定剂量的联合药物,对比Nivolumab单药治疗之前未经治疗的转移性或不可切除的黑色素瘤患者的疗效。
试验患者按1∶1比例随机进行分配,分别接受Relatlimab 160mg和Nivolumab 480 mg固定剂量组合或单药Nivolumab 480 mg治疗,两组患者均为每4周静脉滴注一次药物。根据LAG-3表达(≥1%或<1%)、PD-L1表达(≥1%或<1%)、BRAF V600突变状态和转移分期(M0或M1乳酸脱氢酶[LDH]水平正常vs. M1乳酸脱氢酶水平升高)进行分层,直到患者出现疾病进展,不可接受的不良反应,或撤回同意。
试验主要终点为盲法独立中心评价的无进展生存期(PFS)。次要终点包括总生存期(OS)和客观缓解率(ORR)。
结果表明,Relatlimab联合Nivolumab的中位无进展生存期(PFS)vs而Nivolumab组PFS 10.1个月(95%CI:6.4~15.7)vs 4.6个月(95% CI:3.4~5.6,P=0.006);不仅如此Relatlimab联合Nivolumab治疗患者12个月PFS vs 单药使用Nivolumab12个月 :47.7%(95%CI:41.8~53.2)vs 36.0%(95%CI:30.5~41.6)。
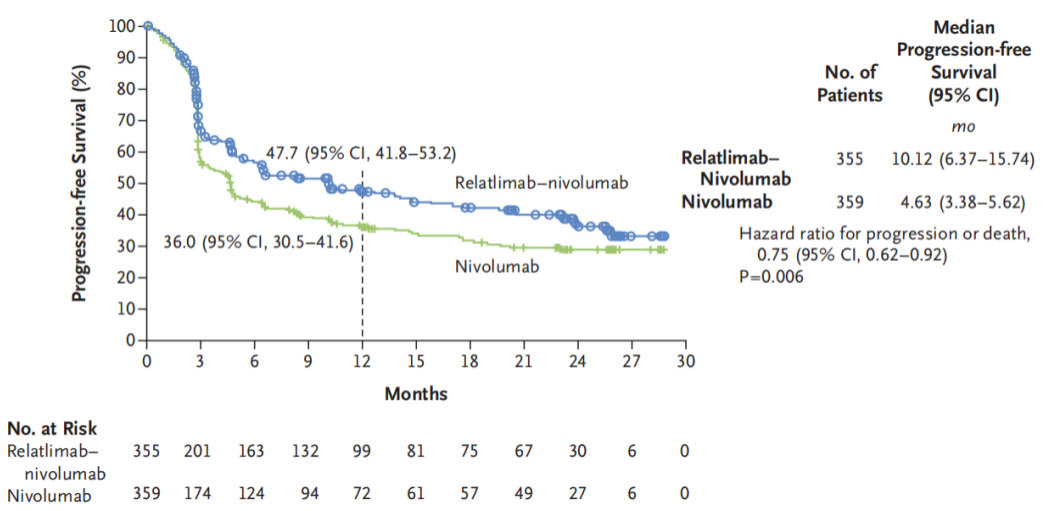
数据结果表明,与PD-1单药治疗相比,使用LAG-3+PD-1双免联合疗法的中位PFS显著延长,这表明对于既往未经治疗的转移性或不可切除的黑色素瘤患者,双免联合更加有效。
LAG-3:肿瘤的另一个免疫调节因子
LAG3(lymphocyte activation gene 3)是一种免疫检查点受体蛋白,主要表达在活化的T细胞、NK细胞、B细胞和浆细胞树突细胞。LAG3主要通过与配体MHC II分子的结合,下调T细胞的活性。同时,LAG3也可增强调节性T细胞(Treg)的抑制活性。利用治疗性抗体抑制LAG3,可解除对T细胞的抑制,增强机体免疫应答。于是,LAG-3调节剂被研发,而immutep在研的IMP321是可溶性LAG-3融合蛋白,属于LAG-3调节剂的一种。
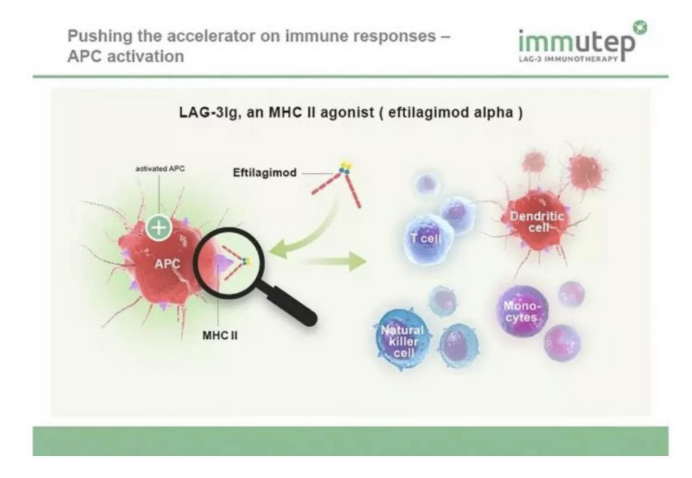
在多种癌症类型中,如黑色素瘤、结肠癌、乳腺癌等,肿瘤浸润淋巴细胞(TILs)表达LAG-3,这与癌细胞侵略性的临床特征相关联。而阻断LAG-3则可以逆转以上的抑制作用,恢复CD8+T细胞增殖和活性,并减少调节性T细胞数量;而且还提高了T细胞免疫应答的敏感度。同时再阻断PD-1,免疫反应会协同性增强,抑制肿瘤。
LAG-3疗法联手PD-1不仅应用于黑色素瘤,
一线治疗肺癌疗效翻倍!
有研究表明,一款可溶性LAG-3融合蛋白eftilagimod alpha(efti,又名IMP321)与PD1单抗联用,在2期试验中取得积极的研究结果。可以一线治疗晚期NSCLC(非小细胞肺癌)患者,其ORR(客观缓解率)达到47%。二线治疗头颈鳞癌患者,ORR达到33%。且无论患者的PDL1表达如何,该方案都可见效。

Nature发文,LAG3+PD-1新辅助治疗疗效优异
近期发表在Nature上的一项研究(2期,NCT02519322)探索了LAG3+PD-1组合新辅助疗法的临床疗效。

结果显示,在可评估的30名患者,29名(97%)进行了手术。其中17名(57%)患者获得病理完全缓解(pCR),2例(7%)接近pCR(Near pCR),2例(7%)部分病理反应(pPR),合计70%的患者有病理缓解反应。8例(27%)无病理反应(pNR)。

中位随访24.4个月(范围为7.1-34.6个月),30例接受治疗的患者1年和2年的无事件生存率分别为90%和81%。1年和2年的RFS率(接受手术患者从手术到复发的时间)分别为97%和82%。有pCR患者的1年和2年RFS率分别为100%和91%,而无pCR患者的RFS率分别为92%和69%(P=0.10)。
全球LAG3抑制剂研发现状
虽然目前获批上市的LAG3抑制剂只有一款,但全球已经有多款LAG抑制剂进入临床研究。
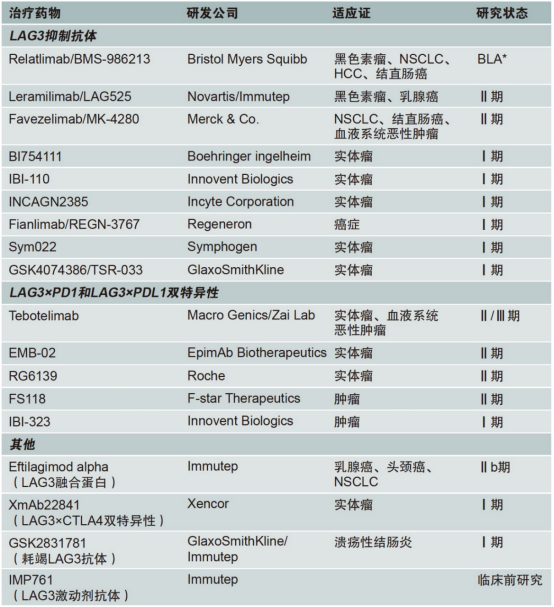
来源:Biomedtracker、Cortellis以及公司网站。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














#LAG3##肿瘤免疫治疗##靶点#
64