这种病毒90%的人都有感染,不仅诱导染色体断裂,还引发多发性硬化症
2023-05-31 风立宵 生物探索 发表于上海
EBNA1和CRYAB之间的抗体交叉反应,会使得身体中的某种抗体错误地攻击大脑和脊髓,导致引发MS。
Epstein-Barr病毒(Epstein-Barr virus,EBV),也被称为人类巨细胞病毒4(Human herpesvirus 4,HHV-4),是一种广泛存在于人类群体中的病毒,据统计,全球90%以上的人口都有感染。大多数人都是在儿童时期就被感染,通常不会引起症状,并在人体内潜伏持续一生,不过有时会在年轻人身上引起俗称“接吻病”的传染性单核细胞增多症,表现为发热、咽喉疼痛、淋巴结肿大等症状。
然而,EBV的危害并不局限于此。过去,科学家发现EBV与多种类型的癌症相关,包括淋巴瘤、鼻咽癌和胃癌等。还有证据表明EBV与系统疾病多发性硬化症(multiple sclerosis,MS)之间存在联系,然而,EBV为何在某些人身上表现得如此凶险,其背后的分子机制尚不明了。
EBV编码的蛋白诱导11q23断裂
4月12日,美国加利福尼亚大学圣地亚哥分校的博士后Julia Su Zhou Li及同事在Nature上发表论文“Chromosomal fragile site breakage by EBV-encoded EBNA1 at clustered repeats”。论文指出,EBV编码的蛋白质EBNA1(Epstein–Barr nuclear antigen 1)可通过与人类11号染色体上的特定区域结合并触发断裂,从而导致基因组不稳定。

图1 研究成果(图源:[1])
EBNA1是在所有EBV相关癌症中表达的唯一病毒蛋白,能够与EBV基因组中的多个特定序列结合,使之能够持续存在和复制。之前的生物化学和结构研究已经确定了EBNA1的DNA结合域与18碱基对回文DNA序列的相互作用。这一发现促使人们思考,EBNA1是否也能够识别宿主DNA中的特定序列并与之结合。过去通过对EBV感染的淋巴细胞的研究,已经发现了许多可能的靶序列,其中包括在11号染色体上位于FAM55D和FAM55B基因的一组高亲和力EBNA1位点。然而,学界尚未达成共识。
Li及其同事在原代细胞系和癌细胞系等几种EBV阴性细胞系中表达EBNA1并进行观察。他们发现,EBNA1在原代细胞系和癌细胞系细胞核中的两个不同位点高度富集。将EBNA1结合位点映射到11q23的一个21kb的重复序列区域后,Li发现该区域存在一个18bp序列的300多个拷贝。该序列与病毒上的18碱基回文DNA序列非常相似,而破坏这一位点则会消除EBNA1的富集。
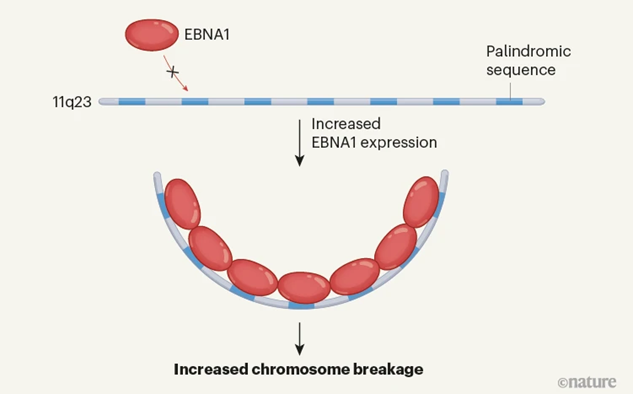
图2 EBNA1蛋白结合并破坏人类11号染色体(图源:[2])
通过进一步的观察,Li及其同事发现11号染色体上的这一区域存在DNA脆性位点。在EBV潜伏感染的细胞中,将EBNA1的蛋白质浓度提高两倍,就足以触发11q23断裂。而且,11q23的这个EBNA1区域位于肿瘤抑制基因ATM和原癌基因MLL之间,断裂如果发生,细胞分裂后子细胞中的这些基因的拷贝数就极易发生改变。
Li及其同事还发现,EBNA1的另一个区域能与一种名为泛素特异性蛋白酶7(ubiquitin-specific protease 7,USP7)的细胞酶相互作用。USP7能够刺激EBNA1的DNA结合活性,ENBA1又反过来促进了USP7的募集,同时,USP7还能去除核小体蛋白质中的泛素修饰。这提示了USP7在染色质结构改变中的双重作用。
Li及其同事还调查了11q23断裂在EBV相关癌症中的发生率。结果发现,在人类鼻咽癌中,81%的肿瘤样本中在11号染色体上表现出结构变异。另外作者还考察了2000多种不同类型癌症的全基因组测序数据,发现与EBV阴性肿瘤相比,EBV阳性肿瘤的11号染色体结构变异有所增加。
虽然尚不清楚EBNA1诱导的11q23断裂是由于DNA结合域引起了DNA的结构变化,还是USP7造成了染色质结构变化,或是出于其他可能,但可以确定的是,EBNA1在促进癌症发展中的直接作用。
EBNA1与CRYAB之间交叉抗体反应引发MS
瑞典卡罗林斯卡学院临床神经科学系的博士后研究员Olivia Thomas和同事则在5月17日在Science Advances发表题为“Cross-reactive EBNA1 immunity targets alpha-crystallin B and is associated with multiple sclerosis”的论文。他们在文中指出,EBNA1和CRYAB之间的抗体交叉反应,会使得身体中的某种抗体错误地攻击大脑和脊髓,导致引发MS。

图3 研究成果(图源:[3])
研究人员分析了700多名MS患者和700多名健康人的血液样本。结果发现,在MS患者身上,抗CRYAB蛋白的自身抗体增加。CRYAB蛋白全称αB-结晶蛋白(Alpha-B Crystallin),是一种热休克蛋白,存在于人体的细胞中,并参与细胞的保护和应激响应。当高EBNA1抗体反应和抗CRYAB血清阳性在一个人身上同时发生时,疾病风险尤其增加。
分析EBNA1和CRYAB的氨基酸序列,研究人员发现,CRYAB第8至20位氨基酸与EBNA1第399至408位氨基酸之间存在高度序列同源性,而在血浆中掺入对应的EBNA1肽可降低对CRYAB 肽的反应性,这表明CRYAB 自身抗体与EBNA1之间存在交叉反应。

图4 EBNA1和CRYAB氨基酸序列的比对(图源:[3])
在小鼠身上,研究人员还发现存在EBNA1和CRYAB 之间的T细胞交叉反应。在使用那他珠单抗(Natalizumab)治疗的MS患者身上,发现T细胞对CRYAB和EBNA1的反应增加且高度相关,这表明EBNA1引发了T细胞对CRYAB的敏感。
值得注意的是,抗CRYAB蛋白的自身抗体存在于大约23%的MS患者和7%的健康个体身上。“这表明,虽然这些抗体反应不是在疾病进展过程中必然发生的,但仍可能与多达四分之一的MS患者有关。”Olivia说,“这也证明了患者之间存在高度差异性,开发针对性的个性化疗法是十分必要的。”
论文的共同第一作者、卡罗林斯卡医学院临床神经科学系附属研究员Mattias Bronge表示:“我们将扩大当前的研究,包括T细胞如何对抗EBV感染,以及这些免疫细胞是如何损害MS患者的神经系统并促进疾病进展的。”目前,现有的疗法仅能减少MS复发,但不能阻止疾病进展。
参考资料:
[1Li, J.S.Z., Abbasi, A., Kim, D.H. et al. Chromosomal fragile site breakage by EBV-encoded EBNA1 at clustered repeats. Nature 616, 504–509 (2023). https://doi.org/10.1038/s41586-023-05923-x
[2]https://www.nature.com/articles/d41586-023-00936-y
[3]Thomas OG, Bronge M, Tengvall K, et al. Cross-reactive EBNA1 immunity targets alpha-crystallin B and is associated with multiple sclerosis. Sci Adv. 2023 May 19;9(20):eadg3032. doi: 10.1126/sciadv.adg3032.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言