浅表 CD34 阳性纤维母细胞性肿瘤的临床病理特点
2023-03-29 衡道病理 网络 发表于上海
浅表 CD34 阳性纤维母细胞性肿瘤的临床病理特点,一文详解。
2022年10月,哈佛医学院病理学系William J. Anderson博士为第一作者,在病理学顶尖期刊《American Journal of Surgical Pathology》(IF值为6.298分)上发表题为
“Superficial CD34-Positive Fibroblastic Tumor:
A Clinicopathologic, Immunohistochemical,and Molecular Study of 59 Cases”
的研究型文章,通过对收集病例的分析,详尽总结了SCPFT的临床病理学特点及分子遗传学改变。甘肃省人民医院病理科陈旭医生对这篇文献要点进行了编译,供大家参考。

甘肃省人民医院病理科
主治医师 陈旭
研究历史
临床表现
-
患病男女比例相当,年龄从14岁到85岁不等(中位年龄:42岁)。
-
通常表现为皮下组织内、筋膜上长期存在的无痛性肿块,与肌肉组织无粘连,偶尔也有毗邻或局灶性累及筋膜(13%)。病史常在 1 年以上,有的可达十年,无特殊全身表现。 -
好发于下肢(73%),其中大部分发生在大腿(42%)。偶尔发生于上肢(8%)、背部(7%)和锁骨上区域(3%)。极少发生于颈部、胸部、腋窝、腹壁和乳房。乳房SCPFT可伴发对侧乳房的叶状肿瘤。 -
部分患者在首次切除时切缘呈阳性,有个别患者复发或发生远处转移。
组织病理学特点
1、肿瘤中位大小为3.0cm(范围:1.0~9.0cm)。大体上,大多数肿瘤边界清楚,有纯褐色/米褐色的切面(图1),没有坏死。
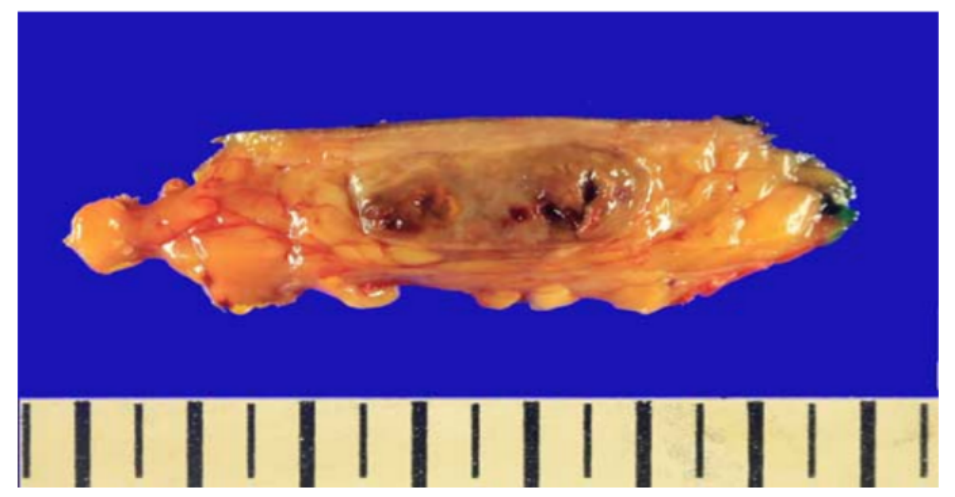
图1. SCPFT的大体特征。总体而言,SCPFT是典型的皮下肿块,切面为棕灰色/白色。有时可以发现出血的区域,但没有坏死。
2、显微镜下,肿瘤在低倍镜下呈局限性分布,常伴有周围淋巴细胞聚集(图2)。在高倍镜下,可见浸润性生长的区域。肿瘤由纺锤形和多形性细胞组成,胞质通常为嗜酸性,可呈“玻璃样”(图3)。
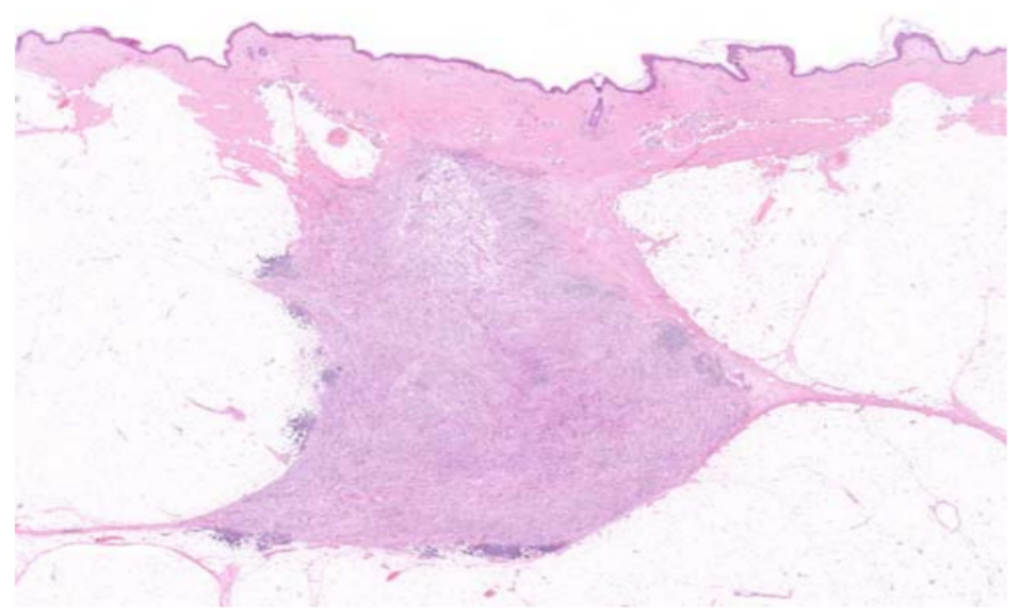
图2. 在低倍镜下,SCPFT通常表现为界限清晰的肿块,内含实性细胞,可见外周淋巴细胞聚集。
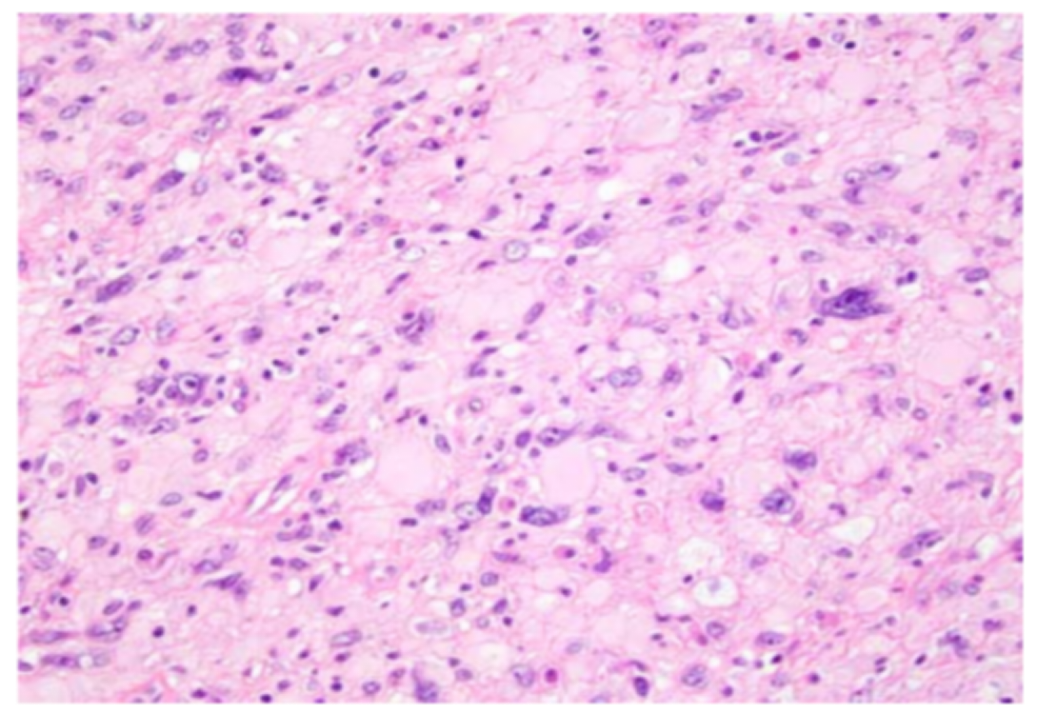
图3. 肿瘤细胞有多形性的细胞核和明显的“玻璃状”细胞质。
3、所有细胞均具有明显的核多形性,常伴有深染、一个或多个明显的核仁、假包涵体,以及多核。虽然多形性细胞通常很丰富,但在个别病例中,它们分散在主要的成纤维细胞梭形细胞群中。在一部分病例(19%)中,可见颗粒细胞变化,通常是小簇细胞(图4A)。
组织细胞、淋巴细胞和浆细胞浸润非常常见(图4B),还有含铁血黄素沉积灶,间质主要是纤维状的,粘液样区域非常少见。偶尔会出现细胞质呈脂化/空泡化的细胞(图5A)。个别肿瘤包含化生骨(图5B)。
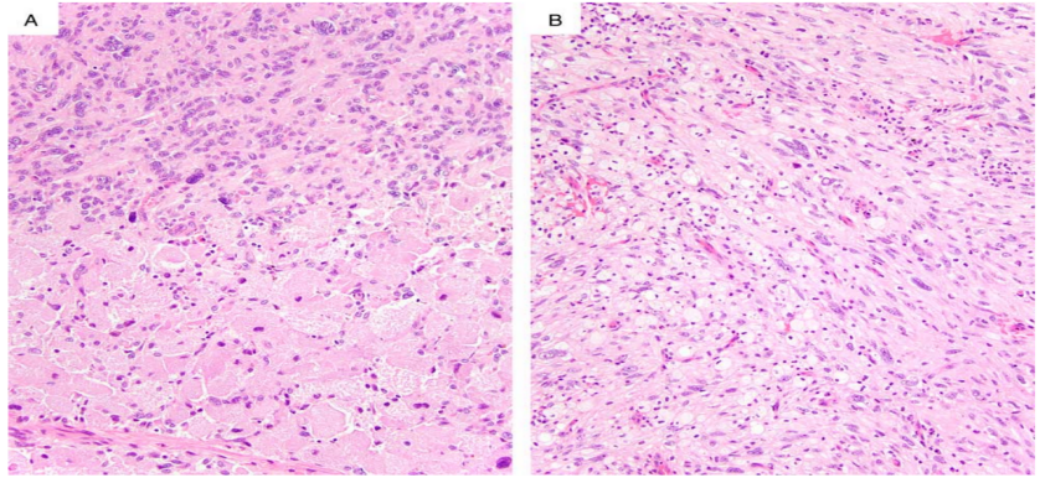
图4. (A)19%的SCPFT中存在颗粒细胞改变。(B)组织细胞、淋巴细胞和浆细胞的浸润是常见的。
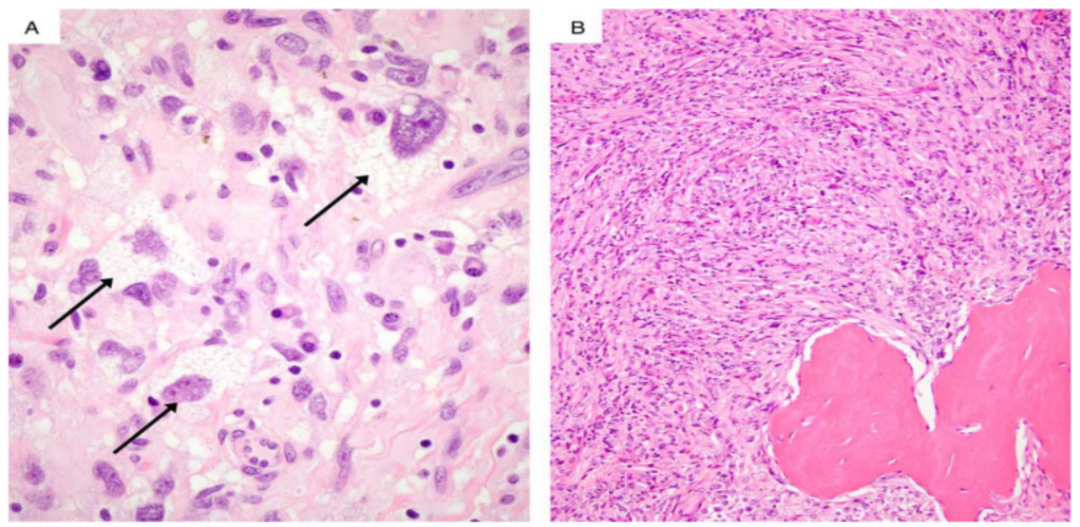

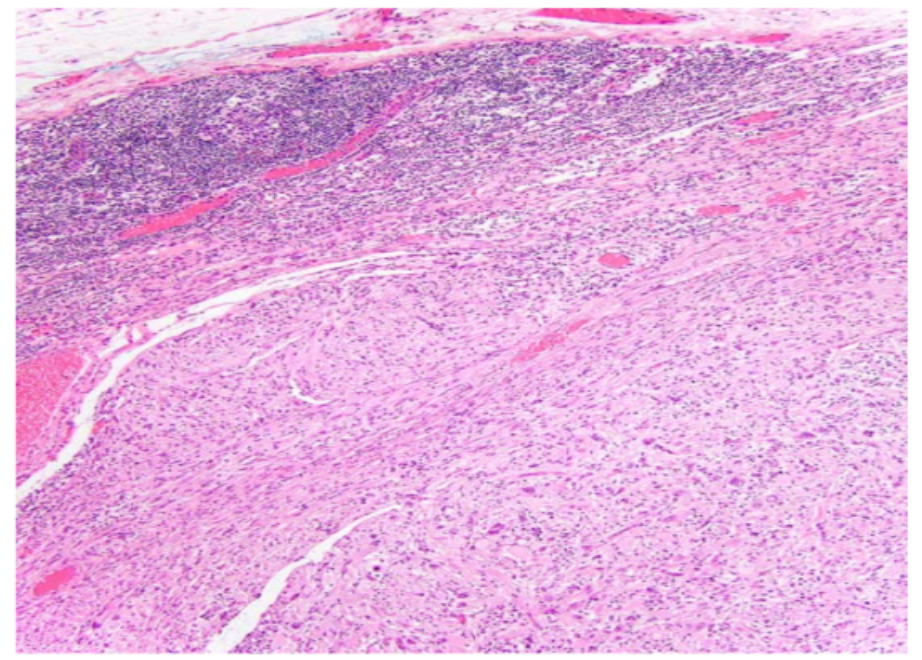
图7. 转移性SCPFT累及区域淋巴结。该肿瘤在形态学上与原发性SCPFT相似,且有丝分裂活性非常低。
免疫组织化学染色
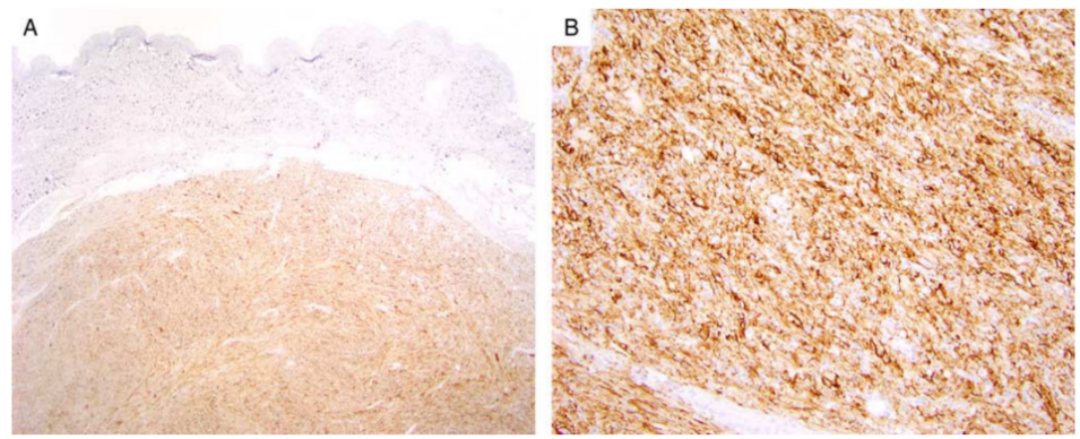
图8. CADM3在SCPFT中的表达。(A)在低倍镜下,SCPFT为典型的弥漫性阳性表达,与周围阴性染色的间质界限分明。(B)在肿瘤细胞的胞浆中呈弥漫强阳性表达。
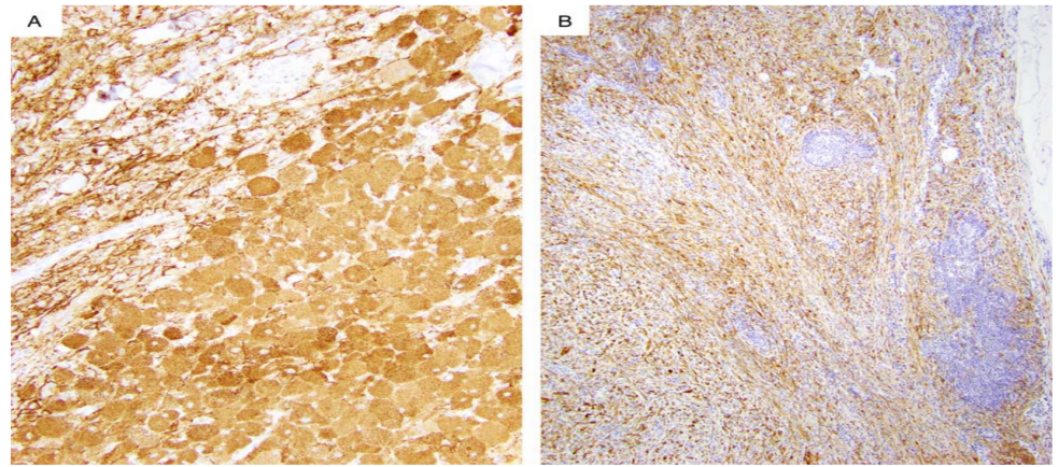
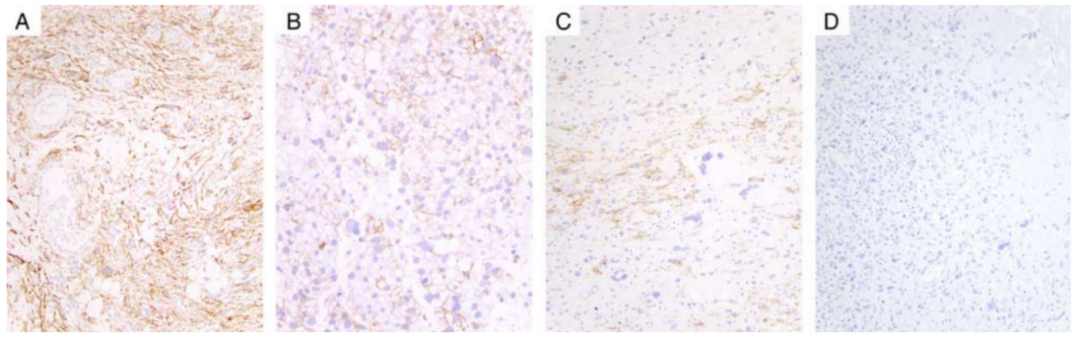
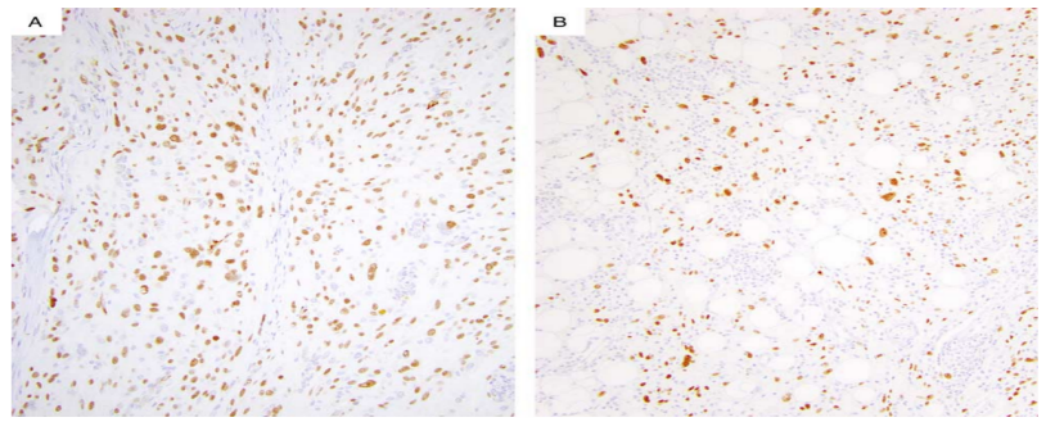
图11. SCPFT中WT1的表达。(A)WT1在52%的SCD34FT中呈弥漫性阳性。(B)当呈阳性时,WT1清晰地显示了肿瘤细胞的细胞核。
分子遗传学改变
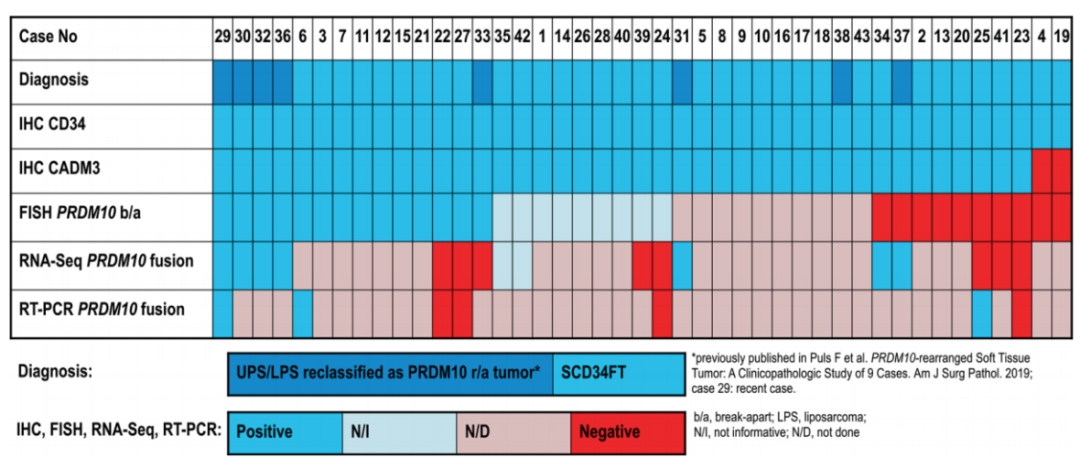
图12. 18例PRDM10重排的患者中,7例最初分类为未分化多形性肉瘤或脂肪肉瘤,11例分类为SCPFT。所有发生PRDM10重排的肿瘤均表达CADM3。图片源自于Modern Pathology (2022) 35:767–776; https://doi.org/10.1038/s41379-021-00991-8
分子遗传学改变
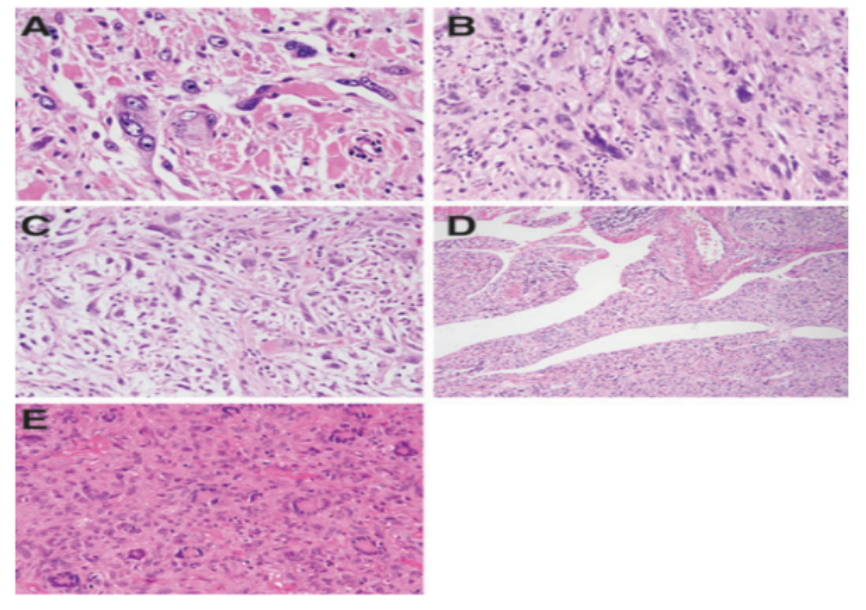
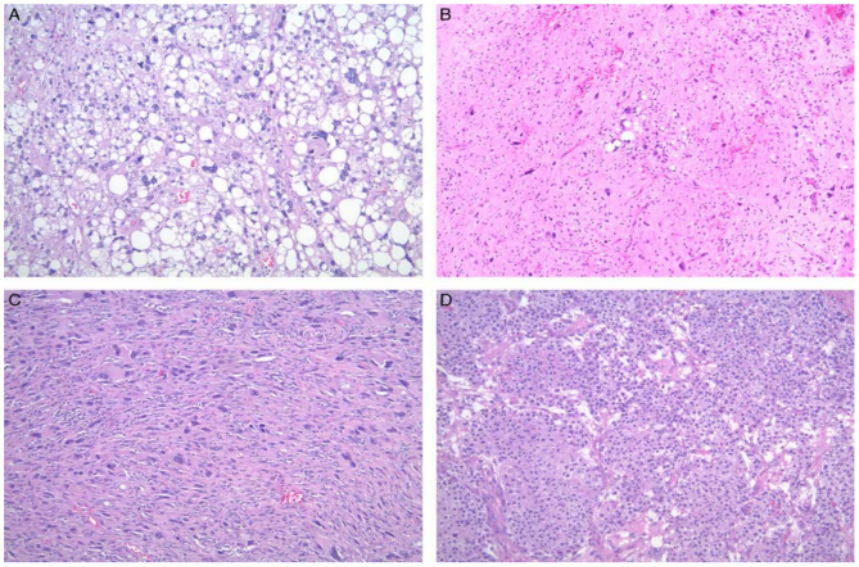

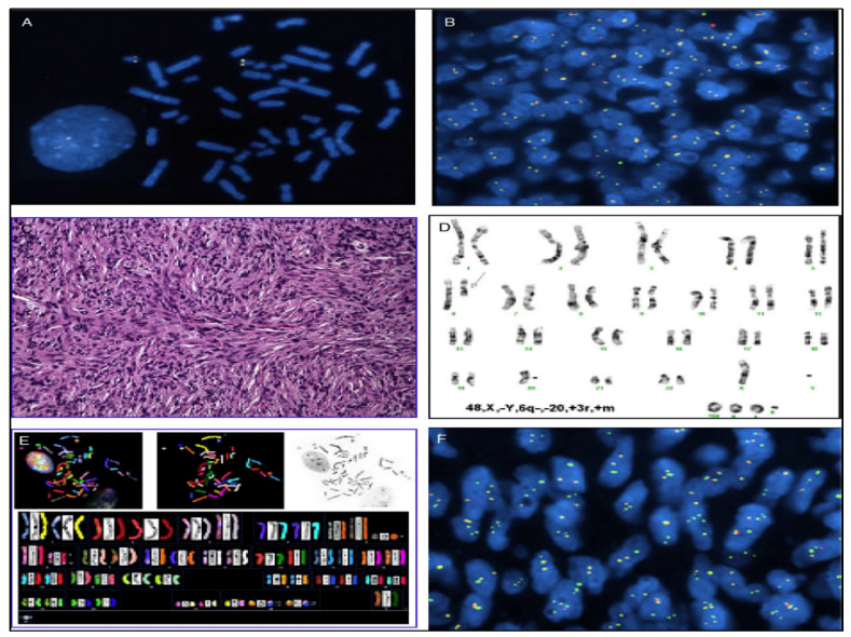

图17. MIFS组织学特点。(A)从具有明显核仁(箭头)的轻度增大的泡状核、胞浆丰富的肿瘤细胞,到具有病毒细胞样核仁的大细胞。肿瘤细胞的特点包括(B)神经节样细胞,胞浆丰富、大泡状核,具有病毒细胞样核仁,(C)上皮样肿瘤细胞,伴增大、轮廓不规则的细胞核、模糊的异染色质和(D)非典型假成脂细胞,胞浆可见明显膨胀的粘蛋白液泡。图片源自于Am J Surg Pathol 2014;38:1–12。
治疗及预后
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







