肥胖治疗新靶点:惠晓艳/吴东海团队揭示雄激素受体对米色脂肪细胞的负调控
2023-05-27 生物世界 生物世界 发表于上海
该研究揭示了雄激素受体(AR)通过直接抑制米色脂肪激活的关键分子PRDM16的表达,负向调控米色脂肪细胞活性。这一新发现可能为开发靶向PRDM16的抗肥胖和抗代谢疾病药物提供一个良好的治疗窗口。
据世界卫生组织(WHO)估计,全世界有13%的成年人患有肥胖症。更重要的是,肥胖还会进一步引发代谢综合症并伴随各种并发症,例如2型糖尿病、高血压、非酒精性脂肪性肝炎(NASH)、心血管疾病以及癌症。
人类主要有两类脂肪:白色脂肪和褐色脂肪,白色脂肪负责储存能量,褐色脂肪负责产热耗能。米色脂肪是一类新发现的脂肪,其静息时表现出白色脂肪的特质,而在寒冷或β肾上腺素能受体激动剂等激活的情况下,具有褐色化潜力,促进产热和能量消耗,改善机体糖脂代谢,显示出巨大的可塑性。
近年来研究发现,成年人体内的白色脂肪在特定条件下可转变成米色脂肪,从而将机体多余能量以热量形式消耗。激活米色脂肪成为目前防治肥胖与代谢疾病的重要方式。
近日,中国科学院广州生物医药与健康研究院吴东海团队和香港中文大学惠晓艳团队合作,在 Advanced Science 期刊发表了题为:Androgen Receptor is a Negative Regulator of PRDM16 in Beige Adipocyte 的研究论文。
该研究揭示了雄激素受体(AR)通过直接抑制米色脂肪激活的关键分子PRDM16的表达,负向调控米色脂肪细胞活性。这一新发现可能为开发靶向PRDM16的抗肥胖和抗代谢疾病药物提供一个良好的治疗窗口。

PRDM16是白色脂肪细胞褐色化的关键转录因子。在该研究中,研究团队通过PRDM16报告小鼠模型和单克隆筛选技术,系统性分析了细胞全转录因子谱(1600个)与PRDM16的表达水平相关性,发现雄激素受体(AR)与PRDM16呈现最强的负相关性。
细胞及动物水平实验进一步证实雄激素受体直接结合Prdm16基因位点,抑制其转录表达,脂肪细胞特异性敲除雄激素受体小鼠的米色脂肪细胞活性增强,而脂肪细胞高表达雄激素受体的小鼠则表现出米色化减弱。
值得一提的是,该研究同时发现人体脂肪组织中PRDM16 的表达存在性别差异——相比男性个体,女性具有更高的PRDM16表达水平,从临床上证实了雄激素及其受体通路对PRDM16和米色脂肪的抑制作用。
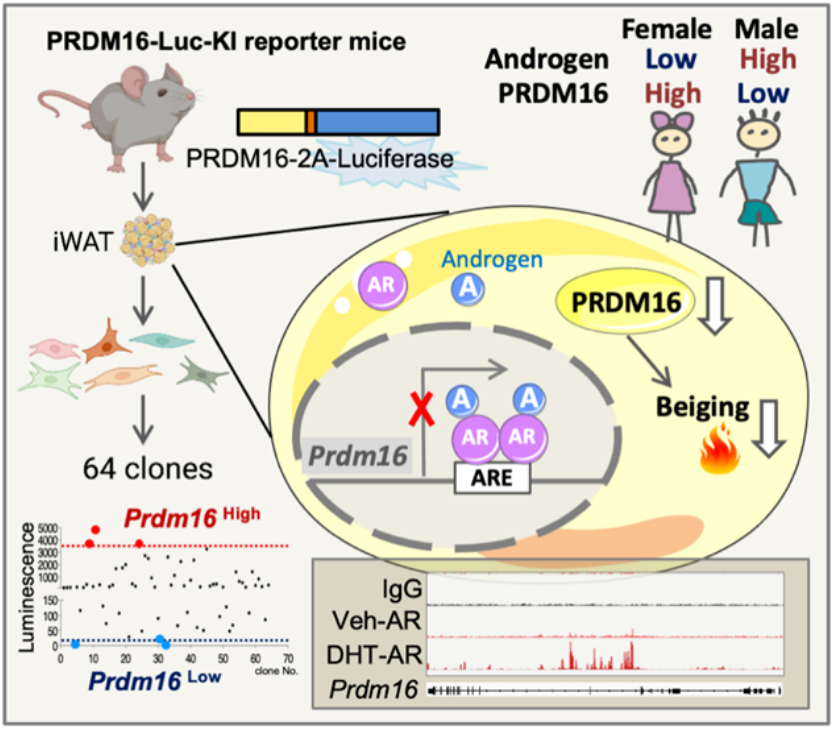
雄激素受体负调控米色脂肪细胞活性作用与机制示意图
该工作从多方面证实了雄激素受体在米色脂肪细胞的负调控作用,为理解脂肪组织的性别差异提供了新的观点。
总的来说,由于全球超重、肥胖和代谢综合征发病率的持续增加,我们必须提高对白色脂肪组织,特别是内脏白色脂肪组织能量利用的认知。这项研究新发现的雄激素在PRDM16负调控中的作用,可能为开发靶向PRDM16的抗肥胖和抗代谢疾病药物提供一个良好的治疗窗口。
论文链接:
https://onlinelibrary.wiley.com/doi/10.1002/advs.202300070
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













学习学习
46