Nat Biotech:北京大学周德敏/纪德重在肿瘤个性化治疗疫苗研发领域取得突破
2023-05-27 吕 “iNature”公众号 发表于上海
与单独使用多肽相比,这种结构的疫苗接种产生了强大的树突状细胞抗原摄取,特异性免疫细胞反应和肿瘤浸润淋巴细胞的显著增加。
iNature
促进抗肿瘤免疫反应的癌症新抗原疫苗的发展在一定程度上受到新抗原递送到肿瘤的挑战的阻碍。
2023年5月25日,北京大学周德敏及纪德重共同通讯在Nature Biotechnology在线发表了题为“An engineered influenza virus to deliver antigens for lung cancer vaccination”的研究论文,该研究在黑色素瘤模型中使用模型抗原卵清蛋白(OVA),展示了一种嵌合抗原肽流感病毒(CAP-Flu)系统,用于将与甲型流感病毒(IAV)结合的抗原肽递送到肺部。该研究将减毒IAV与先天免疫刺激剂CpG结合,经鼻给药小鼠肺后,观察到肿瘤免疫细胞浸润增加。然后用点击化学将OVA共价显示在IAV-CPG上。
与单独使用多肽相比,这种结构的疫苗接种产生了强大的树突状细胞抗原摄取,特异性免疫细胞反应和肿瘤浸润淋巴细胞的显着增加。最后,该研究设计了IAV来表达抗PD- L1纳米体,进一步增强肺转移灶的消退,延长小鼠再攻击后的生存期。工程化的IAV可以与任何感兴趣的肿瘤新抗原结合以产生肺癌疫苗。

尽管发现了多种肿瘤新表位,但肿瘤特异性肿瘤免疫治疗的肿瘤抗原递送仍然具有挑战性。迄今为止,各种形式的新抗原,如基于蛋白质、多肽和核酸(mRNA/DNA)的疫苗,正在临床试验中进行评估。已经开发了许多递送新抗原的方法,包括基于树突状细胞(DC)的疫苗、病毒载体和生物材料/纳米材料辅助疫苗。然而,这些方法的成功受到诸如新表位的不良摄取和呈现以及低免疫原性等问题的限制。此外,实体肿瘤的免疫抑制环境,由肿瘤相关巨噬细胞、T调节细胞(Tregs)和髓源性抑制细胞富集,增加了免疫激活阈值,这是耐受被打破之前必须满足的。
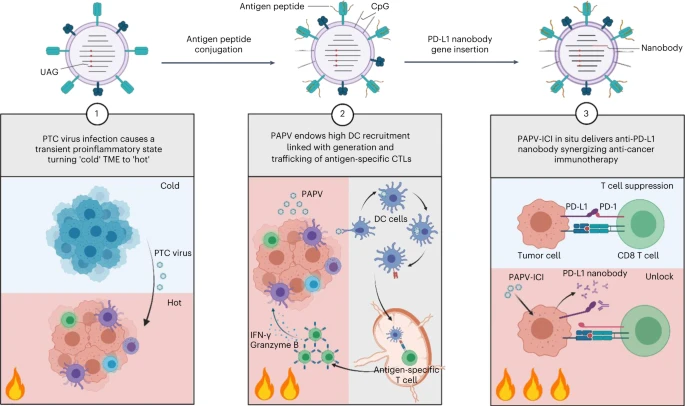
个性化肿瘤免疫治疗的PAPV-ICI平台(图源自Nature Biotechnology )
为了解决这一挑战,该研究利用了先前在甲型流感病毒(IAV)感染背景下肿瘤缓解的观察结果。然而,严重的呼吸系统并发症阻碍了IAV转化为癌症治疗。在这里,该研究报告了一种从活的但非生产性IAV中产生嵌合抗原肽流感病毒(CAP-Flu)的策略。研究结果证明了CAP-Flu将肿瘤模型抗原卵清蛋白(OVA)递送到肺部,在那里它引发强大的抗原摄取,启动先天和适应性免疫反应,并将肿瘤微环境重塑为短暂的炎症状态,从而增加肿瘤特异性细胞毒性T细胞浸润到肿瘤中。
作为一种病毒载体,CAP-Flu可以在肺肿瘤中表达抗PD - L1纳米体,进一步消除免疫抑制环境,协同增强抗癌效力。该方法为合成肽引导、肿瘤特异性和个性化免疫治疗提供了一种策略,并通过鼻内接种在黑色素瘤、结肠癌和乳腺癌肺转移小鼠模型中得到了验证。
北京大学周德敏团队助理研究员纪德重、博士研究生张缘洁为论文共同第一作者,纪德重博士和周德敏教授为论文通讯作者。北京大学药学院天然药物及仿生药物全国重点实验室为第一责任单位,深圳湾实验室和北京大学宁波海洋药物研究院为合作单位。该研究得到国家自然科学基金、国家创新药物重大专项、中国博士后科学基金、宁波市重大科技任务攻关项目、宁波市甬江引才项目的支持。
原始出处:
Ji, D., Zhang, Y., Sun, J. et al. An engineered influenza virus to deliver antigens for lung cancer vaccination. Nat Biotechnol (2023). https://doi.org/10.1038/s41587-023-01796-7.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言