EMA 收到molnupiravir的上市许可申请
2021-11-29 Allan MedSci原创
在COVID-19病例中使用molnupiravir旨在减轻医院的压力,从而降低患者出现更严重的疾病症状的风险。
在COVID-19病例中使用molnupiravir旨在减轻医院的压力,从而降低患者出现更严重的疾病症状的风险。
欧洲药品管理局 (EMA) 已开始评估 molnupiravir 的上市许可申请,molnupiravir在欧洲将以 Lagevrio 的名义销售,这是一种用于治疗成人 COVID-19 的口服抗病毒药物。
EMA 将在更短的时间内评估 Lagevrio 的安全性和有效性,如果显示 Lagevrio 的益处数据足以超过风险,则可能会在数周内就治疗发表意见。这个时间框架是可能的,因为 EMA 在滚动审查期间审查了大部分药物数据。在这次审查期间,EMA人用药品委员会 (CHMP) 评估了实验室和动物研究的数据(非临床数据)、有关药物质量和生产方式的信息,以及有关其功效和安全性。
EMA 的儿科委员会 (PDCO) 已就该公司的儿科调查计划 (PIP) 发表意见,该计划描述了应如何开发和研究该药物以用于儿童,同时与 COVID-19 产品的加速时间表相吻合。
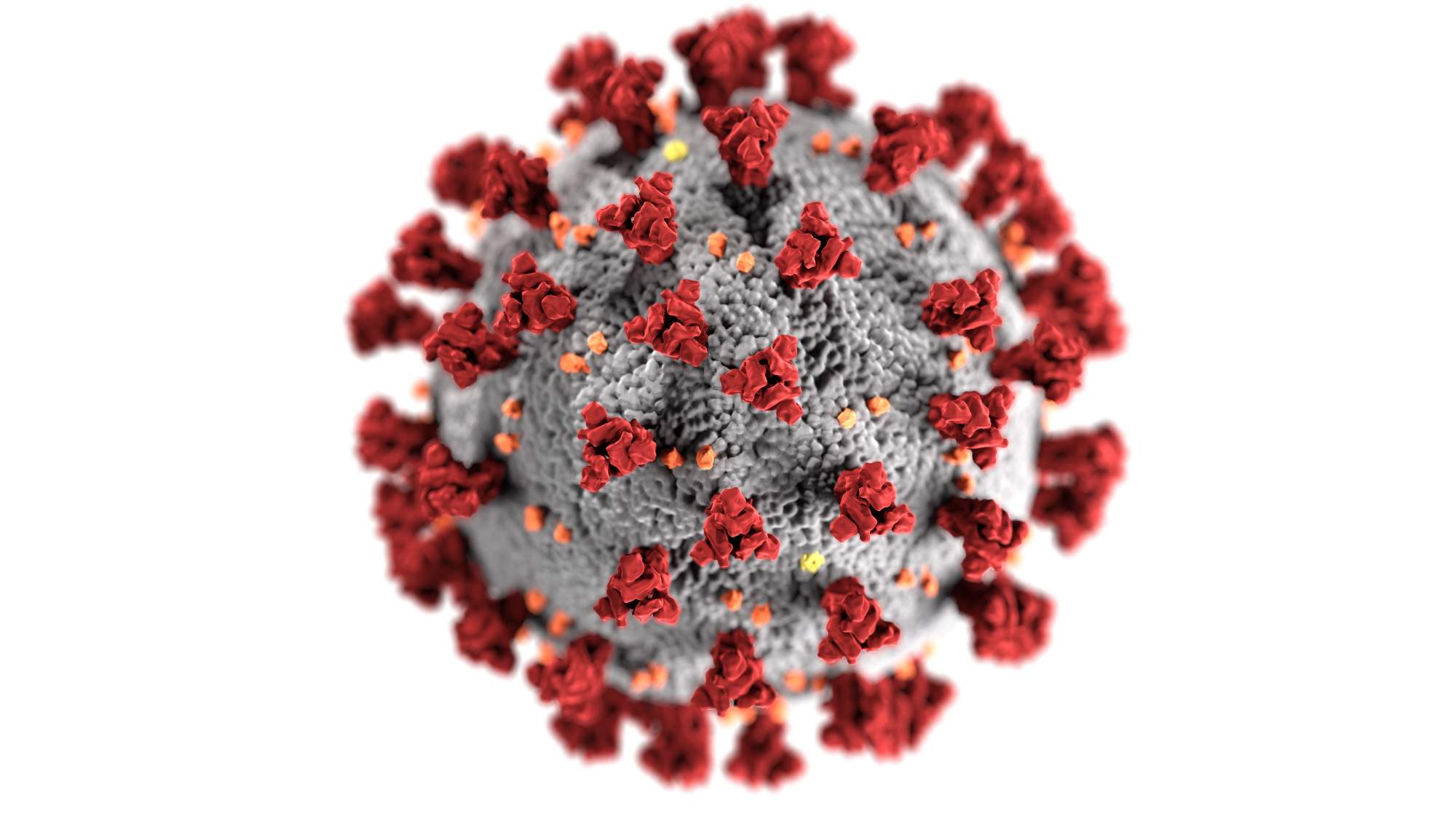
Lagevrio是一种口服抗病毒药,可降低SARS-CoV在体内繁殖的能力。该药物在复制过程中会在 SARS-CoV-2 的遗传物质(称为 RNA)中引入突变,从而削弱病毒的繁殖能力。Lagevrio 旨在通过减少住院 COVID-19 患者的数量,同时降低患者出现 COVID-19 严重症状的风险来减轻医院的负担。
如果 EMA 得出结论认为提交的数据足够可靠和完整,可以显示药物治疗 COVID-19 的有效性、安全性和质量,它将建议授予营销授权。欧盟委员会随后将加快其决策过程,以期在几天内授予在所有欧盟和欧洲经济区成员国有效的营销授权。
原始出处:
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#上市许可#
31
#EMA#
30
下载
42