山东大学陈子江/吴克良/赵涵等合作发现人类合子基因组激活始于父系基因组
2023-02-03 iNature iNature 发表于上海
尽管亲本基因组在受精后经历了广泛的表观遗传重编程以达到平衡,但它们是否在人类合子基因组激活(ZGA)中发挥不同的作用仍然未知。
尽管亲本基因组在受精后经历了广泛的表观遗传重编程以达到平衡,但它们是否在人类合子基因组激活(ZGA)中发挥不同的作用仍然未知。
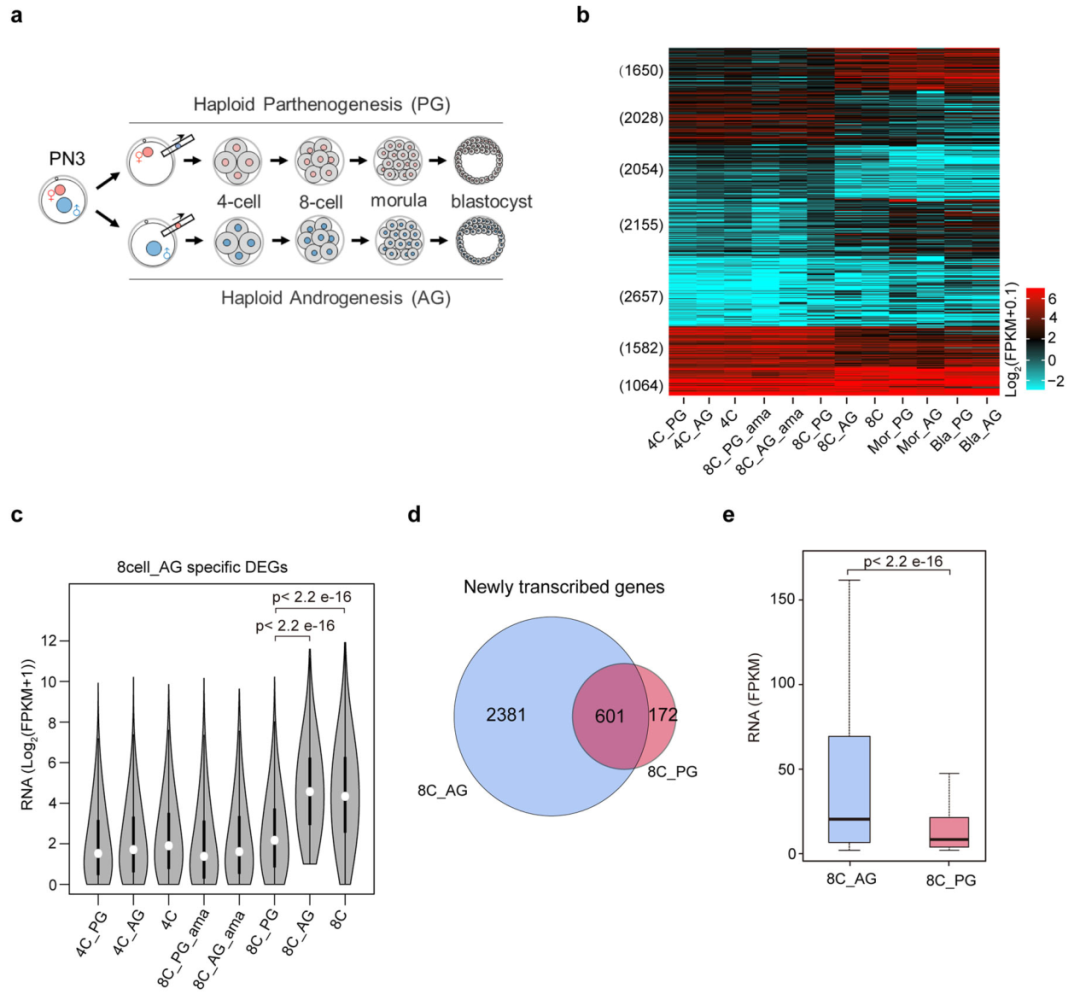
2023年1月31日,山东大学陈子江、吴克良、赵涵、中国科学院大学刘江、高磊共同通讯在Cell Discovery在线发表题为“Human zygotic genome activation is initiated from paternal genome”的研究论文,该研究表明人类合子基因组激活始于父系基因组。该研究使用人类孤雌生殖(PG)和雄激素发生(AG)胚胎在ZGA期间绘制了父母转录组。数据表明,人类ZGA在AG和双亲胚胎的8细胞阶段启动,但在PG胚胎的桑椹胚阶段启动。
相比之下,小鼠ZGA在PG和AG胚胎中发生在同一阶段。AG特异性表达的灵长类动物特异性ZNF675在8细胞期由父系基因组启动的人类ZGA中起作用。AG特异性表达的LSM1对人类母体RNA降解(MRD)和ZGA也至关重要。ZNF675和LSM1的等位基因表达与其等位基因表观遗传状态相关。值得注意的是,在二倍体胚胎中也观察到ZNF675和LSM1的父系特异性表达。总的来说,人类ZGA是从父系基因组开始的。

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







