Cytotherapy:CAR T治疗DLBCL后,外周嗜酸性粒细胞计数影响预后
2022-12-05 聊聊血液 聊聊血液 发表于上海
CAR T 细胞疗法是复发性或难治性弥漫性大 B 细胞淋巴瘤 (DLBCL) 患者的突破性治疗方法,但也有许多患者未获得缓解或缓解后复发。因此寻找 CAR T 细胞治疗中的预后生物标志物至关重要!
嗜酸性粒细胞
CAR T 细胞疗法是复发性或难治性弥漫性大 B 细胞淋巴瘤 (DLBCL) 患者的突破性治疗方法,但也有许多患者未获得缓解或缓解后复发。因此寻找 CAR T 细胞治疗中的预后生物标志物,指导患者的选择和早期干预是当下研究重点,探索重点包括乳酸脱氢酶、肿瘤负荷(总代谢性肿瘤体积)、PET/CT扫描的最大标准摄取体积和基因异常(如 TP53 突变)等。
那么临床常用指标是否同样具有预后价值?嗜酸性粒细胞参与细胞因子的抗肿瘤作用,与部分恶性肿瘤患者的结局相关,与CD8+ T细胞具有协同抗肿瘤作用。在 B 细胞非霍奇金淋巴瘤 (B-NHL) 中发现预处理化疗前外周嗜酸性粒细胞计数与 CAR T 细胞疗效相关,此外,人多能干细胞来源的嗜酸性粒细胞与 CAR T 细胞联合使用具有更好的抗肿瘤活性。上述结果推动进一步探索嗜酸性粒细胞在 CAR T 细胞治疗中的作用。
目前关于嗜酸性粒细胞抗肿瘤作用的临床研究主要关注 CAR T 细胞输注前的数据,而关于 CAR T 细胞输注后血细胞变化的研究未专门检查嗜酸性粒细胞的作用。因此李萍、梁爱斌、钱文斌教授等分析了 CAR T 细胞治疗前后 DLBCL 患者的嗜酸性粒细胞计数,发现 CAR T 细胞输注后嗜酸性粒细胞计数越高患者的结局越好。研究结果近日发表于《Cytotherapy》杂志。

研究设计
本研究纳入2019.1.1- 2021.12.31期间在同济大学附属同济医院的临床试验中,接受自体CD19 CAR T(包括鼠源和人源)、CD20 CAR T(人源)、双特异性CD19/20 CAR T(人源)细胞治疗的连续复发/难治性DLBCL患者,患者ECOG PS评分≤2、器官功能正常、有可测量疾病、预期寿命≥12周且未患有导致嗜酸性粒细胞功能障碍的其他疾病(如噬血细胞性淋巴组织细胞增生症),收集患者和治疗的基础数据以及外周血嗜酸性粒细胞计数。根据 CAR T 细胞输注时间将纳入患者分为发现队列(discovery cohort)和验证队列(validation cohort);发现队列包括2020.6.30前接受 CAR T 细胞治疗的患者,验证队列包括2020.7.1后接受 CAR T 细胞治疗的患者。
所有患者均在第-5、-4和-3天用 FC 方案(每日 25 mg/m2氟达拉滨和 300 mg/m2环磷酰胺,共3天)进行清淋化疗,然后在第0天静脉输注 CAR T 细胞。CAR T细胞的剂量水平为1-3 X 106 CAR阳性T细胞/公斤体重。
研究结果
患者
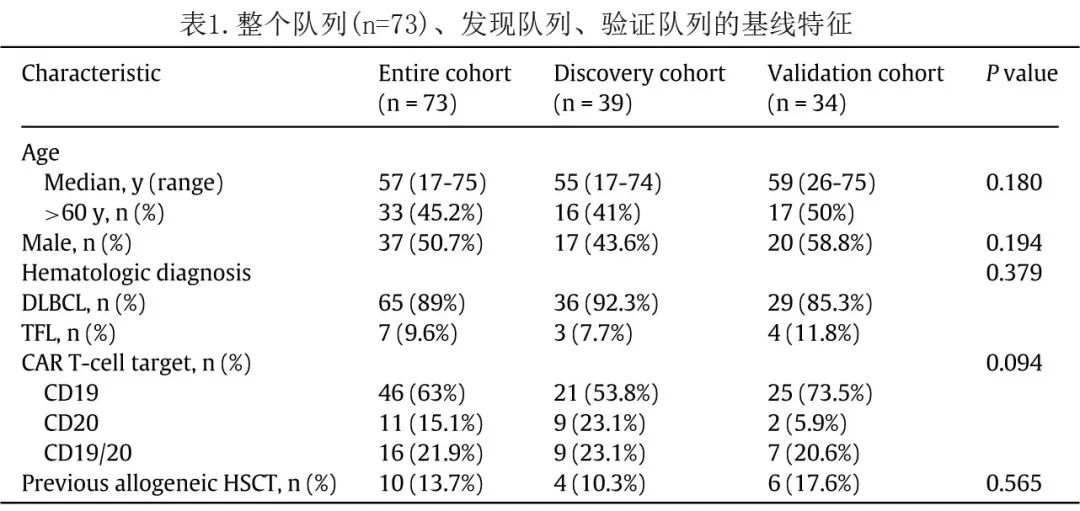
本研究共纳入73例接受 CAR T 细胞治疗的连续患者。所有患者均接受过≥2线化疗。中位年龄为57岁,37例 (50.7%) 患者为男性;65例 (89.0%) 为DLBCL,7例 (9.6%)为转化滤泡性淋巴瘤;共46例 (63.0%) 患者接受 CD19 CAR T 细胞治疗,11例 (15.1%) 患者接受 CD20 CAR T 细胞治疗,16例 (21.9%) 患者接受了CD19/20 CAR T 细胞治疗。发现队列39例,验证队列34例。所有73例患者和两个队列患者的基本特征见表1。
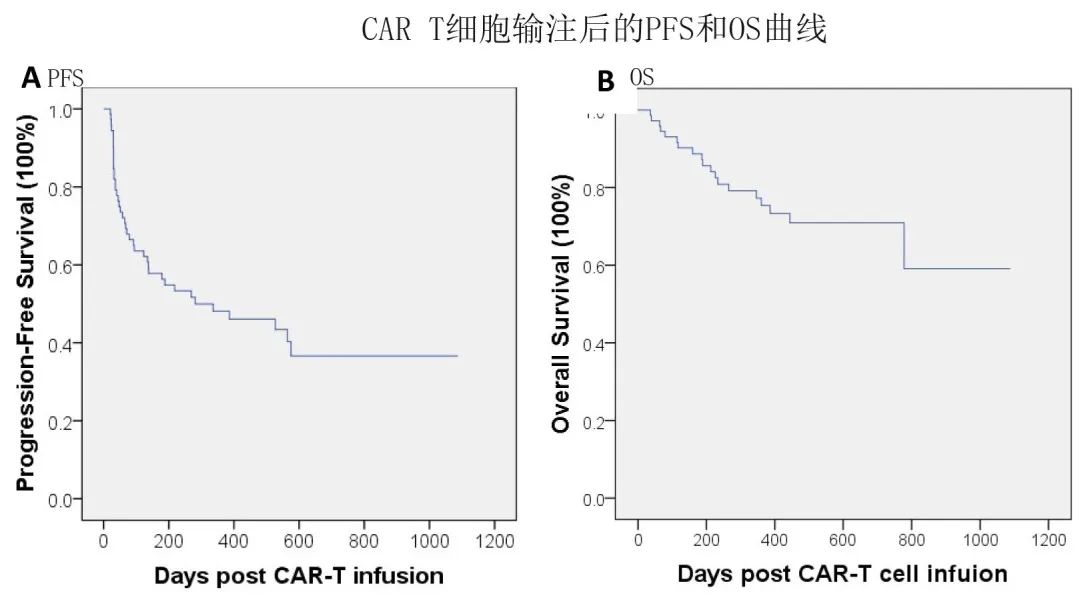
中位 PFS 为281天,41例 (56.1%) 患者在随访期间进展。
CAR T细胞输注后CR患者嗜酸性粒细胞计数高于未达CR患者
分析的数据为基线时(清淋化疗后和输注前)的外周血嗜酸性粒细胞计数和第1个月 (M1)、第2个月 (M2) 和第3个月 (M3) 期间的最大外周血嗜酸性粒细胞计数。嗜酸性粒细胞计数的正常上限为0.5*109。
CAR T 细胞输注后,发现队列的嗜酸性粒细胞计数急剧增加,最大 M1 计数(平均值0.3249*109)在统计学上大于基线(平均值0.1197*109),计数随后下降,M2的最大计数(平均值0.1637*109)低于M1。发现队列的嗜酸性粒细胞计数从基线至 M3 的变化见图1A。
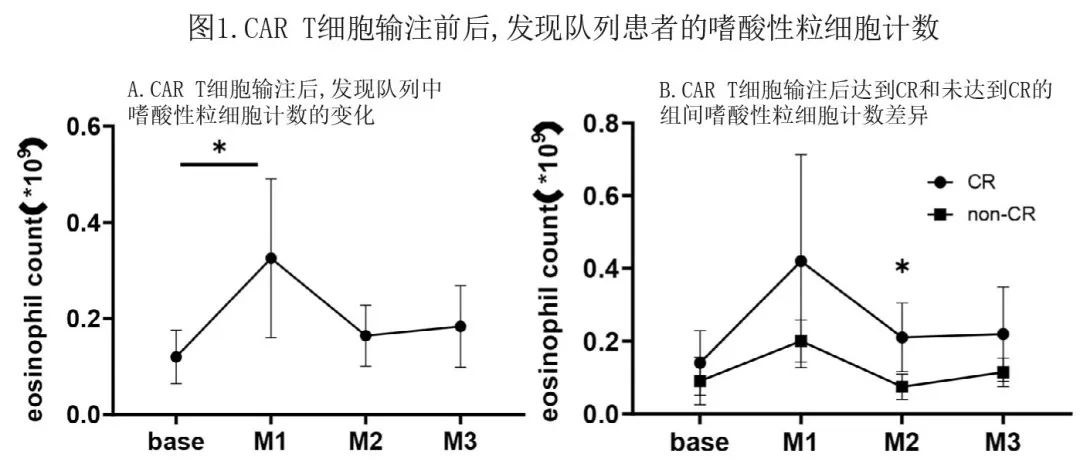
根据最佳疗效,将发现队列中的患者进一步分为 CR 组(CAR T细胞输注后达到 CR 的患者)和 nCR 组(CAR T细胞输注后未达到 CR 的患者),并比较 CR 组和 nCR 组的嗜酸性粒细胞计数。M2 期间,CR组的嗜酸性粒细胞计数统计学上高于 nCR 组(CR组为0.2175 X 109/L,nCR组为0.0742 X 109/L;P = 0.006),而两组在基线、M1或 M3 时均无统计学差异(图1B)。
作者还比较了 PD/SD 组与 PR/CR 组患者的嗜酸性粒细胞计数,发现PR/CR 组的基线嗜酸性粒细胞计数有大于 PD/SD 组的趋势,但未达到统计学显著性。
嗜酸性粒细胞计数与CAR T细胞治疗患者的预后相关
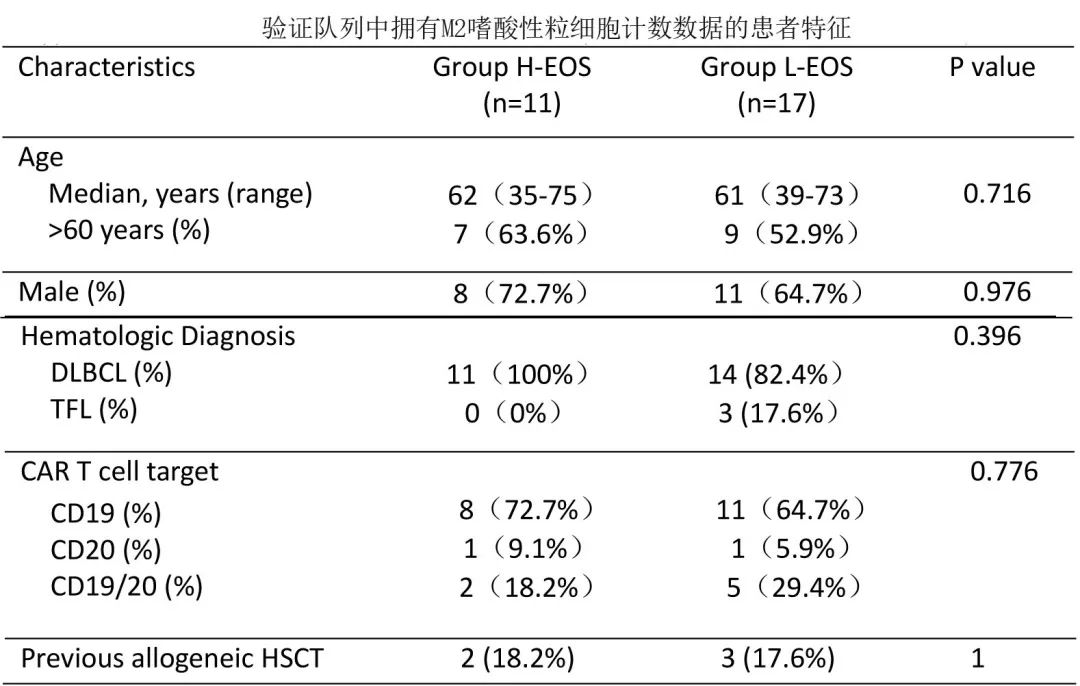
在验证队列的34例患者中,6例患者因失访或快速进展而无 M2 嗜酸性粒细胞计数的数据。基于M2 期间的最大嗜酸性粒细胞计数将验证队列患者分为 H-EOS 组和 L-EOS 组。H-EOS 和 L-EOS 之间的临界值为0.2*109/L,这是发现队列中特定时间点(基线、M1、M2和M3)嗜酸性粒细胞计数的平均值。H-EOS 组和 L-EOS 组在年龄、性别、血液学诊断和 CAR T 细胞靶点方面均无统计学差异。两组特征如下。
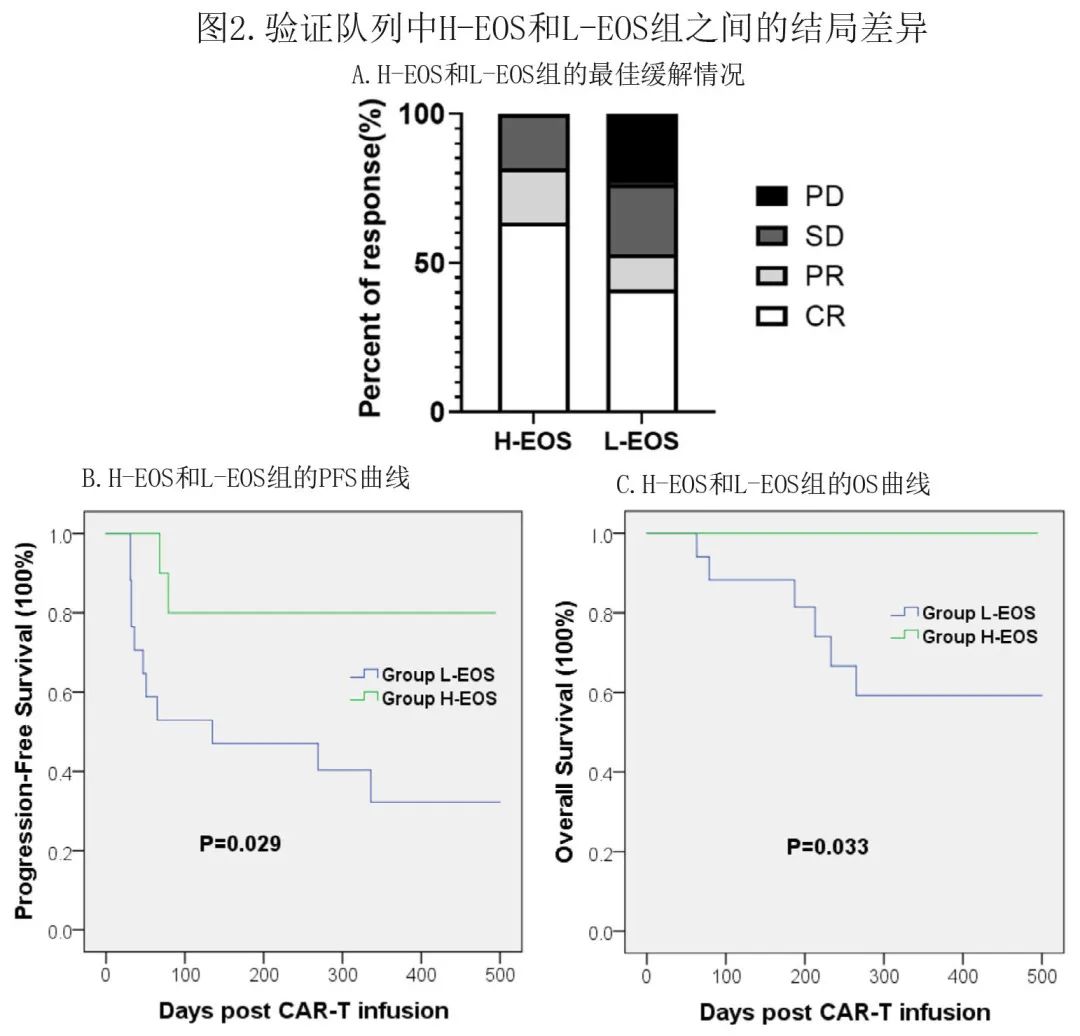
H-EOS 组 CAR T 细胞治疗后达到 CR 的患者比例高于 L-EOS 组(63.6% vs 41.2%),且H-EOS组中 CAR T 细胞输注后无患者发生PD(图2A)。基于 PFS 的 H-EOS 和 L-EOS 组的 Kaplan-Meier 曲线显示,H-EOS组的 PFS 在统计学上优于 L-EOS 组(中位PFS未达到 VS 135天,P= 0.029;图2B);基于 OS 的相同分析显示,H-EOS组的 OS 在统计学上也优于 L-EOS 组(图2C)。
嗜酸性粒细胞计数可预测CAR T治疗的6个月DOR
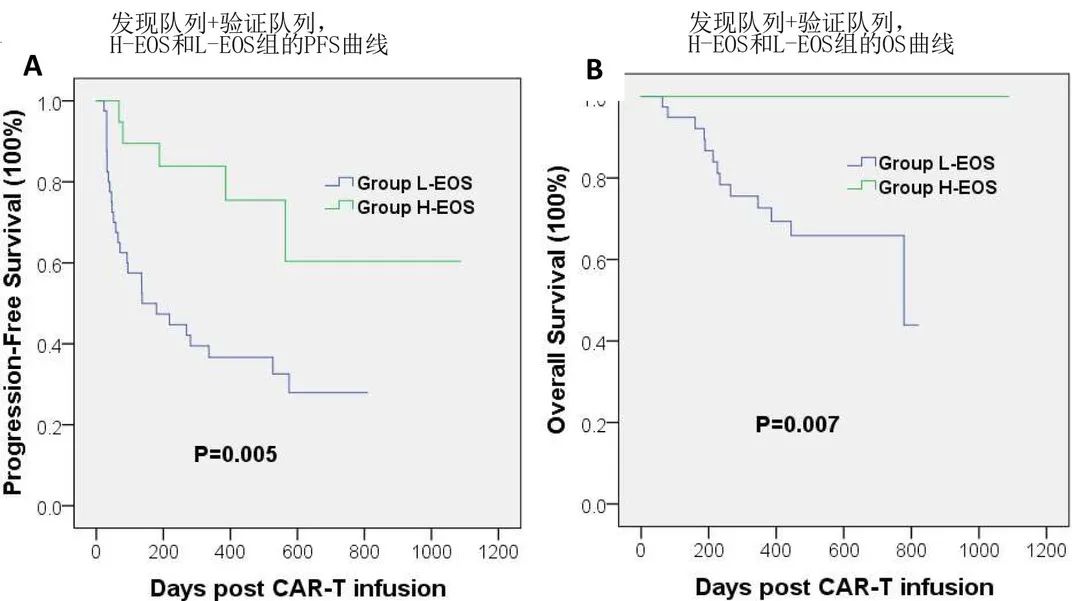
作者合并分析发现队列和验证队列中有或无高嗜酸性粒细胞组之间的 PFS 和 OS ,发现嗜酸性粒细胞计数与患者结局之间的相关性仍然存在。
作者进一步关注 CAR T 细胞治疗后达到 CR 或 PR 的患者,根据缓解持续时间将其分为两组:L-DOR(DOR为6个月的患者)和S-DOR(DOR小于6个月的患者)。L-DOR 组的 M2 嗜酸性粒细胞计数显著倾向于大于 SDOR 组,但无统计学显著性(L-DOR组为0.2409 X 109/L,S-DOR组为0.117 X 109/L;P= 0.090)。
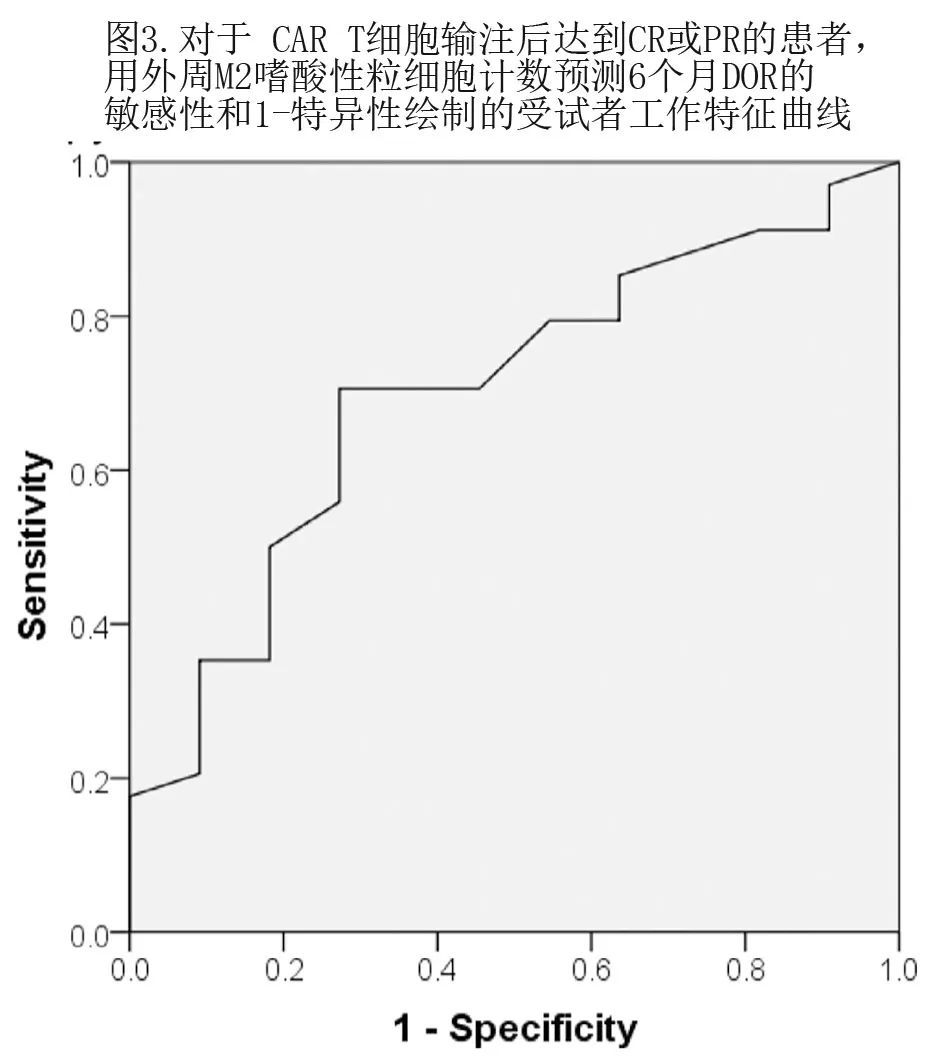
作者绘制了受试者工作特征曲线,确定 M2 的嗜酸性粒细胞计数能否预测 CAR T 细胞治疗后达到 CR 或 PR 患者的6个月DOR。曲线下面积为0.699,P值为0.049(图3)。
论
嗜酸性粒细胞计数是一种常规、廉价、简单和可重现的检测,本研究发现它与接受CAR T 细胞治疗的 DLBCL 患者的预后相关,并且可作为6个月 DOR 的预测因素,可对患者进行更全面的评估,及时调整治疗方案。但仍需更大样本的前瞻性研究进一步证明嗜酸性粒细胞与患者结局之间的关系,并确定嗜酸性粒细胞是未来细胞治疗的重要组成部分。
参考文献
Xiuyong Dan, Shiguang Ye, Lili Zhou, Yan Lu, Ping Li, Aibin Liang, Wenbin Qian. Prognostic impact of peripheral eosinophil counts in patients with diffuse large B-cell lymphoma receiving chimeric antigen receptor T-cell therapy.Cytotherapy . 2022 Nov 28;S1465-3249(22)01013-1. doi: 10.1016/j.jcyt.2022.10.010.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言