DARA皮下剂型获批
2023年5月23日,杨森公司兆珂速:registered:(通用名:达雷妥尤单抗注射液(皮下注射))正式获得中国国家药品监督管理局(NMPA)批准,用于多发性骨髓瘤全线和新诊断原发性轻链型淀粉样变性的治疗,共涵盖两大治疗领域7个适应症(NDMM:DRd、DVPM;RRMM:DRd、DVd、DPd、Dd;NDAL:DVCd)。
达雷妥尤单抗的皮下给药制剂(DARA SC,含DARA 1800mg)可通过改善给药特征减轻患者和提供者的负担。研究显示DARA SC 和 DARA IV (静脉输注给药)在疗效、总体安全性和药代动力学方面相当。此外与 DARA IV 相比,DARA SC的输液相关反应(ARR)更少,并且具有给药的其他显著获益,包括缩短给药时间(DARA SC为3-5 min,DARA IV为3-7小时)和提高患者满意度。
随着国外DARA SC的使用增加,需要更好地表征和评估该制剂在真实世界临床实践中使用的潜在优势,即患者在医院停留的时间、给药前和给药后药物的使用以及 ARR 相关事件的发生率等指标均是评估 DARA SC 潜在获益的有力手段,这些获益可能对临床实践产生影响,尤其是与资源有效利用和诊疗能力最大化相关。
梅奥诊所Scott A. Soefje教授等开展一项真实世界研究,将一种新的经验数据提取方法应用于梅奥诊所的电子健康记录 (EHR) 系统,以描述 DARA 给药特征,包括与门诊患者管理相关的的时间参数,研究结果近期发表于《JCO Oncology Practice》。

作者评估了2017年04月05日至2021年10月14日期间,梅奥诊所输液中心患者的达雷妥尤单抗 (DARA) 给药特征。将患者分组至以下队列:接受DARA IV、接受 DARA SC 、从 DARA IV 转换为 DARA SC 的患者。
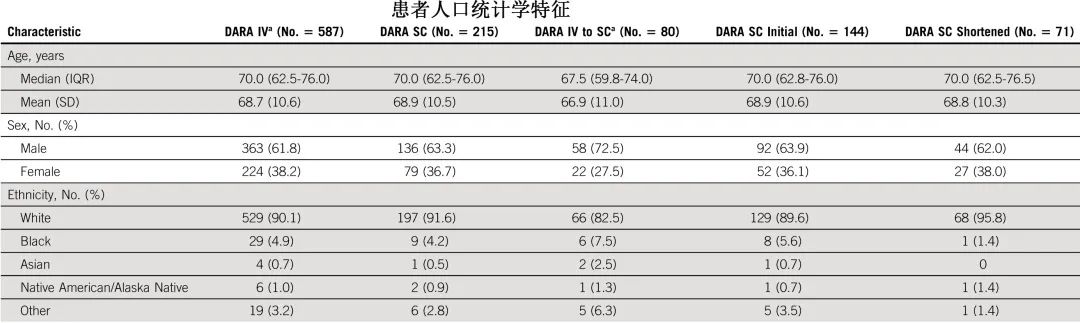
共纳入802例接受 DARA 治疗 MM 的患者(初始给药:DARA IV,n=587;DARA SC,n=215);在587例 DARA IV 患者中,80例从 DARA IV 转换为DARA SC。此外将DARA SC 队列作为两个子队列进行分析:在梅奥诊所初始 DARA SC 治疗计划下接受治疗的受试者(DARA SC intial)和在治疗计划修正后接受治疗且观察时间缩短的受试者(DARA SC shortened)。分为两个队列的原因在于,根据 DARA SC 给药的临床经验,2021年05月03日修订了 DARA SC 的治疗计划,将第1次给药的强制性给药后观察时间从4小时缩短至2小时,第2次和第3次给药的强制性给药后观察时间从1小时缩短至30 min,第4+次给药无强制性观察时间。但如果发生ARR,下一次给药的观察时间恢复至4小时。
对于所有给药,接受 DARA IV 的患者的中位总给药时间为4.8小时。接受 DARA SC 的患者,无论是初始给药还是从 IV 给药转换,所有给药组合的中位总给药时间均缩短2.7-3.0小时。在所有队列中,首次给药时的时间最多,且随着后续给药而减少,这与DARA IV 给药延长第1天给药时间和DARA SC 第1次给药时延长强制观察时间的要求相一致(下图)。此外对于所有合并剂量,DARA SC的中位总椅旁时间(chair time)比 DARA IV 短2.7-2.8小时。

DARA给药前药物的使用通常高于 DARA 给药后药物的使用。此外,DARA SC队列中接受 DARA 给药后用药的患者少于 DARA IV 队列。
DARA SC 的 ARR 相关事件发生率较低,尤其是那些通过排除药物使用所确定的事件:第1-3次给药的发生率为2%,第4次给药及之后的累积发生率为3%。
对于探索DARA SC 作为治疗 MM 患者的一种有效和方便的给药选择,本研究增加了更多的真实世界证据。通过使用 DARA SC 节省的额外时间可以释放诊所资源,如椅子、护士和其他工作人员;为患者安排提供更多灵活性;并允许医疗机构为更多患者提供治疗,不仅是接受 DARA 治疗 MM 的患者,还包括接受其他癌症治疗的患者。
更广泛地说,本研究是原理验证,使用新的经验数据提取方法分析 EHR 可以识别和量化不同临床工作流程、治疗或治疗计划改变的潜在时间优势。该方法还能够评估这种情况下的药物使用和安全性相关参数。此类分析方法可能适用于其他临床情境,以帮助优化临床资源的使用并改善患者护理。
参考文献
Scott A Soefje,et al. Clinical Administration Characteristics of Subcutaneous and Intravenous Administration of Daratumumab in Patients With Multiple Myeloma at Mayo Clinic Infusion Centers.JCO Oncol Pract . 2023 Apr;19(4):e542-e549. doi: 10.1200/OP.22.00421. Epub 2023 Feb 9.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言