马剑英:针对射血分数较低的复杂高危(CHIP)的血流动力学支持
2020-12-31 《门诊》杂志 门诊新视野
在PCI技术及相关器械不断发展的大背景下,CHIP PCI作为全新的概念诞生,其旨在针对射血分数较低的复杂高危(CHIP)患者进行有效、安全的介入治疗,最终目标在于完全血运重建。
讲者 复旦大学附属中山医院马剑英教授
在PCI技术及相关器械不断发展的大背景下,CHIP PCI作为全新的概念诞生,其旨在针对射血分数较低的复杂高危(CHIP)患者进行有效、安全的介入治疗,最终目标在于完全血运重建,并在改善患者预后方面表现出色。在此过程中,IABP、Impella、ECMO等一系列血流动力学支持装置为CHIP患者的介入治疗提供了重要保障;然而在临床实践中,血流动力学支持装置的选择方面仍存在不少尚乏定论的问题,为此,在充分认识各种血流动力学装置的特性并基于循证证据予以合理应用,是为患者带来获益的重要前提。
LVEF≤35%是CHIP的关键指标
CHIP的临床定义涉及三重意义(图1):
病变复杂且外科手术风险高,如左主干分叉、钙化、扭曲及CTO病变;
复杂的基础上患者为高危患者,伴有多种全身合并症,如糖尿病、肾功能不全、严重瓣膜病变等;
心功能严重受损或血流动力学不稳定,以LVEF≤ 35%为重要指标,且PCI过程需要血流动力学支持。
这一概念与以往的复杂冠脉病变概念有类似之处,但也存在不同。复杂的冠状动脉病变本身增加了手术风险,但并非所有复杂病变均为高危病变,因此CHIP这一概念有它的新颖和独特之处。这类患者介入治疗往往风险高,手术难度大,但患者获益也更为明显,血运重建后能有效改善患者的心功能、顽固性心绞痛,并提高患者的生活质量,甚至改善患者的长期预后。2019年,一项欧洲新发布的CHIP相关的共识中,对CHIP血流动力学方面进行了明确阐述,认为非急诊下的CHIP应以LVEF≤35%为危险分层,LVEF越低者PCI治疗耐受性更差,术后预后不良的情况更为严重。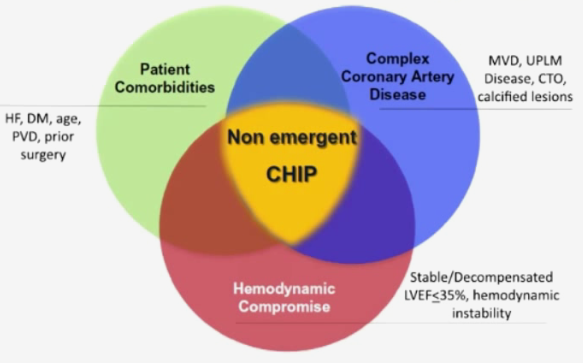
图1. CHIP的三重意义
血流动力学的支持方法
血流动力学支持对于CHIP 患者的PCI治疗而言至关重要,其方法有药物支持、呼吸机支持、全麻支持以及一系列的器械支持。药物支持是血流动力学支持的根本方法,在其基础上,对于射血分数稍低但心肌存活情况良好的患者可采用无创呼吸机,有着创伤小、临床获益优的特点;全麻支持可以避免患者术中出现不配合的情况,但需注意的是,全麻可能引起患者术后心衰以及感染的情况,综合来说全麻支持与无创呼吸机为患者带来的获益相当。
此外,血流动力学支持装置如IABP、Impella、ECMO、Tandem Heart等,可为CHIP患者的介入治疗提供更好的保障。在提升心脏输出量方面(图2),作为目前国内常用的支持手段,主动脉内球囊反搏(IABP)能减轻心脏后负荷,同时增加心脏冠脉灌注,但其提供血流动力学支持较小,达1L左右,对于部分患者单纯的IABP无法提供足够的支持。Impella可通过直接把血液从左室泵到主动脉以提供血流动力学支持,提升的心脏输出量平均约2.5L,是目前国外比较推崇的手段,但鉴于其价格昂贵,国内的使用较为受限。VA-ECMO可提升5~6L的心脏输出量,且可有效维持外周灌流;与此同时,ECMO增加心脏后负荷的副作用可被IABP、Impella抵消,因此联合应用ECMO和IABP或Impella在临床中将更为实用。
图2. 各装置所提升的心脏输出量(0~7L)
机械支持尚存的争议
然而临床实践中,如何进行血流动力学支持装置的选择以及各装置的安全性、长远疗效等方面,仍存在诸多尚未确定的问题。相关注册登记研究(图3)显示,血流动力学支持装置中应用最多的是IABP,左心室辅助装置(LVAD)等机械支持装置应用比例相对较低;由于IABP的临床疗效相关研究认为其短期疗效不理想,2005至2014年间,IABP的临床使用率逐年下降,2009年后, ECMO、Impella等临床效果更佳的器械被采用得更多。
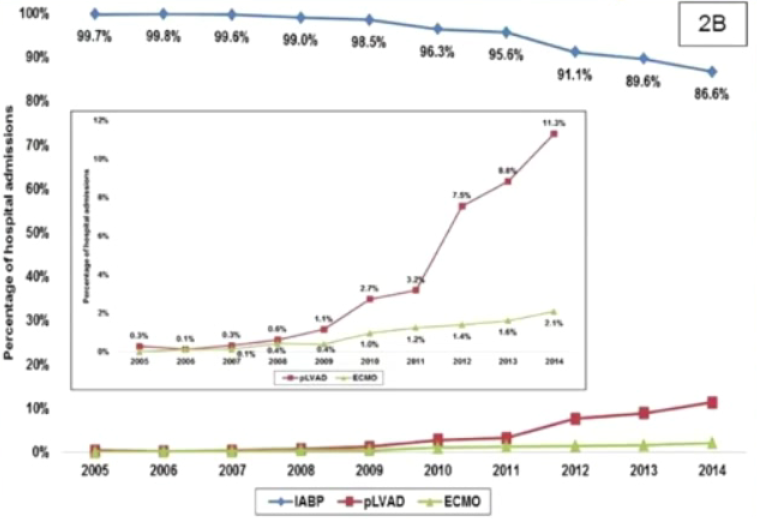
图3.2005~2014年间各器械的临床使用率
但从长远疗效来看,一项关于高风险PCI中应用IABP的疗效研究显示(图4),在LVEF<30%的严重冠脉病变患者中,在良好选择下有使用IABP,分别在术后前6个月、术后1年内乃至术后1年以上,皆表现出患者的良好获益。这亦提示,单从术后30天的短期疗效否定IABP的最终临床获益存在不合理性。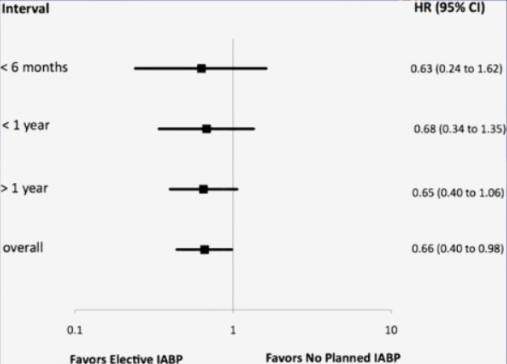
图4. IABP应用于高风险PCI的疗效观察
有研究显示,与IABP相比,新型血流动力学支持装置Impella可提供更好的血流动力学支持效果:更好地改善患者血流动力学,有助于实现更完全的血运重建,且低血压事件风险更低。此外,亦有研究提示该装置具有良好的肾脏保护、终末器官保护作用和成本效益,认为Impella是CHIP患者冠脉介入治疗血流动力学支持的更好选择。但这个理论并未受到学术界的一致认同,2017年发布的一项小规模的随机对照研究(图5)结果显示,IABP或Impella为患者带来的临床获益相当,术后死亡率亦接近。

图5. IABP vs LVAD小样本随机对照研究
那么,尽管Impella的临床效果备受认可,是何种原因导致IABP与左心室辅助装置两者间最终获益如此相近?从改善血流动力学相关指标的效果看,IABP与左心室辅助装置似乎各有优势。其中,左心室辅助装置改善心指数及平均动脉压的作用更具优势,而IABP改善肺毛细血管楔压的作用更显著;安全性方面,两者的死亡率以及下肢缺血、发热或脓血症等并发症风险无差异,而应用LVAD的出血风险似乎更高。今年发布的一项关于心源性休克患者中应用IABP及LVAD的研究发现,院内大出血事件方面,应用Impella的患者出血风险可达31.3%,而应用IABP者为16.0%;全因死亡率方面,应用Impella的患者(45.0%)显著高于应用IABP患者(34.1%)。这一定程度上揭示了Impella与IABP两者最终获益相近的原因,同时也提示了临床中应用Impella时,应密切关注患者的出血风险。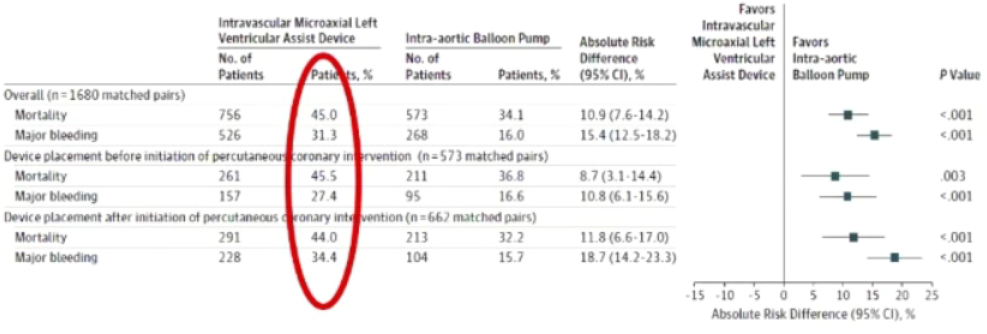
图6.心源性休克患者中应用 IABP vs LVAD的出血与死亡率
除此之外, ECMO装置亦是临床推崇之选,近年ECMO的相关循证研究及其在临床应用中展现的优良效果,均肯定其确实可改善患者总体的生存率。VA-ECMO可提升5~6L的心脏输出量,提供充足血流动力学支持下有效维持了外周灌流,但研究发现ECMO增加心脏后负荷的副作用明显,而IABP能够减轻心脏后负荷,同时增加心脏冠脉灌注,ECMO的副作用可被IABP抵消,因此两者的联合应用将是未来临床的推荐选择。
总 结
CHIP PCI作为介入技术的进阶领域,发展前景令人期待,而我国CHIP患者群体庞大,CHIP PCI仍处于初期摸索阶段。临床中,CHIP PCI的血流动力学支持方面至关重要,各类器械支持方式为患者带来的临床净获益却仍未有定数,由于IABP、Impella、ECMO等装置的作用机制各不相同,未来可考虑多器械相互联用以提高CHIP患者在血流动力学支持下的综合获益。需强调的是, CHIP PCI的血流动力学支持因人而异,在术前进行准确的评估并合理的选择支持方法,方能为患者谋求更好的预后。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#血流动力#
0
#血流动力学#
42
好文章!
74
认真学习了
84