赛诺菲和再生元的抗PD-1药物Libtayo显著提高肺癌患者的存活率
2020-04-27 Allan MedSci原创
赛诺菲和再生元制药公司(Regeneron Pharmaceuticals)披露称,在一项抗PD-1药物Libtayo(cemiplimab)一线治疗局部晚期或转移性非小细胞肺癌(NSCLC)。
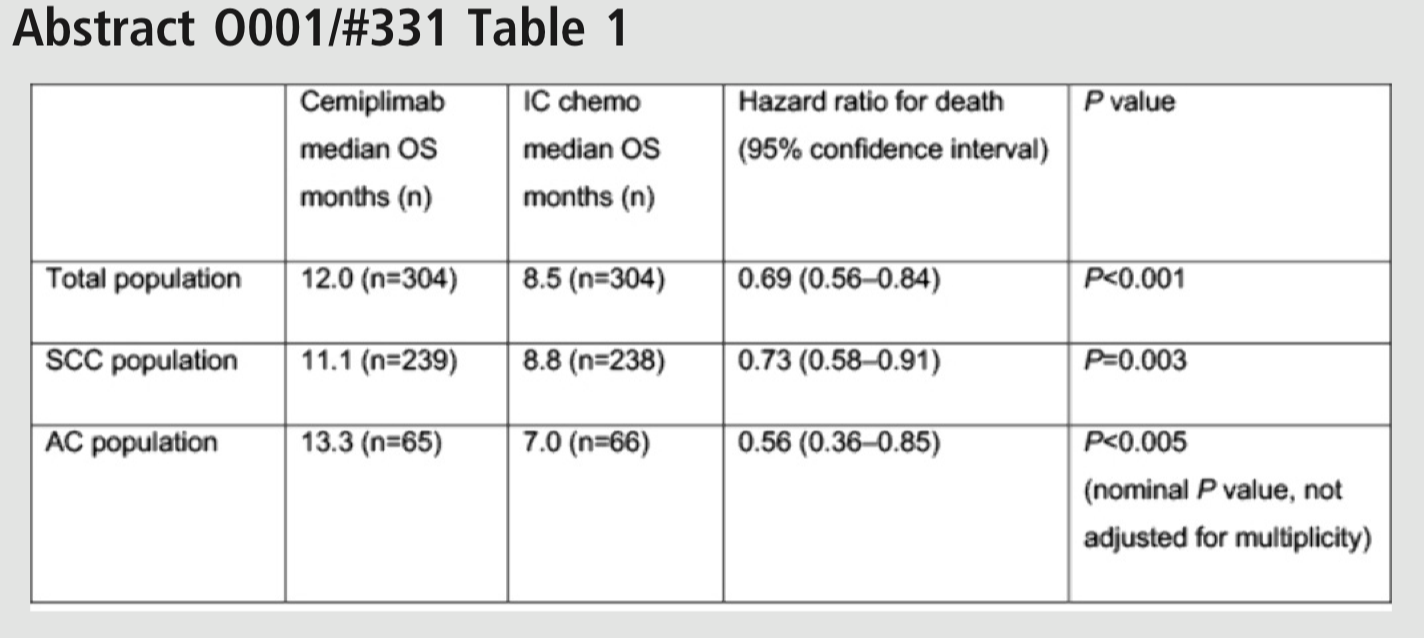
赛诺菲和再生元制药公司(Regeneron Pharmaceuticals)披露称,在一项抗PD-1药物Libtayo(cemiplimab)一线治疗局部晚期或转移性非小细胞肺癌(NSCLC)的III期临床研究中,患者的存活率的显著提高。根据独立数据监测委员会的建议,该研究应尽早停止,且该研究将进行修改,以允许所有患者接受Libtayo治疗。
根据这项分析,接受Libtayo单药治疗的患者的总生存期显著增加。与铂类双药化疗相比,Libtayo单药治疗将死亡风险降低了32.4%。
PD-1是一种重要的免疫抑制分子,通过向下调节免疫系统对人体细胞的反应,以及通过抑制T细胞炎症活动来调节免疫系统并促进自身耐受。这可以预防自身免疫性疾病,但它也可以防止免疫系统杀死癌细胞。
原始出处:
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#肺癌患者#
33
#存活率#
45
#Libtayo#
35