Cell Commun Signal:FKBP12是多发性骨髓瘤细胞ALK2活性的主要调节因子
2023-02-02 将军的九分裤 MedSci原创 发表于上海
这项研究的数据表明FKBP12是多发性骨髓瘤细胞中ALK2活性的主要调节因子,部分原因是将NSC转化为活性信号传导复合物。
 免疫亲蛋白FKBP12与TGF-β家族I型受体结合,包括BMP I型受体ALK2。FKBP12使I型受体保持非活性状态并控制信号传导活性。用FKBP-配体FK12等药物去除FKBP506可增强各种细胞类型的BMP活性。在多发性骨髓瘤细胞中,SMAD1/5/8的活化导致细胞凋亡。一研究团队假设从骨髓瘤细胞的ALK2中去除FKBP12会增强BMP诱导的ALK2-SMAD1/5/8活性,从而导致细胞死亡。
免疫亲蛋白FKBP12与TGF-β家族I型受体结合,包括BMP I型受体ALK2。FKBP12使I型受体保持非活性状态并控制信号传导活性。用FKBP-配体FK12等药物去除FKBP506可增强各种细胞类型的BMP活性。在多发性骨髓瘤细胞中,SMAD1/5/8的活化导致细胞凋亡。一研究团队假设从骨髓瘤细胞的ALK2中去除FKBP12会增强BMP诱导的ALK2-SMAD1/5/8活性,从而导致细胞死亡。
在分析SMAD1/5/8活性和细胞活力之前,用FK506或其他FKBP结合化合物结合不同的BMP处理多发性骨髓瘤细胞系。SMAD1/5/8活性也使用报告细胞系INA-6 BRE-luc进行了研究。为了表征功能信号受体复合物,他们通过siRNA、shRNA和CRISPR/Cas9技术对受体表达进行了基因调控。

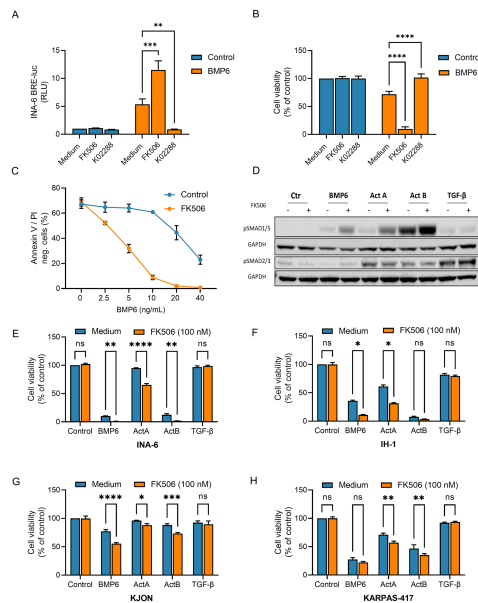
图1 FK506增强多发性骨髓瘤细胞中SMAD1/5/8的激活和凋亡。
FK506在多发性骨髓瘤细胞系中增强BMP诱导的SMAD1 / 5 / 8活化和凋亡。通过使用具有不同亲和力谱的FKBP结合化合物和靶向FKBP12的siRNA,研究表明FK506效应是通过与FKBP12结合介导的。通常通过骨髓瘤细胞中的ALK3发出信号的配体BMP2,BMP4和BMP10不会在缺乏ALK3的细胞中诱导细胞凋亡。值得注意的是,BMP10与BMP6和BMP9竞争,并通过ALK2拮抗它们的活性。然而,在添加FK506后,研究人员看到了特异性的惊人变化,因为ALK3配体获得了通过ALK2发出信号并诱导细胞凋亡的能力。这表明受体复合物可以通过添加FK506从无活性的非信号复合物(NSC)切换到活性复合物。这种活性的增加也出现在其他类型的细胞中,这表明所观察到的影响具有更广泛的相关性。BMP2, BMP4和BMP10依赖于BMPR2作为II型受体来发出信号,这与BMP6和BMP9形成对比,当BMPR2被敲除时,BMP6和BMP9更有效地激活ALK2。

图2 FK506通过FKBP12增强SMAD1/5/8激活
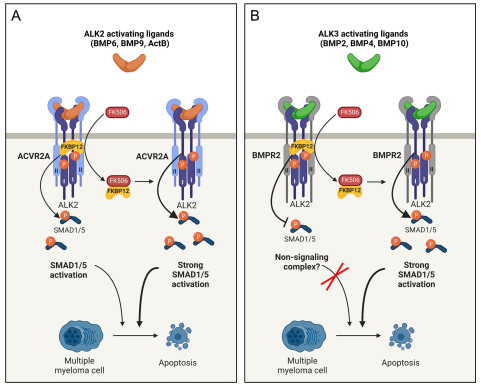
图3:多发性骨髓瘤细胞中配体依赖ALK2活性的调控。
总的来说,这项研究的数据表明FKBP12是多发性骨髓瘤细胞中ALK2活性的主要调节因子,部分原因是将NSC转化为活性信号传导复合物。靶向缺乏免疫抑制活性的化合物FKBP12可能在旨在减少多发性骨髓瘤肿瘤负荷的新治疗策略中具有潜力。
原始出处:
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言















靶向缺乏免疫抑制活性的化合物FKBP12可能在旨在减少多发性骨髓瘤肿瘤负荷的新治疗策略中具有潜力
43