Cell Reports︱浙江大学蔡志坚/王建莉揭示干扰素信号反馈调节抗病毒免疫应答新机制
2023-01-27 iNature iNature 发表于陕西省
病毒感染是一个严重危害人类健康和生命的全球性问题,因其所致传染性疾病多种多样,同时伴随着较高的发病率和死亡率,因此极大地威胁着人类的健康和生命。
病毒感染是一个严重危害人类健康和生命的全球性问题,因其所致传染性疾病多种多样,同时伴随着较高的发病率和死亡率,因此极大地威胁着人类的健康和生命。
I型干扰素(IFN-I)信号是机体抗病毒天然免疫应答的核心。病毒感染发生时,模式识别受体(PRRs)通过检测识别病毒核酸和蛋白成分,迅速启动下游抗病毒免疫反应,激活IFN-I信号并诱导干扰素刺激基因(ISGs)表达,发挥抗病毒效应,保护机体抵抗病毒入侵。抗病毒免疫应答受到机体的精准调控,但IFN-I信号通路如何调节抗病毒天然免疫应答,目前很大程度上依然未知。
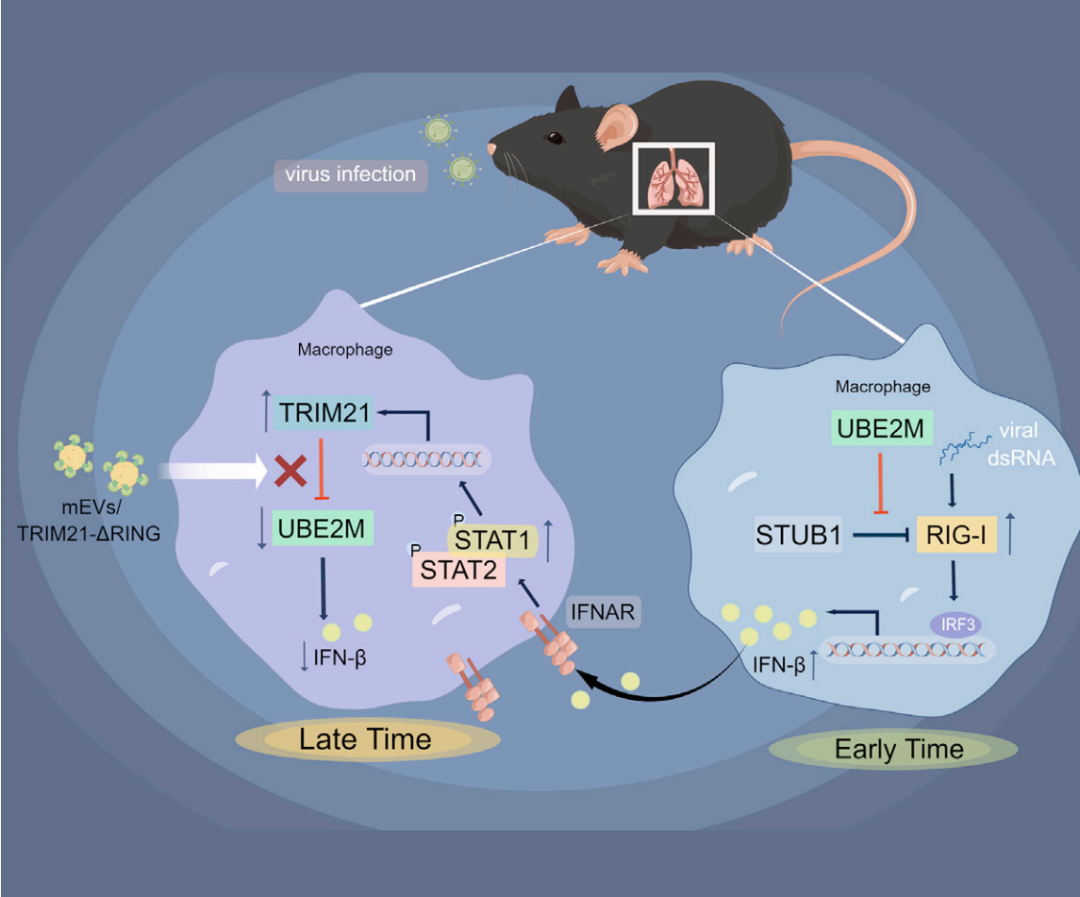
2023年1月21号,浙江大学基础医学院免疫学研究所蔡志坚/王建莉课题组在Cell Reports 在线发表题为“Type I interferon/STAT1 signaling regulates UBE2M-mediated antiviral innate immunity in a negative feedback manner”的研究论文,该研究阐明了巨噬细胞的UBE2M在激活机体抗病毒感染过程中的重要作用,揭示了一条IFN信号通过抑制UBE2M水平,负反馈调节抗病毒免疫应答的新机制,并开发了一款以牛奶来源的胞外囊泡为递送载体,通过口服便可提高机体抗病毒免疫的新制剂。

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







