Sci Trans Med:攻克“癌症之王”,科学家们找到了新方法,小鼠100%存活 !
2019-07-06 学术经纬 药明康德
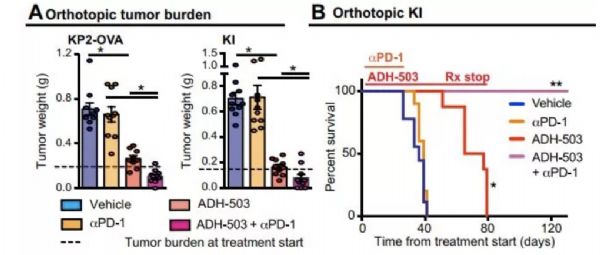
日前,《科学》子刊Science Translational Medicine上,发表了一篇治疗胰腺癌的研究论文,并吸引了不少报道。研究人员们发现,一种小分子药物能够促进免疫反应,有效攻击肿瘤。在小鼠实验中,它能有效减少胰腺癌的肿瘤生长与转移。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#TRA#
30
#新方法#
29
#Med#
32