Science Signaling:王晓东实验室揭示高渗应激诱导程序性细胞坏死的分子机制
2022-05-23 北京生命科学研究所 北京生命科学研究所
该研究揭示了高渗应激诱导的细胞坏死分子机制,发现了细胞坏死关键蛋白RIPK3新的激活机制,拓宽了对细胞坏死信号通路的认识。
水是生命之源,组成生物体的细胞都生活在液态水环境中。细胞内部由疏水的细胞膜和外界隔开。细胞内外离子和其他如葡萄糖等小分子对细胞内外的水分子保持着等同的渗透压,从而使水分子不会单项流动造成细胞损伤。细胞内和血浆中渗透压于0.9%的氯化钠相当,故被称为生理盐水。当细胞外液渗透压过高(高渗应激)或过低(低渗应激)时,细胞会失水或涨水,都会对细胞造成损害。在正常情况下,除少数专门处理水盐平衡的细胞外(肾髓质),人体内细胞生长所处液态环境的渗透压被严格限定在285-300 mOsm/kg之间(1);在疾病或应激状态下,可能会出现因水电解质紊乱而导致的渗透压变化,如果纠正不及时则会引起严重后果。之前的研究表明,在高渗应激下,即细胞内液渗透压低于细胞外液渗透压,会导致细胞内水分流失,细胞骨架改变以及细胞皱缩,细胞内离子和生物大分子因浓度升高而积聚,DNA发生断裂,细胞正常的信号转导受到影响。于此同时,处于高渗环境的细胞也会启动包括激活离子转运蛋白在内的一系列适应性反应,可是一旦高渗应激超过细胞适应阈值,细胞将会不可避免的走向死亡(2-3)。尽管人们早就观察到这一现象,但其中的分子机制尚不清楚。
长期以来,王晓东实验室深耕于包括程序性细胞凋亡(apoptosis)和程序性细胞坏死(necroptosis)在内的程序性细胞死亡信号通路的研究,先后发现了细胞坏死的关键调控蛋白RIPK3(4)和MLKL(5)。2022年5月17日,王晓东实验室在Science Signaling杂志上发表了题为“Osmotic stress activates RIPK3/MLKL-mediated necroptosis by increasing cytosolic pH through a plasma membrane Na+/H+ exchanger”的研究成果,揭示了高渗应激诱导细胞死亡的分子机制—高渗应激通过诱发RIPK3介导的程序性细胞坏死导致细胞死亡。

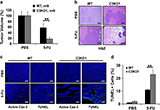
在这项研究中,研究人员发现当细胞处于高浓度的NaCl或Sucrose制造的高渗应激环境中时,除观察到细胞死亡之外还可以检测到RIPK3以及RIPK3依赖的MLKL的磷酸化信号,而敲除RIPK3或MLKL基因均可以阻断上述生化反应和细胞死亡,这表明高渗应激会诱导RIPK3介导的程序性细胞坏死的发生。出乎意料的是,RIPK3的激活并不依赖于其已知的上游蛋白RIPK1、DAI或TRIF,此外,针对RIPK3结构功能实验也证明了高渗应激诱导的RIPK3激活仅需要其激酶结构域而并不依赖RHIM(RIP homotypic interaction motif)结构域,这表明高渗应激诱导的RIPK3激活与所有已知的程序性细胞坏死信号通路均不相同,并不需要通过RHIM结构域与上游蛋白直接发生相互作用。
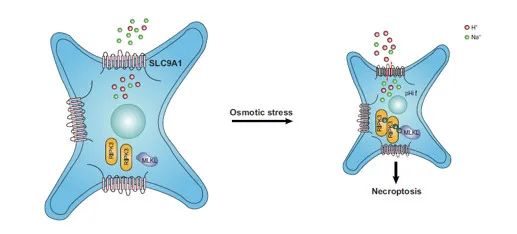
为了进一步找到高渗应激诱导RIPK3激活的上游关键分子,研究人员采用CRISPR/Cas9全基因组筛选的方法,发现并证明了Na+/H+转运体SLC9A1参与了高渗应激诱导的细胞坏死信号通路。进一步的细胞和生化实验证明了高渗应激通过激活SLC9A1导致细胞内pH升高,而细胞内环境的碱化可以直接激活RIPK3进而诱导细胞坏死的发生(下图)。
总的来说,该研究揭示了高渗应激诱导的细胞坏死分子机制,发现了细胞坏死关键蛋白RIPK3新的激活机制,拓宽了对细胞坏死信号通路的认识。
本文的第一作者是王晓东实验室的博士研究生张文彬,其他作者包括王晓东实验室樊炜亮博士和郭佳博士。王晓东博士为本文的通讯作者。该课题的研究经费来自中国科技部、国家自然科学基金和北京市科学技术委员会。
参考文献:
1. Noda, M. & Sakuta, H. Central regulation of body-fluid homeostasis. Trends in Neurosciences 36, 661–673 (2013).
2. Burg, M. B., Ferraris, J. D. & Dmitrieva, N. I. Cellular response to hyperosmotic stresses. Physiological reviews 87, 1441–1474 (2007).
3. Stöhr, D. & Rehm, M. Linking hyperosmotic stress and apoptotic sensitivity. The FEBS journal 288, 1800–1803 (2021).
4. He, S. et al. Receptor interacting protein kinase-3 determines cellular necrotic response to TNF-alpha. Cell 137, 1100–1111 (2009).
5. Sun, L. et al. Mixed lineage kinase domain-like protein mediates necrosis signaling downstream of RIP3 kinase. Cell 148, 213–227 (2012).
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#signaling#
41
#Sign#
40
#Signal#
31
#坏死#
45
#SCIE#
32
#应激#
38