blood:CAR T作为LBCL二线治疗的TRANSFORM研究主要分析结果
2023-01-18 聊聊血液 聊聊血液 发表于安徽省
在原发难治性或早期复发性 LBCL 患者中,与化疗敏感患者接受含铂免疫化疗后接受大剂量化疗和 ASCT 的标准治疗相比,liso-cel作为二线治疗具有优效性,并且具有良好的安全性特征。
去年12月,新英格兰医学杂志先后发表了axicabtagene ciloleucel (axi-cel)和tisagenlecleucel (tisa-cel)在二线LBCL中对比ASCT的ZUMA-7和BELINDA研究详细结果,而Lisocabtagene maraleucel(liso-cel)的TRANSFORM研究中期分析结果今年6月才在《Lancet》正式发表,彼时中位随访6.2个月,证实对于一线治疗原发难治或12个月内复发的大B细胞淋巴瘤(LBCL),liso-cel较标准治疗(SOC)在无事件生存期(较SOC增加近4倍)、完全缓解率(增加27%)和无进展生存期(增加2.5倍)方面均表现出优效性,同时安全性可控,但OS结果尚不成熟。
近日《blood》报道了TRANSFORM研究的随访17.5个月主要分析结果,进一步证实了liso-cel较SOC在PFS、CR率和EFS的优势,中位OS分别为未达到和29.9个月,18个月OS率分别为73.1%和60.6%。现整理如下。
 研究设计
研究设计
TRANSFORM研究是一项在美国、欧洲和日本47家医疗癌症中心的复发/难治性LBCL成人患者中进行的关键、全球、随机、开放标签、3期研究,目的是比较liso-cel与二线标准治疗(SOC)的疗效和安全性。
研究纳入患者:年龄18-75岁、符合ASCT条件、难治性LBCL或一线治疗(包括蒽环类药物和CD20单抗)后12个月内复发、ECOG PS≤1、器官功能良好、随机化前根据Lugano 2014版标准判定的PET阳性疾病;允许患有继发性中枢神经系统淋巴瘤入组。主要排除标准包括:既往接受过基因或CD19靶向治疗,有活动性感染。
患者1:1随机进入liso-cel组或SOC组。liso-cel组的患者在氟达拉滨/环磷酰胺清淋化疗后3天,连续两次静脉输注CD8+ 和CD4+细胞,目标剂量为100×106 CAR-T细胞,允许使用SOC化疗方案进行桥接治疗。SOC组患者接受3个疗程的R-DHAP、R-ICE或R-GDP(如果出现毒性或疗效不满意,研究者可以在方案规定的三种挽救方案中进行一次转换),然后CR或PR患者进行BEAM+ASCT。
允许SOC组接受liso-cel作为三线治疗:免疫化疗3个周期后未达到CR或PR,任何时间疾病进展,或由于随机化后18周后无CR而需要开始新的抗肿瘤治疗。这些患者被称为交叉亚组,不视为liso-cel组的一部分。
主要研究终点为EFS(IRC依照2014版LUGANO标准),次要终点包括CR率、PFS和OS。
研究结果
患者
本次分析的中位随访时间为17.5个月。共有184例患者接受随机分组,每组92例。SOC 组91例患者接受了二线免疫化疗(1例撤回知情同意),43例患者 (47%) 接受了大剂量化疗和ASCT,61例患者 (66%) 被批准交叉接受liso-cel,其中58例患者 (63%) 接受了输注(57例患者接受liso-cel,1例患者接受了不合格产品)。liso-cel 组89例接受了 liso-cel 输注(1例撤回知情同意,1例生产失败,1例接受了不合格的 CAR T 细胞产品);58例 (63%) 患者接受了桥接治疗。根据研究者评估,接受桥接治疗的最常见原因是高肿瘤负荷 (28/58 [48%]) 和快速进展 (23/58 [40%])。19例患者 (21%) 在门诊接受了liso-cel。
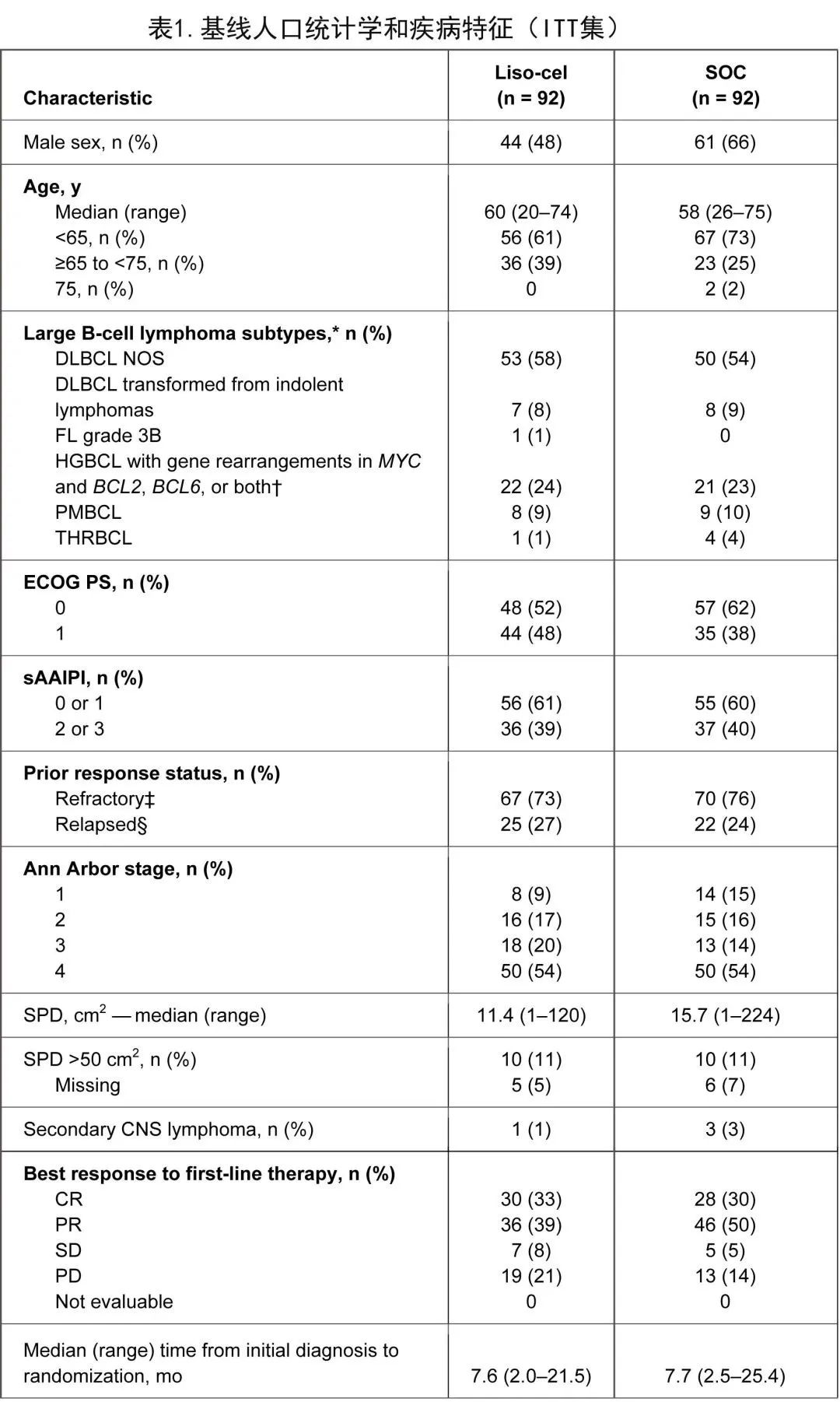
两组之间的基线特征基本平衡。总体而言,33%的患者年龄≥65岁,64%为弥漫大B细胞淋巴瘤(55%为NOS,8%由惰性淋巴瘤转化而来),23%为高级别 B 细胞淋巴瘤(双/三打击),73%在一线治疗后患有难治性疾病,27%在一线治疗后12个月内疾病复发(表1)。
 疗效
疗效
liso-cel中位EFS未达到(NR),SOC为2.4个月(HR= 0.356;图1A)。liso-cel 组18个月 EFS 率为52.6%,SOC组为20.8%。此外在亚组分析中,在所有预先规定的亚组中EFS均有利于liso-cel。
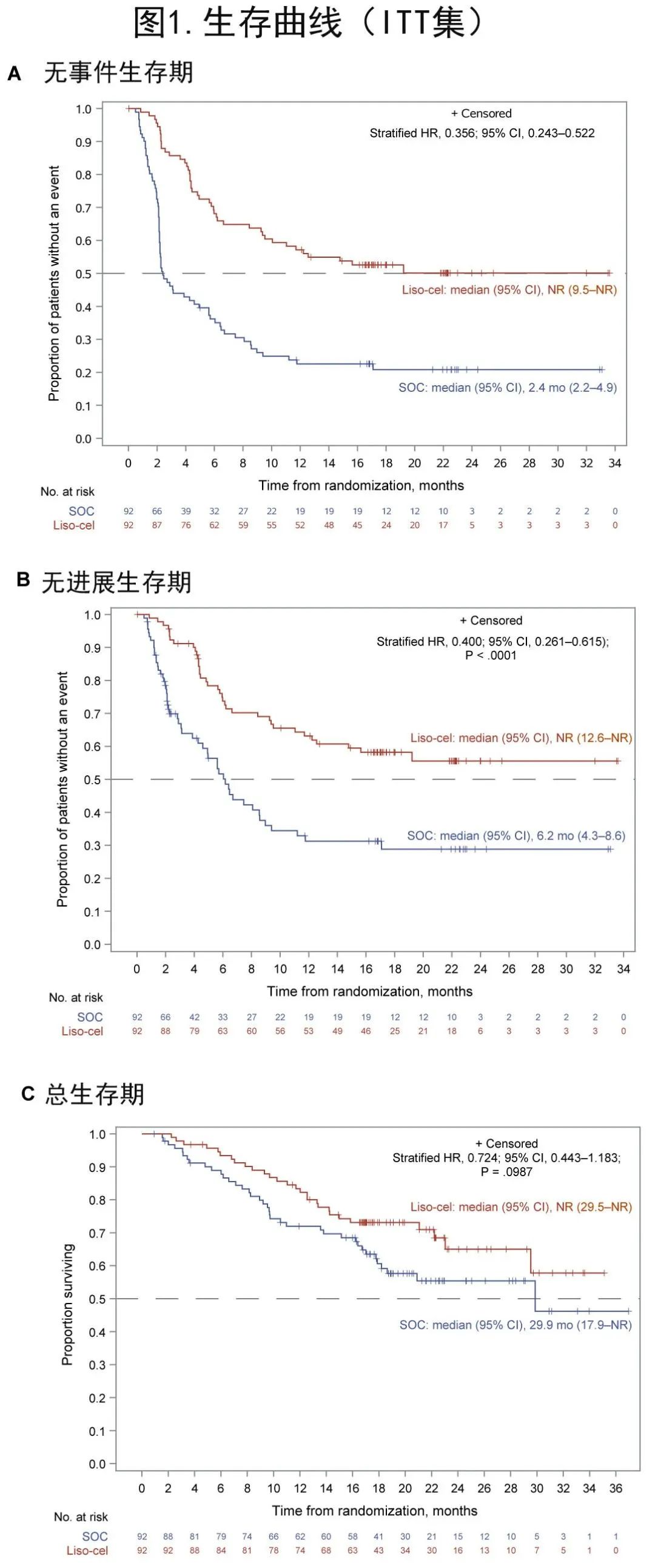 本研究也达到了关键次要终点 CR 率和PFS,证明了 lisocel 相对于 SOC 的优效性。liso-cel 组的 CR 率为74%,SOC组为43%(P< 0.0001),中期分析时最佳总体缓解为 PR 的26例患者中9例患者在主要分析时缓解加深至CR(liso-cel组6/18例患者;SOC组3/8例患者)。liso-cel 组的中位 PFS 为NR,SOC组为6.2个月(HR= 0.400;P< 0.0001;表2和图1B),18个月 PFS 率分别为58.2%和28.8%。
本研究也达到了关键次要终点 CR 率和PFS,证明了 lisocel 相对于 SOC 的优效性。liso-cel 组的 CR 率为74%,SOC组为43%(P< 0.0001),中期分析时最佳总体缓解为 PR 的26例患者中9例患者在主要分析时缓解加深至CR(liso-cel组6/18例患者;SOC组3/8例患者)。liso-cel 组的中位 PFS 为NR,SOC组为6.2个月(HR= 0.400;P< 0.0001;表2和图1B),18个月 PFS 率分别为58.2%和28.8%。
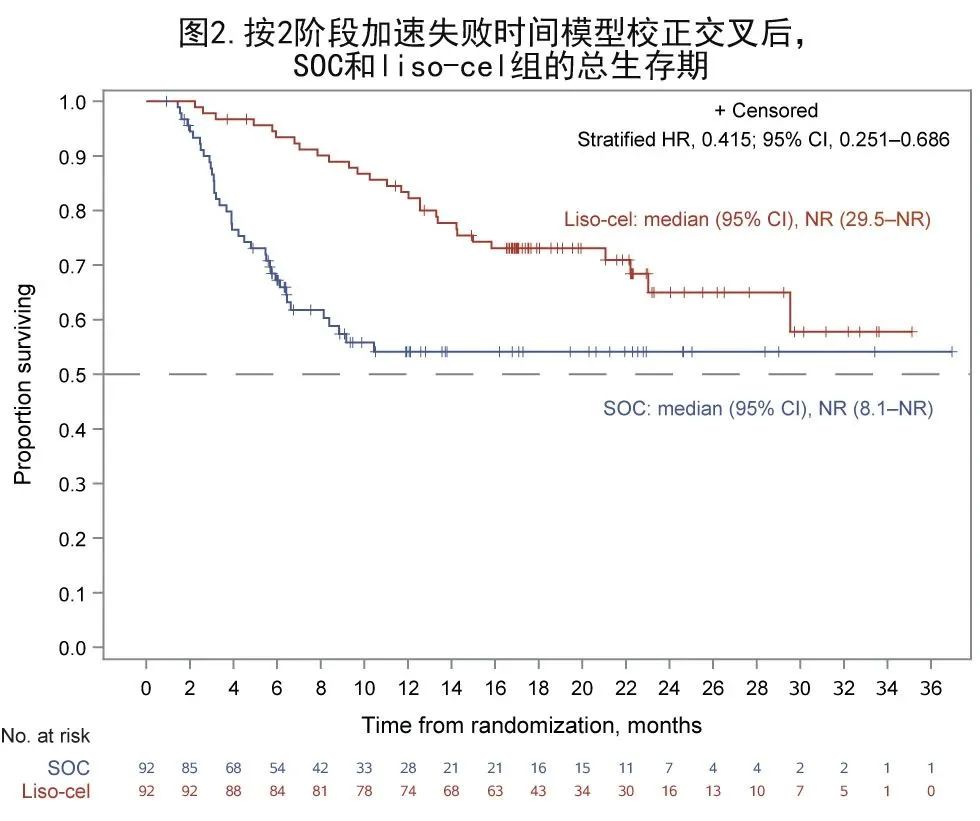
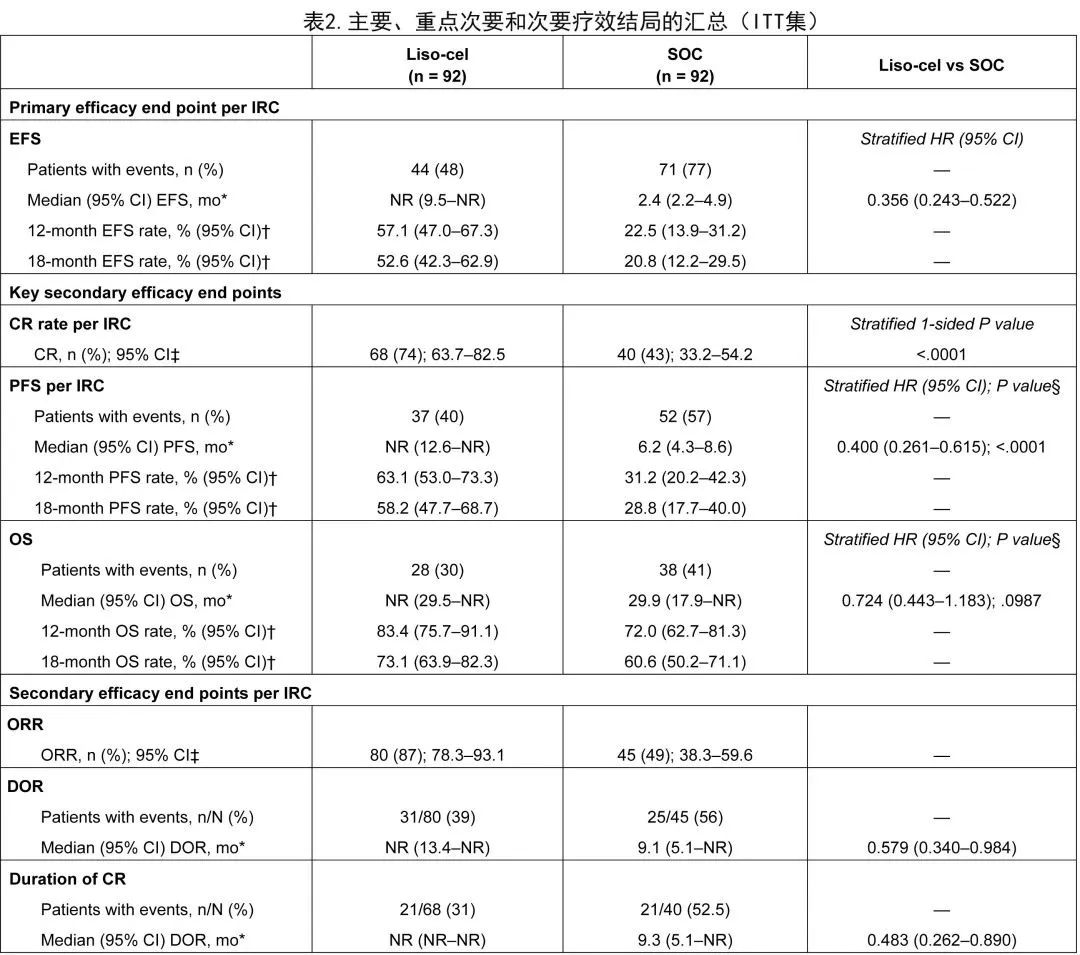 liso-cel 组有28例死亡,SOC组有38例死亡。liso-cel 组的中位 OS 为NR,SOC组为29.9个月(HR= 0.724;P= 0.0987;图1C),18个OS 率分别为73.1%和60.6%。使用2阶段加速失败时间模型(2-stage accelerated failure time model),针对交叉至接受 liso-cel 的 SOC 患者的治疗效应进行调整,liso-cel和 SOC 的中位 OS 均为NR(HR= 0.415,图2),liso-cel 组的18个月 OS 率为73.1%,SOC组为54.1%。与2阶段加速失败时间模型的结果一致,使用秩保持结构失败时间模型(rank-preserving structural failure time model)进行额外的 OS 分析显示 HR 为0.279,也有利于 liso-cel 组。
liso-cel 组有28例死亡,SOC组有38例死亡。liso-cel 组的中位 OS 为NR,SOC组为29.9个月(HR= 0.724;P= 0.0987;图1C),18个OS 率分别为73.1%和60.6%。使用2阶段加速失败时间模型(2-stage accelerated failure time model),针对交叉至接受 liso-cel 的 SOC 患者的治疗效应进行调整,liso-cel和 SOC 的中位 OS 均为NR(HR= 0.415,图2),liso-cel 组的18个月 OS 率为73.1%,SOC组为54.1%。与2阶段加速失败时间模型的结果一致,使用秩保持结构失败时间模型(rank-preserving structural failure time model)进行额外的 OS 分析显示 HR 为0.279,也有利于 liso-cel 组。
 次要疗效终点ORR、DOR和 CR 持续时间也有利于liso-cel(表2)。liso-cel 组的中位 CR 持续时间为NR,SOC组为9.3个月。在接受桥接治疗的58例患者中,桥接治疗后47例为 PET 阳性,9例为 PET 阴性,2例患者未进行清淋前化疗评估。当按桥接治疗使用情况进行分析时,无论患者在接受桥接治疗后是PET 阳性还是 PET 阴性,liso-cel也始终优于SOC。
次要疗效终点ORR、DOR和 CR 持续时间也有利于liso-cel(表2)。liso-cel 组的中位 CR 持续时间为NR,SOC组为9.3个月。在接受桥接治疗的58例患者中,桥接治疗后47例为 PET 阳性,9例为 PET 阴性,2例患者未进行清淋前化疗评估。当按桥接治疗使用情况进行分析时,无论患者在接受桥接治疗后是PET 阳性还是 PET 阴性,liso-cel也始终优于SOC。
安全性
两组中几乎所有患者均发生了治疗后出现的AE (TEAE)(表3)。最常见的任何级别 TEAE 为中性粒细胞减少、贫血、血小板减少和恶心,每组有超过半数的患者报告。两组中最常见的≥3级 AE 为中性粒细胞减少、血小板减少和贫血。66例患者在研究中死亡,其中liso-cel组28例,SOC组38例,包括交叉后29例,最常见的死亡原因是疾病进展。
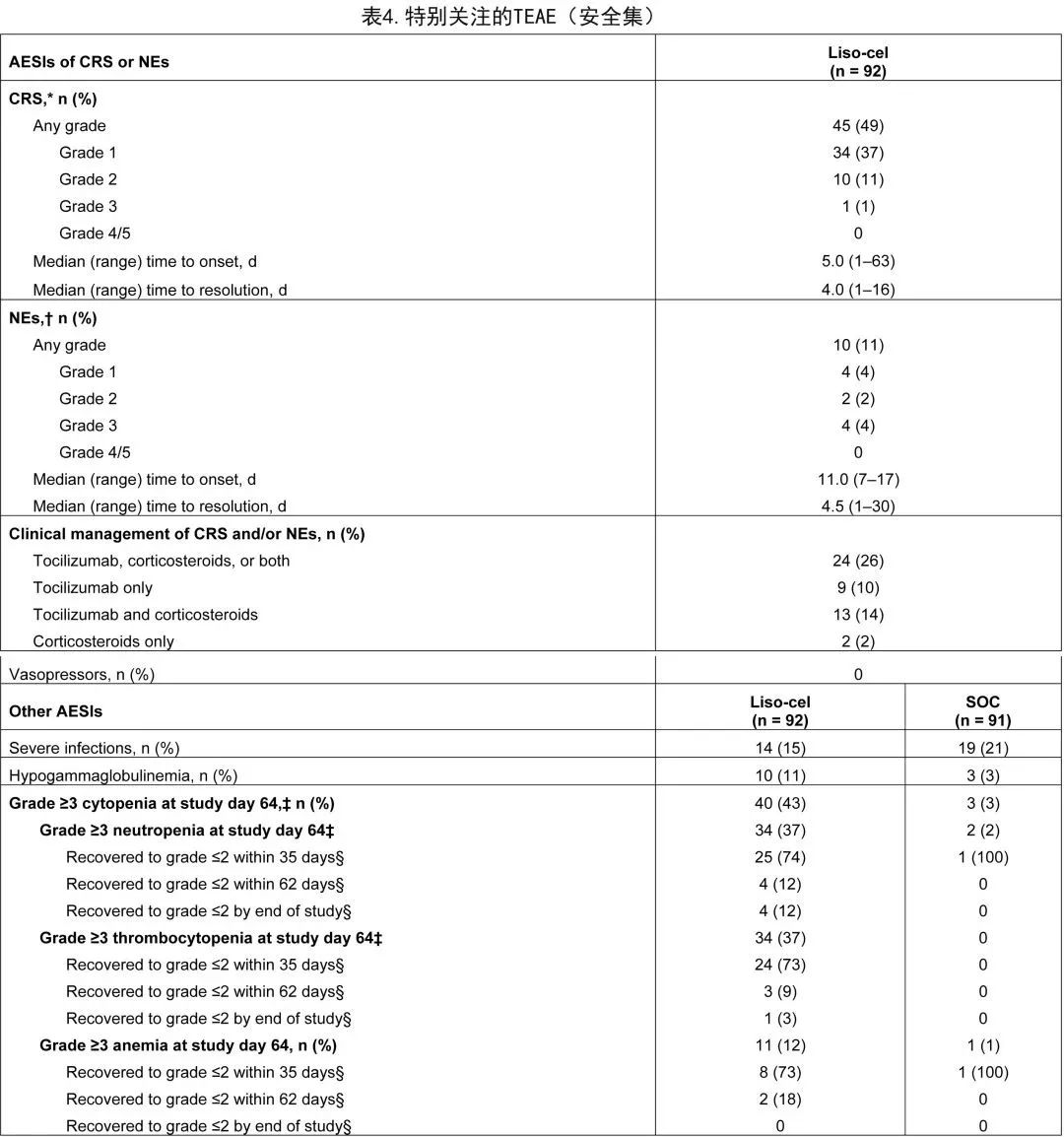
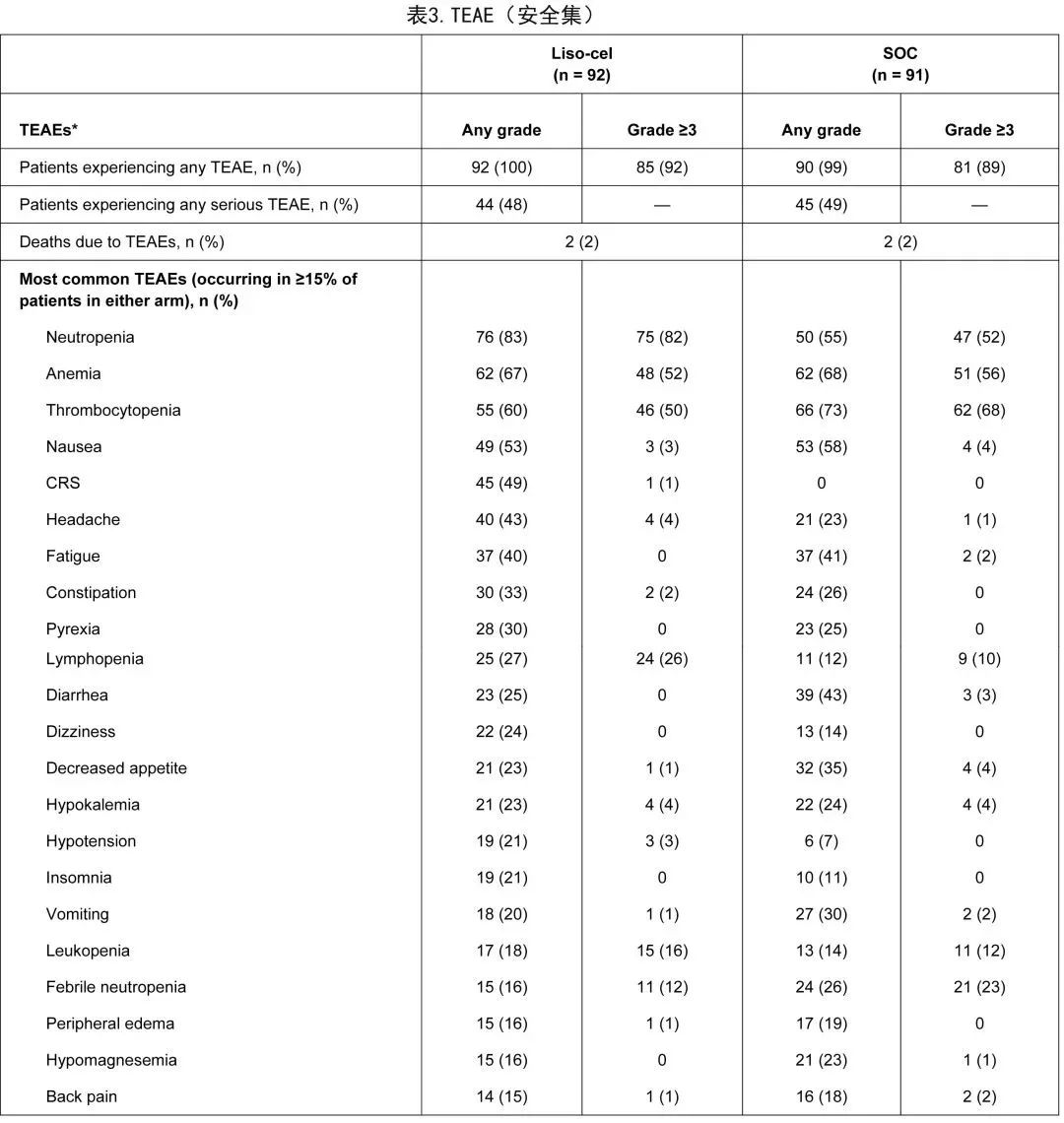 表4为 CAR T 细胞疗法特别关注的TEAE及其管理。任何级别 CRS 和 NE 的发生率分别为49%和11%,但3级 CRS 和 NE 的发生率分别仅为1%和4%,且无4级或5级事件。liso-cel 组和 SOC 组分别有14例 (15%) 和19例 (21%) 患者报告了重度感染。liso-cel 组40例 (43%) 患者报告了持续性血细胞减少,大多数 (73%) 在 liso-cel 输注后2个月内恢复至≤2级;SOC 组3例 (3%) 患者报告了长期血细胞减少。92例患者中有2例在 liso-cel 输注后90天以上报告感染(带状疱疹和肺炎各1例),未报告出血事件。liso-cel 组40例患者在随机化后研究第64天或之后接受至少一剂粒细胞集落刺激因子,12例患者接受免疫球蛋白,32例患者接受至少一剂浓缩红细胞输注,34例患者接受至少一剂血小板输注。liso-cel 组和 SOC 组分别有3例 (3%) 和7例(8%,包括交叉后的3例)患者报告第二原发恶性肿瘤。
表4为 CAR T 细胞疗法特别关注的TEAE及其管理。任何级别 CRS 和 NE 的发生率分别为49%和11%,但3级 CRS 和 NE 的发生率分别仅为1%和4%,且无4级或5级事件。liso-cel 组和 SOC 组分别有14例 (15%) 和19例 (21%) 患者报告了重度感染。liso-cel 组40例 (43%) 患者报告了持续性血细胞减少,大多数 (73%) 在 liso-cel 输注后2个月内恢复至≤2级;SOC 组3例 (3%) 患者报告了长期血细胞减少。92例患者中有2例在 liso-cel 输注后90天以上报告感染(带状疱疹和肺炎各1例),未报告出血事件。liso-cel 组40例患者在随机化后研究第64天或之后接受至少一剂粒细胞集落刺激因子,12例患者接受免疫球蛋白,32例患者接受至少一剂浓缩红细胞输注,34例患者接受至少一剂血小板输注。liso-cel 组和 SOC 组分别有3例 (3%) 和7例(8%,包括交叉后的3例)患者报告第二原发恶性肿瘤。
 结论
结论
TRANSFORM研究中位随访17.5个月的主要分析证实了 liso-cel 优于SOC,liso-cel 治疗导致EFS (NR vs 2.4个月)、CR率(74% vs 43.5%)和 PFS (NR vs 6.2个月)均显著改善;liso-cel 的OS (NR vs 29.9个月)在数值上优于SOC但无统计学差异。且与 liso-cel 的既往研究一致,任何级别和重度 CRS 和 NE 的发生率相对较低(CRS:分别为49%和1%;NE:分别为11%和4%;无4级或5级事件),并且本研究未预防性使用类固醇。
本研究与ZUMA-7和BELINDA研究一起,构成了在二线 LBCL 患者人群中开展的CAR T 细胞治疗重磅 III 期研究,但只有BELINDA研究失败。主要差异在于 TRANSFORM 允许使用方案定义的 SOC 方案进行1个周期的桥接治疗,而 ZUMA-7 中的桥接治疗仅限于糖皮质激素,TRANSFORM则包括内置交叉,能够立即使用 liso-cel 治疗(中位时间为15天),这在真实世界环境中是无法实现的。总的来说,这些结果支持使用 CAR T 细胞疗法作为 LBCL 患者的二线治疗。此外有趣的是,与交叉接受 liso-cel 作为三线治疗的患者相比,liso-cel组患者的 EFS 更长、缓解率更高。这一发现表明,在 CAR T 细胞治疗前二线免疫化疗失败的患者可能存在更高的耐药性或快速进展疾病;这些结局与 ZUMA-7 SOC 组中接受 CAR T 细胞治疗作为后续三线治疗的患者报告的结局一致。
综上所述,在原发难治性或早期复发性 LBCL 患者中,与化疗敏感患者接受含铂免疫化疗后接受大剂量化疗和 ASCT 的标准治疗相比,liso-cel作为二线治疗具有优效性,并且具有良好的安全性特征。这些数据支持与 SOC 相比,使用 liso-cel 作为原发性难治性或早期复发性 LBCL 患者的首选二线治疗。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












认真学习了
59