每年23包烟,基因突变就“顶天”!《自然》子刊:吸烟会加重支气管基底细胞的基因突变,每年23包烟突变增加达到顶峰
2022-05-31 奇点网 奇点网
当你读这篇文章的时候,世界上有多少人正在点燃那一缕烟雾?谁操控了烟草,而烟草又操控了谁?
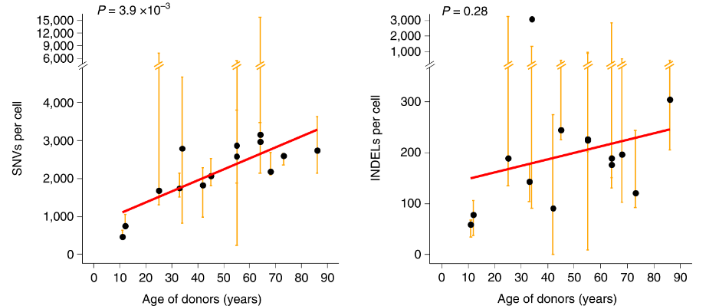
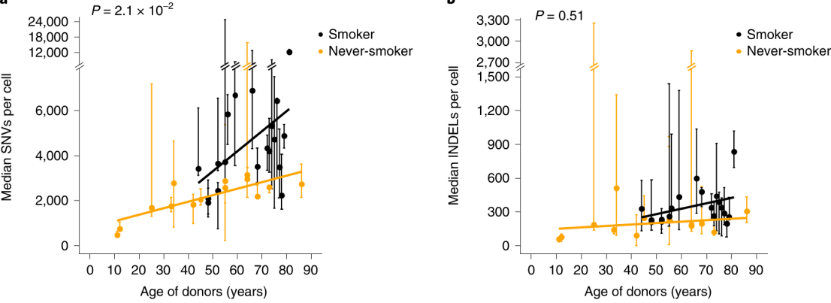
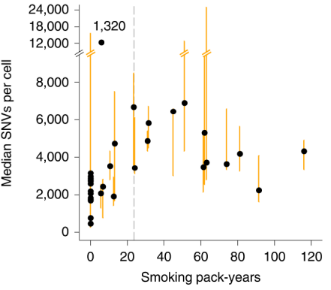
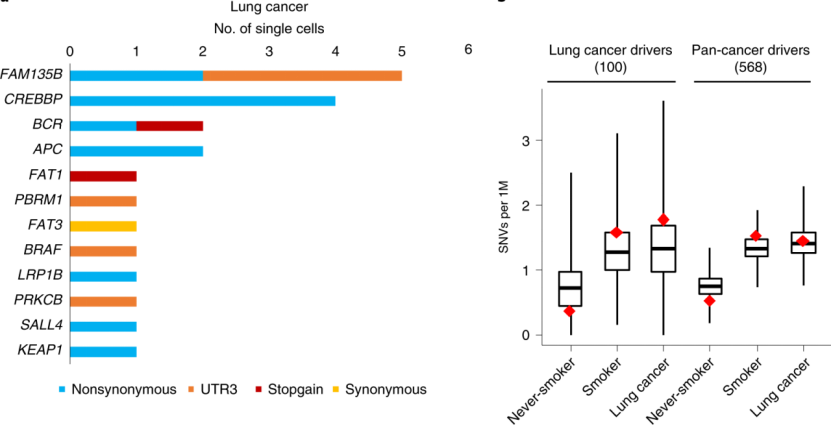
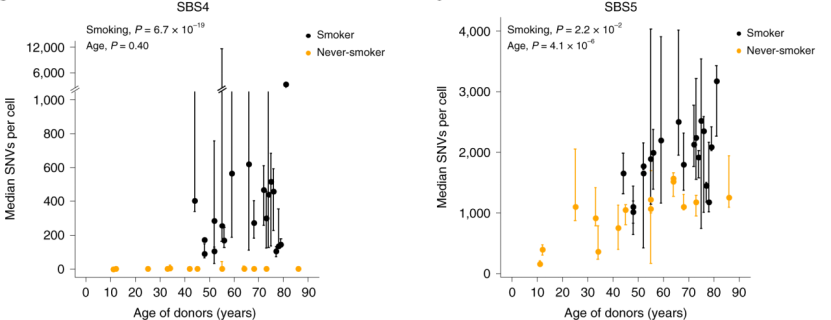
吸烟是肺癌的最主要“帮凶”之一这件事,已经是板上钉钉的了[1]。香烟中的化学物质,如多环芳香烃,能够引起细胞内DNA损伤,并导致癌症相关的基因突变[2]。但无法忽视的一个现象是,70%吸烟相关的死亡发生于高龄人群,并且80-90%终生吸烟者并未患肺癌[3, 4]。这也成了许多嗜烟人的借口,有恃无恐地“吞咽吐雾”。 已有多项研究表明,有吸烟史的肺癌患者肿瘤细胞中存在大量体细胞突变[5]。然而,对于鳞状细胞癌的主要祖细胞——远端支气管基底细胞的体细胞突变情况,尚缺乏研究[6]。另外,鲜少有量化、系统性的研究去探讨,年龄和吸烟量对于基因突变的影响。 基于上述现象和前期研究,来自美国阿尔伯特爱因斯坦医学院的Zhenqiu Huang领衔的团队,通过采集不同年龄段的14名从未吸烟者和19名吸烟者的远端支气管基底细胞,并进行单细胞全基因组测序,对单个基底细胞内的突变进行量化分析,结果发现,基因突变随年龄渐长而增多,吸烟会大大加重突变。还有个有意思的发现,就是突变水平随吸烟量的增加而变多,但是一旦超过每年23包,突变水平就不会显著增加了。 研究结果于近期发表在著名期刊Nature genetics上[7]。 研究首先探讨了年龄这一因素对于基因突变的影响。研究人员通过量化分析从未吸烟者基底细胞的基因突变情况,结果发现,随着年龄的增长,细胞核内单核苷酸位点变异(SNVs)和插入缺失突变(INDEL)中位值均呈升高趋势,其中SNVs的变化具有统计学差异(图1)。这就说明,即使不吸烟的情况下,年龄越大,远端支气管基底细胞的基因突变水平也会随之升高。 图1. SNVs(左图)和INDEL(右图)随年龄增长而增多 研究人员进一步分析了吸烟者基底细胞的基因突变情况,结果发现,吸烟者的SNVs和INDELs中位值也随年龄增长而升高,并且其SNVs的升高率要显著高于未吸烟者的。这说明,伴随年龄增长,吸烟会加重支气管基底细胞的基因突变(图2)。 图2. 吸烟与不吸烟两组参与者的SNVs(左)和INDELs(右)中位值随年龄增长而增高 研究人员还分析了吸烟量对基因突变的影响。研究过程发现了一例特殊的参与者(1320),这位参与者81岁轻度吸烟(每年6包),并刚刚诊断肺癌,其所有被检测的共6个细胞核内均出现高度突变。其中4个细胞核内均出现了DNA修复基因和多个肿瘤驱动基因的突变,提示这些细胞可能来源于同一个已具有恶性变化的细胞克隆。 当排除这位参与者后,基因突变频率随着吸烟量的增多也“直线”上升,然而,当每年吸烟量超过23包(中位值)后,基因突变频率就没这么“迅猛”升高了(图3)。这坐实了,吸越多的烟,基因就越“活跃”得突变。当然了,戒不掉烟的人看到这儿,千万不要想着“那我再多抽点儿也没事儿了”。因为累积的基因突变并不是引起肺癌的单纯因素,即使“再多抽几包烟”不会让基因突变更多,但可能通过其他途径促进肺癌的发生。 图3. 吸烟量少于每年23包时,SNVs中位值随年龄增长而升高 既然肿瘤驱动基因在肿瘤发展中很重要,研究人员分析了样本中已知肺癌和泛癌驱动基因的突变情况。结果发现,分别有11%和50%的细胞核内出现了肺癌驱动基因突变和泛癌驱动基因突变,但这在吸烟量相关肺癌的分析中并没有统计学差异(图4)。 图4. 包含肺癌驱动基因突变的细胞核数量(左);不吸烟、吸烟、肺癌三组中肺癌驱动基因和泛癌驱动基因存在SNVs的数量 就像水过留痕,细胞基因在受到各种内外源刺激发生损伤并修复过程中,会出现基因突变,并留下痕迹,我们称之为突变特征,这可以一定程度上用于推断发生了哪些变异[8]。 本研究中也对年龄或吸烟与哪些突变特征有关进行了分析。结果发现,SBS4(单碱基替换4)只在吸烟者的支气管基底细胞中出现。已有报道SBS4是有吸烟史肺癌的主要突变特征。以上提示SBS4是吸烟在基因组留下的“创伤”。另外,研究发现SBS5不仅与吸烟相关,更与年龄呈正相关关系(图5)。 图5. 吸烟和不吸烟两组包含SBS4(左)和SBS5(右)的细胞核内SNVs中位值与年龄的关系 除了体细胞突变外,遗传自父母的胚系突变也与肺癌的发生发展相关。研究人员也对远端支气管基底细胞的遗传背景相关突变进行了分析。其中一个值得注意的结果显示,2位有吸烟史的肺癌参与者的AKR1C2基因上出现了高于2倍的SBS4水平,而AKR1C2编码的蛋白是重要的多环芳香烃“解毒剂”。就提示了,这个基因的突变可能是吸烟容易诱发肺癌的重要因素。 自从500多年前哥伦布从美洲大陆将烟草带出,到今天每包香烟盒上标注着“吸烟有害健康”,烟草见证了人类社会的历史。烟草从当初被用来治病,到现在被证明致病,也伴随着人类疾病种类的改变、平均寿命的增长和医学的发展。随着1950年第一篇关于吸烟引起支气管肺癌的报道的出现,科学家对于烟草引起癌症的探究验证就未曾停止。 在前期研究报道的基础上,本项研究坐实了,吸烟会通过促进正常支气管基底细胞的体细胞突变进而提高患肺癌风险。更重要的是,此项研究加入了年龄这个重要因素,证明了随年龄增长,远端支气管基底细胞的基因突变也会增多,并且吸烟会增加基因突变的频率。 另外,大部分烟民并不患有肺癌,这篇报道也对此进行了解释。可能由于DNA修复准确率的增加或DNA损伤的降低,与肺癌发生发展相关的基因突变随之减少,于是减小了肺癌发生的风险。 当你读这篇文章的时候,世界上有多少人正在点燃那一缕烟雾?谁操控了烟草,而烟草又操控了谁? 参考文献: 1. W. D. Flanders, C. A. Lally, B. P. Zhu, S. J. Henley, M. J. Thun. Lung cancer mortality in relation to age, duration of smoking, and daily cigarette consumption: results from Cancer Prevention Study II. Cancer Res. 2003;63(19):6556-62. 2. J. E. Kucab, X. Zou, S. Morganella, M. Joel, A. S. Nanda, E. Nagy, et al. A Compendium of Mutational Signatures of Environmental Agents. Cell. 2019;177(4):821-36 e16. 3. D. M. Burns. Cigarette smoking among the elderly: disease consequences and the benefits of cessation. Am J Health Promot. 2000;14(6):357-61. 4. A. Crispo, P. Brennan, K. H. Jockel, A. Schaffrath-Rosario, H. E. Wichmann, F. Nyberg, et al. The cumulative risk of lung cancer among current, ex- and never-smokers in European men. Br J Cancer. 2004;91(7):1280-6. 5. L. B. Alexandrov, Y. S. Ju, K. Haase, P. Van Loo, I. Martincorena, S. Nik-Zainal, et al. Mutational signatures associated with tobacco smoking in human cancer. Science. 2016;354(6312):618-22. 6. R. Shaykhiev, R. Wang, R. K. Zwick, N. R. Hackett, R. Leung, M. A. Moore, et al. Airway basal cells of healthy smokers express an embryonic stem cell signature relevant to lung cancer. Stem Cells. 2013;31(9):1992-2002. 7. Z. Huang, S. Sun, M. Lee, A. Y. Maslov, M. Shi, S. Waldman, et al. Single-cell analysis of somatic mutations in human bronchial epithelial cells in relation to aging and smoking. Nat Genet. 2022;54(4):492-8. 8. L. B. Alexandrov, S. Nik-Zainal, D. C. Wedge, S. A. Aparicio, S. Behjati, A. V. Biankin, et al. Signatures of mutational processes in human cancer. Nature. 2013;500(7463):415-21.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#支气管#
54
#基底细胞#
30