提高CAR-T细胞的持久性
2022-10-02 小药说药 网络
在过去十年中,我们在提高CAR-T细胞疗法的疗效方面取得了显著进展。然而,其临床益处仍然有限,尤其是在实体肿瘤中。
前言
在过去十年中,我们在提高CAR-T细胞疗法的疗效方面取得了显著进展。然而,其临床益处仍然有限,尤其是在实体肿瘤中。即使在血液肿瘤中,由于多种因素,包括T细胞扩增不良和过继转移后缺乏长期持续性,对CAR-T疗法有反应的患者仍有复发的风险。这一问题在实体瘤中更为明显,因为肿瘤微环境对T细胞的存活、浸润和活性有负面影响。事实上,癌症的标志之一就是TME中过多的抑制性决定因素导致T细胞功能受损,从而导致T细胞耗竭。
有限的持久性仍然是CAR-T疗法发展的一个重大障碍,这是从细胞制造步骤开始就遇到的问题。包括CAR的设计和体外操作以及培养条件,可能在其中发挥关键作用。因此,工程化CAR-T细胞以提高其存活率并逆转或防止耗竭表型可能是一种合乎逻辑的治疗方法。现代合成生物学和基因组编辑技术提供了机会,迄今为止,一些研究已经采取了一些限制和创造抗耗竭T细胞的方法,并在几个关键的临床试验中进行了测试。这些方法可能改善CAR-T细胞的持久性问题,为患者带来希望。
影响CAR-T细胞持久性的因素
CAR的设计
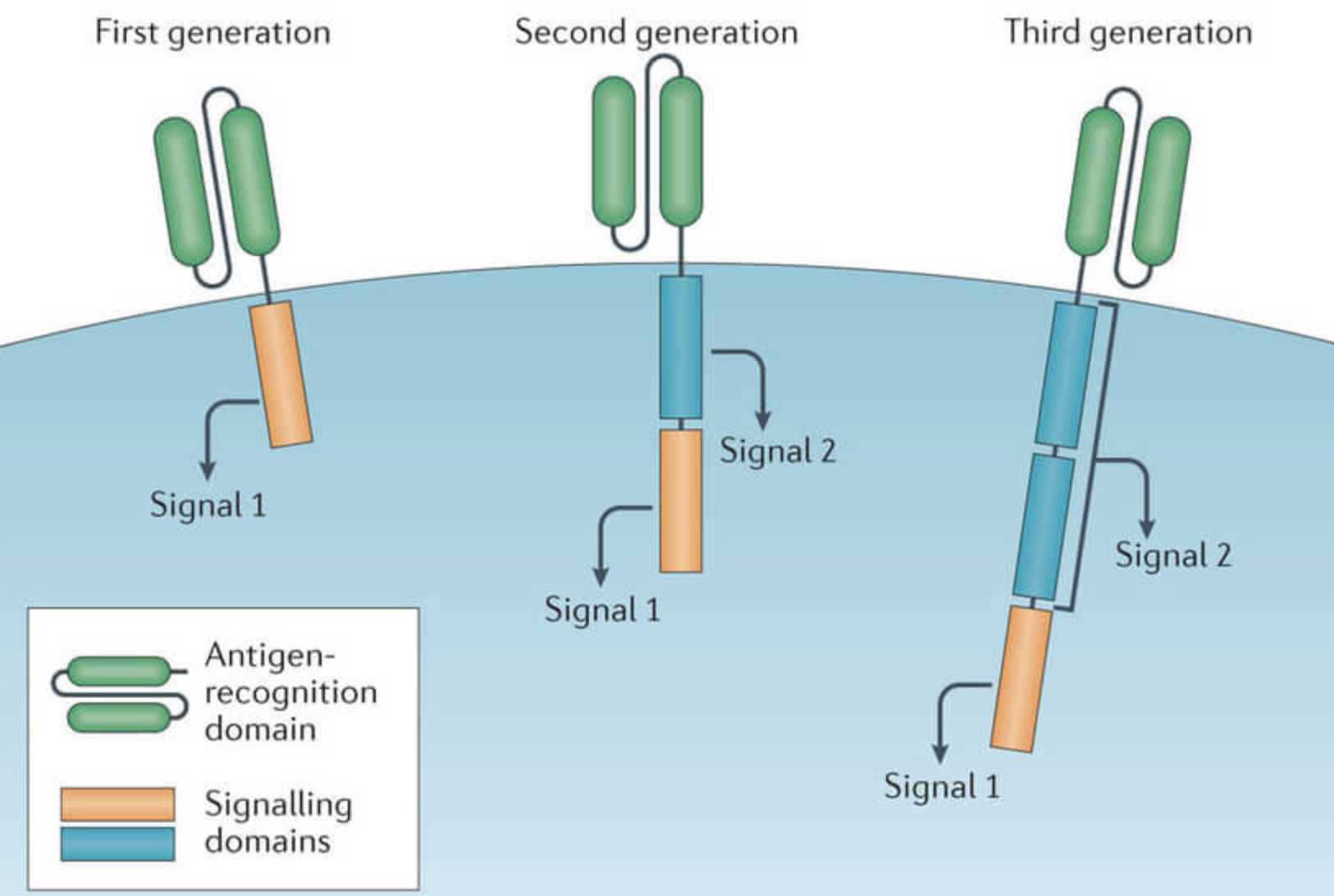
细胞外CAR结构域的类型、连接单链抗体与跨膜结构域的间隔区类型以及构成CAR的共刺激结构域已被证明对T细胞功能和持久性有深远影响。
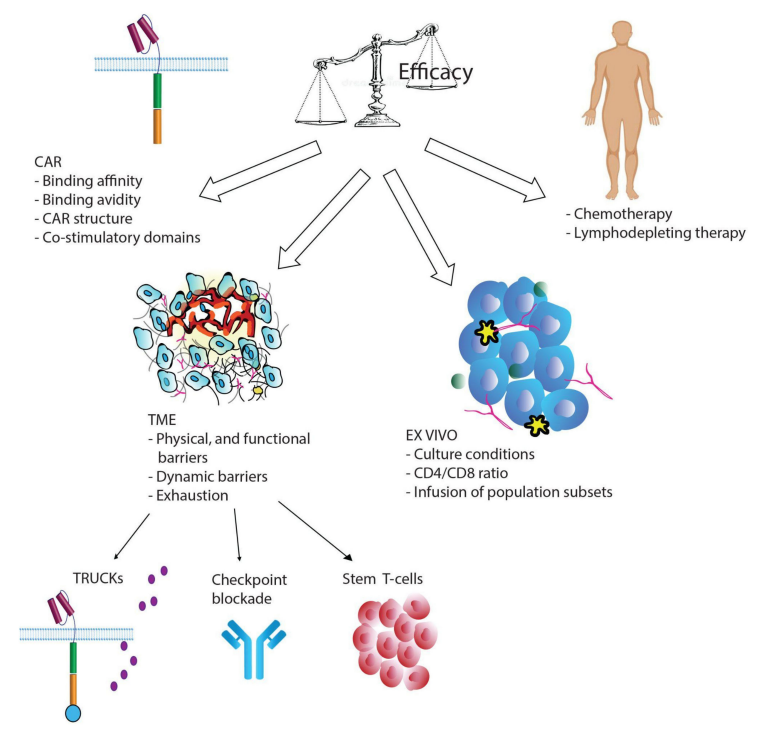
临床试验中使用的大多数CAR来源于小鼠,这可能导致体液和CD8+T细胞介导的免疫反应,导致免疫排斥。将含有小鼠成分的CAR-T细胞重新输入到首次治疗后出现CD19+复发的患者中基本上是无效的。此外,细胞表面的小鼠CAR受体簇可产生强直信号,导致T细胞耗竭。2016年,带有人源化scFv的CAR-T进入临床试验,人源化CAR显示出与小鼠CAR相似的细胞毒性活性,但是由于较低的免疫原性而增强了持久性。
CAR的亲和力影响强直信号,对靶细胞过强的亲和力可能导致T细胞耗竭。一项研究开发了一种CAT-CAR(CD19单链抗体),其与CD19的亲和力比从传统的CAR低40倍。该结构在复发或难治性儿童BLL患者中进行了测试,临床研究发现,14例CAR-T细胞扩增增加的患者中有11例表现出持续性。
此外,共刺激域在CAR-T细胞的持久性和有效性中也起着关键作用,共刺激分子包括CD28、ICOS、CD27、4-1BB、OX40和CD40L。几项研究发现,配备4-1BB结构域而非CD28结构域的CAR结构中的T细胞持久性增强。其他研究报告,含有4-1BB的CAR-T细胞显示出增强的记忆T细胞(TEM)表型,这可能延迟CAR-T细胞耗竭。ICOS属于CD28共刺激分子家族,研究证明,CAR结构中ICOS和4-1BB共刺激结构域的组合显著增加T细胞的持久性。
尽管存在相互矛盾的证据,但人们认识到CD28-CAR与高效应器功能和有限的T细胞持久性相关,而4-1BB-CAR和ICOS-CAR的效力较低,但持续时间较长。因此,这些观察结果表明,共刺激域的结构是影响CAR-T细胞持久性的重要因素。
体外操作和淋巴清除
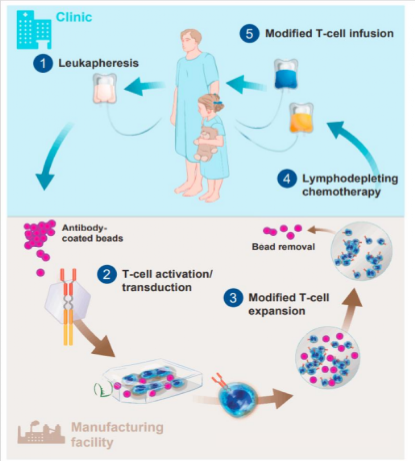
制造T细胞的过程需要从患者身上获取足够数量的健康T细胞。然而,经过化疗治疗,尤其是那些含有氯法拉滨或阿霉素的化疗,导致淋巴细胞减少会使最终的CAR-T细胞质量不理想,用于输注的T细胞类型严重影响治疗的效果。
事实上,通过使CD4/CD8比率正常化或使用幼稚或记忆细胞亚群,在临床前模型中获得了更好的持久性。几项研究表明,使用早期谱系细胞富集的T细胞群能够更好地扩增,并提高CAR-T细胞治疗的持久性和疗效。此外,多项研究表明,在制造过程中向细胞培养物中添加抗氧化剂,如N-乙酰半胱氨酸,也可抑制效应器分化并促进TSCM细胞的扩增。
在CAR T细胞输注的前几天,患者接受一种淋巴清除的化疗方案,最常见的是环磷酰胺(cy)、氟达拉滨(flu)和苯达莫司汀(ben)。淋巴清除疗法根除调节性T细胞(Treg)和其他免疫抑制细胞,增加CAR-T细胞的扩增并延长其持续性。正如在成人B-ALL和B-NHL临床试验中观察到的那样,充分的淋巴清除对治疗成功至关重要,并可能防止CAR的排斥反应。
T细胞耗竭
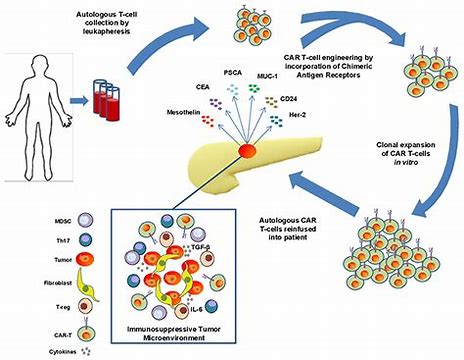
在TME中,髓源性抑制细胞(MDSC)、癌相关成纤维细胞(CAF)和肿瘤细胞产生的免疫抑制细胞因子的存在会导致T细胞耗竭。
慢性暴露于抗原也可导致T细胞衰竭,如果抗原刺激持续存在,T细胞会发生一系列表观遗传、代谢和转录改变,出现耗竭状态的表征。这种过程以递进的方式发生,IL-2和TNF-α在早期丢失,IFN-γ和趋化因子分泌在耗竭进展后期减少。尽管高增殖能力也在早期丧失,但在体内受到刺激时,耗竭的T细胞仍能有限增殖。
耗竭的细胞也表现出抑制性受体的高表达,如PD-1、TIM-3、LAG-3、CD160、BTLA、CTLA-4和TIGIT。
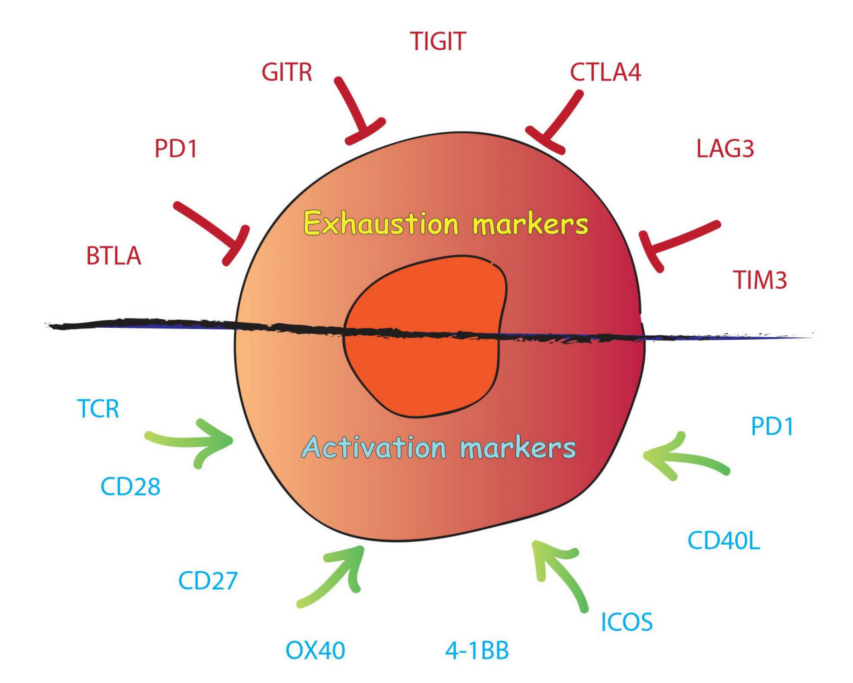
提高CAR-T细胞持久性和效力的策略
表达细胞因子及其受体
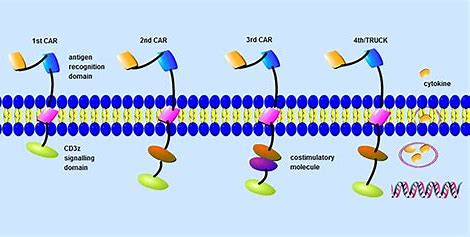
第四代CAR T细胞最近被开发出来,用于抵抗TME中的免疫抑制环境,同时克服免疫耗竭。TRUMKS设计将CAR-T细胞的细胞毒性功能与具有免疫调节能力的细胞因子的原位递送结合起来。在诱导系统的作用下,在CAR结合抗原后,细胞因子被合成,并以自分泌方式发挥作用,以增加T细胞的存活和扩增。细胞因子也可以旁分泌方式发挥作用,调节周围环境,干扰TME中存在的免疫抑制细胞因子。包括IL-12、IL-7、IL-15、IL-18、IL-21和IL-23在内的一系列细胞因子目前正在研究中,并已进入早期临床试验阶段。
IL-12是一种促炎症细胞因子,可诱导Th1CD4+T细胞反应,促进CD8+克隆扩增和持续存在。它还负责调节CTL和自然杀伤(NK)细胞的细胞毒性活性,重新激活无能的肿瘤浸润淋巴细胞,招募NK细胞,并抑制Treg。对结构性表达IL-12的CD19-CAR-T细胞的临床前研究表明,它增强了肿瘤杀伤效果和针对癌症抗原的免疫记忆。然而,与IL-12相关的潜在致命毒性使得有必要开发一种诱导系统,仅在CAR激活时限制IL-12的分泌。一些临床研究(NCT02498912、NCT03932565和NCT03542799)正在进行和招募中。
IL-15是一种刺激CD8+T细胞和NK细胞活化、增殖和细胞毒性活性的细胞因子。IL-18增加Th1细胞细胞因子的产生,同时抑制IL-10的合成。IL-15和IL-18都是免疫反应的增强剂,已经在CAR-T细胞上进行了测试。与传统的CAR-T细胞相比,分泌IL-18和IL-15的CAR-T细胞在荷瘤小鼠中显示出增强的扩张性和持久性,并且在体外和体内显示出增强的肿瘤细胞毒性。目前正在招募多项临床试验,使用工程化T细胞和NK细胞测试IL-15和IL-18分泌的CAR在实体瘤和血液瘤中的作用。
最近的研究表明,在同一个CAR-T细胞中共同表达多种细胞因子是可能的。NCT04833504是最近完成的一项临床试验,其中在复发或难治性B细胞淋巴瘤患者中检测表达IL-7和CCL19的CD19+CART细胞,但结果尚未报道。目前正在招募另外两项临床试验,以检测表达IL-7的CAR-T细胞与PD-1阻断剂或其他细胞因子的分泌相结合。
联合检查点阻断疗法
通过抑制检查点信号减少耗竭的策略包括通过shRNA表达载体或CRISPR/Cas9敲除共抑制分子。许多研究报告,阻断检查点抑制可恢复细胞因子的产生并促进CAR-T细胞存活。此外,同时阻断多个免疫检查点,如PD-1、TIM-3和LAG-3,可协同增加CAR-T细胞的效应器功能。
将CAR-T细胞与免疫检查点阻断疗法相结合可能是增强抗肿瘤活性、持久性和记忆细胞形成的有效策略。在胶质母细胞瘤和乳腺癌细胞系中,抗PD-1抗体增强了抗HER2 CAR-T细胞的抗肿瘤活性。然而,一些临床试验报告,在使用PD-1抑制剂和抗GD2 CAR-T细胞联合治疗神经母细胞瘤患者后,结果为阴性。
此外,一些研究已经采用其他策略来阻断PD-1,例如基因编辑以使CAR-T细胞分泌PD-1阻断抗体或下调PD-1。
使用干性T细胞
效应T细胞最初被认为是ACT的最佳产品,因为它们具有杀死肿瘤细胞的功效。然而,它们的持久性有限,并且扩增能力很差,很容易发生耗竭。
TSCM由于其寿命长、自我更新能力强以及在不同T细胞群中的分化能力,是ACT的理想候选。临床研究表明,输注表型和功能性TSCM样CAR-T细胞(CD62L+、CD28+和CD27+)可产生良好的结果。例如,使用抗CD-19 CAR-T细胞治疗的CLL和多发性骨髓瘤患者显示出与CD27+CD45RO−CD8细胞群相关的良好反应。此外,对小鼠的研究表明,注入富含CD62L+的T细胞群可增加扩增和持久性,从而导致持久的肿瘤消退。
小结
尽管在过去十年中CAR-T细胞治疗取得了显著进展,然而CAR-T细胞在患者体内的有限持久性依然是一个挑战,主要原因是T细胞耗竭。通过对CAR结构设计,改变生产条件,或引入新的治疗方法,我们可能创造抗耗竭的工程化T细胞,从而进一步扩大CAR-T细胞的临床应用。尽管迄今为止的结果仍然有限,但可能性是无穷的,突破可能即将到来。
参考文献:
1.Improving CAR T-Cell Persistence. Int J MolSci. 2021 Oct; 22(19): 10828.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言