FDA批准辉瑞和莫德纳针对奥密克戎BA.4、BA.5新冠疫苗获美紧急使用授权 (EUA)
2022-09-01 MedSci原创 MedSci原创
美国食品药品监督管理局(FDA)8月31日宣布,批准莫德纳和辉瑞-BioNTech二价新冠疫苗的紧急使用。FDA将允许在个人在首次接种新冠疫苗、或者接种加强针两个月后接种上述两款疫苗。本次获得紧急使用
美国食品药品监督管理局(FDA)8月31日宣布,批准莫德纳和辉瑞-BioNTech二价新冠疫苗的紧急使用授权 (EUA)。,以授权将疫苗的二价制剂用作单次加强剂、或在初次加强疫苗接种后至少两个月后使用
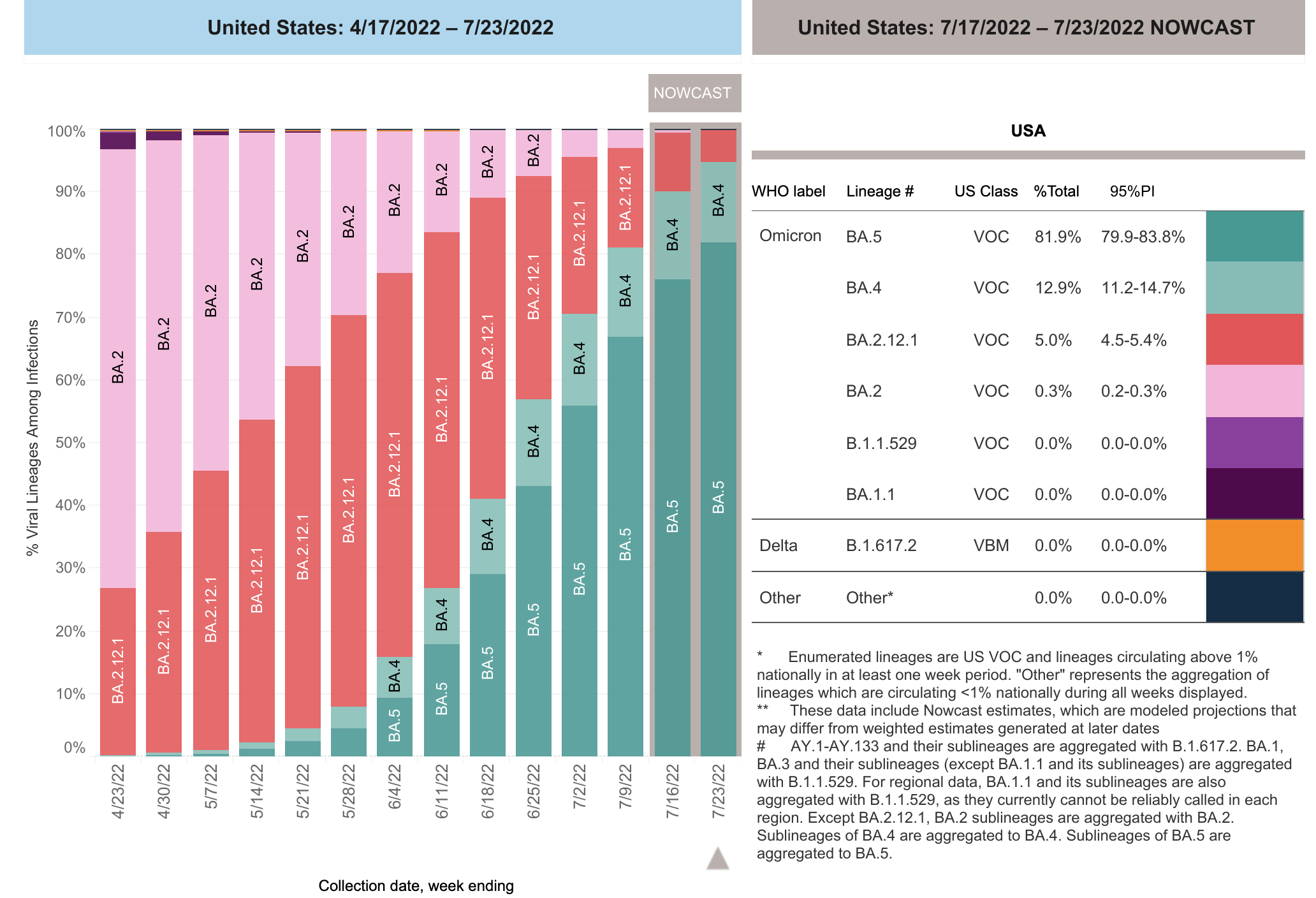
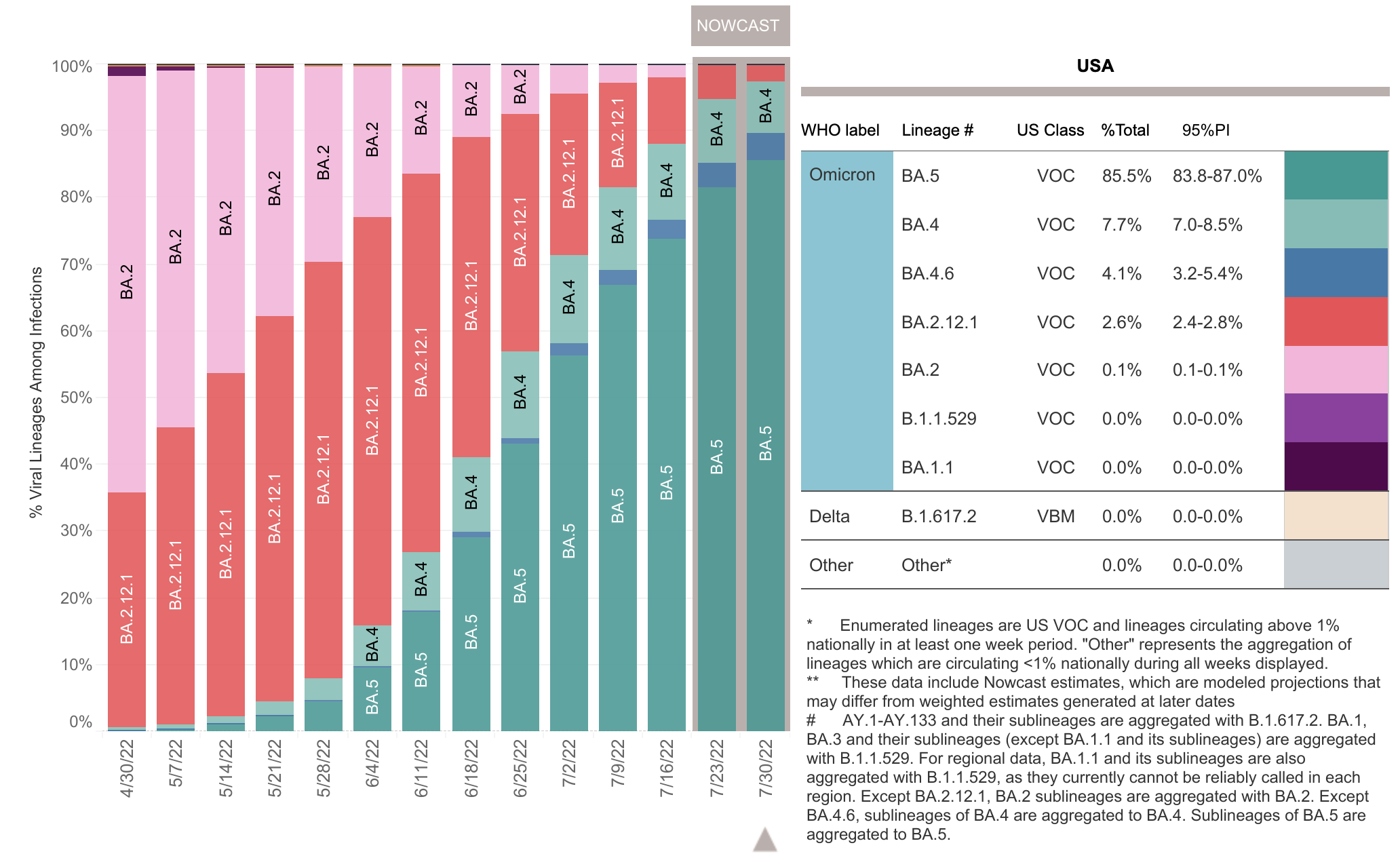
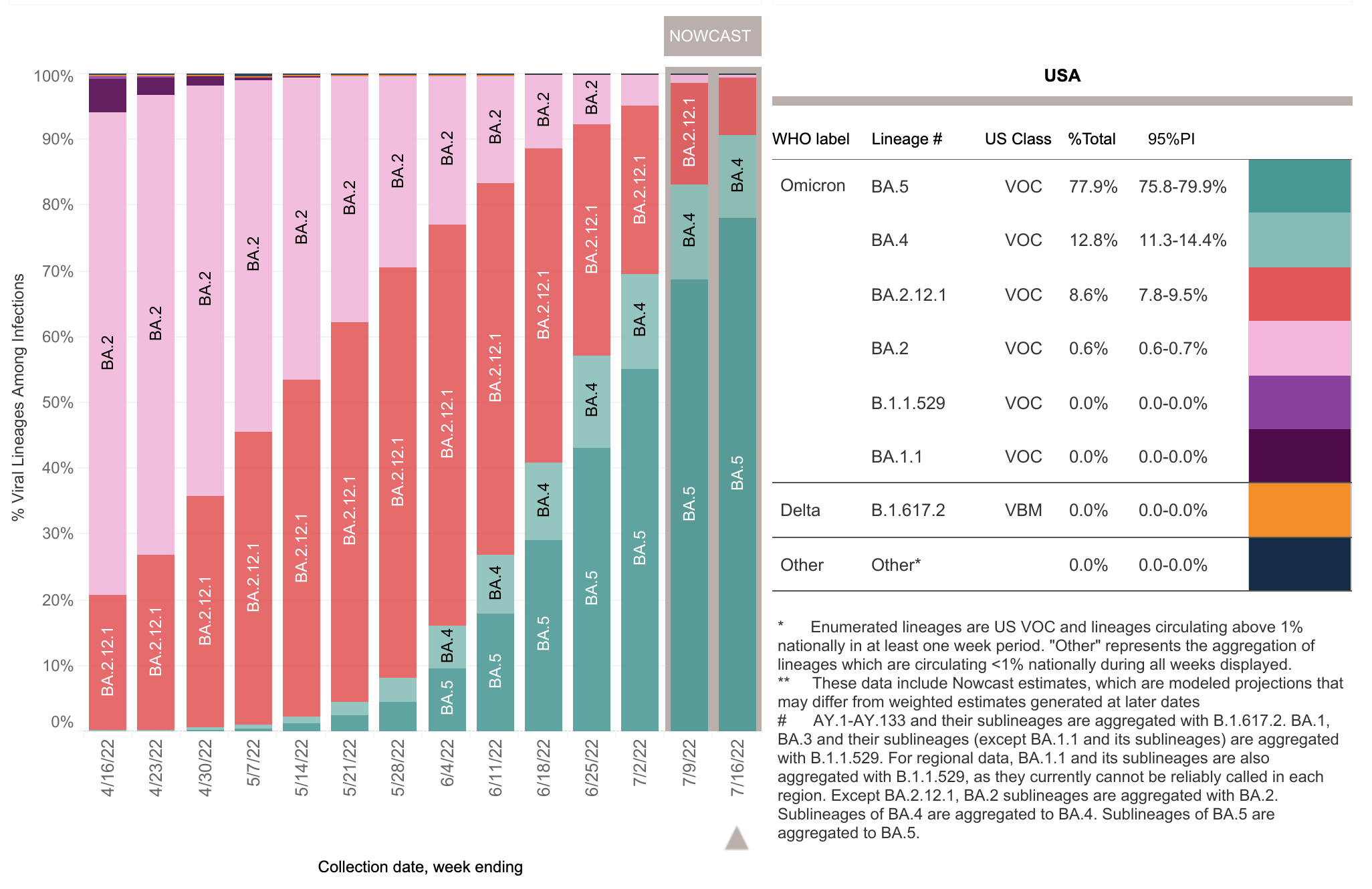
二价疫苗,我们也将其称为“更新的增强剂”,包含 SARS-CoV-2 病毒的两种信使 RNA (mRNA) 成分,一种是 SARS-CoV-2 的原始毒株,另一种是两者之间的共同SARS-CoV-2 omicron 变体的 BA.4 和 BA.5 谱系。
Moderna COVID-19 疫苗,二价,被授权在 18 岁及以上的个体中用作单次加强剂量。 Pfizer-BioNTech COVID-19 疫苗,二价,被授权在 12 岁及以上的个体中用作单次加强剂量。
8月22日与23日,两家公司分别向FDA提交了相关申请,见:
Moderna递交Omicron特异性mRNA疫苗mRNA-1273.222紧急使用授权申请
辉瑞/BioNTech向FDA和EMA提交二价奥密克戎特异性mRNA疫苗上市申请
“包括加强剂在内的 COVID-19 疫苗继续挽救无数生命并防止 COVID-19 最严重的后果(住院和死亡),”FDA 专员 Robert M. Califf 医学博士说,“当我们进入秋季并开始花更多的时间在室内,我们强烈鼓励所有符合二价 COVID-19 疫苗加强剂量标准的人接种加强针,以更好地保护当前流行的变种。”
Moderna COVID-19疫苗,二价和辉瑞-BioNTech COVID-19疫苗,二价含有来自 SARS-CoV-2病毒的 mRNA。这些疫苗中的 mRNA 是一种特定的遗传物质,它指导体内细胞制造原始病毒株和 omicron 变体谱系 BA.4 和 BA.5 的独特“刺突”蛋白。 BA.4 和 BA.5 的刺突蛋白是相同的。
“ FDA 一直在计划可能需要修改 COVID-19疫苗的成分以解决不断出现新的变体的问题。我们也征求了外部专家的意见,就在 COVID-19 加强针中加入 omicron 成分以提供更好的 加强对COVID-19 防护。我们与疫苗制造商密切合作,以确保安全有效地开发这些更新的增强针。 FDA 在年度流感疫苗的毒株变化方面拥有丰富的经验。我们对支持这些授权的证据充满信心,”FDA 生物制品评估和研究中心主任、医学博士Peter Marks 说。 “公众可以放心,FDA 已经采取了大量措施,以确保这些二价 COVID-19 疫苗符合我们严格的安全性、有效性和制造质量标准,以用于紧急使用授权。”
对于今天授权的每种二价 COVID-19 疫苗,FDA 评估了来自二价 COVID-19 疫苗加强剂量的临床研究的免疫原性和安全性数据,该疫苗含有 SARS-CoV-2 原始毒株的一种成分和一种omicron 谱系 BA.1 的组成部分。 FDA 认为这些数据与含有 omicron 变体 BA.4 和 BA.5 谱系成分的疫苗相关且支持。此外,有关当前 mRNA COVID-19 疫苗的安全性和有效性的数据,这些疫苗已用于数百万人,包括在 COVID-19 的暴发期间,也有助于该机构的评估。
为了评估单次加强剂量的辉瑞-BioNTech COVID-19二价疫苗对 12 岁及以上个体的有效性,FDA 分析了大约 600 名 55 岁以上的成年人的免疫反应数据,这些成年人之前曾接受过2 剂单价 Pfizer-BioNTech COVID-19 疫苗的和 1 剂加强剂。这些参与者在第一次加强剂量后 4.7 至 13.1 个月接受了第二次加强剂量的单价 Pfizer-BioNTech COVID-19 疫苗或 Pfizer-BioNTech 的研究性二价 COVID-19 疫苗(原始和 omicron BA.1)。一个月后,接受二价疫苗的参与者对 BA.1 的免疫反应优于接受单价 Pfizer-BioNTech COVID-19 疫苗的参与者的免疫反应。
Pfizer-BioNTech COVID-19 二价疫苗加强剂量对 12 岁及以上个体的安全性基于一项临床研究的安全性数据,该临床研究评估了 Pfizer-BioNTech 研究性二价 COVID-19 疫苗的加强剂量(原始和 omicron BA.1)、评估单价 Pfizer-BioNTech COVID-19 疫苗的初次和加强疫苗接种的临床试验的安全性数据,以及单价 Pfizer-BioNTech COVID-19 疫苗的上市后安全性数据。
二价疫苗(原始和 omicron BA.1)和单价 Pfizer-BioNTech COVID-19 疫苗的安全数据与 Pfizer-BioNTech COVID-19 二价疫苗相关,因为这些疫苗是使用相同的工艺制造的。
评估二价疫苗(原始和 omicron BA.1)加强剂量安全性的临床研究包括大约 600 名 55 岁以上的参与者,他们之前曾接受过 2 剂主要系列疫苗,单价疫苗加强剂量Pfizer-BioNTech COVID-19 疫苗,然后在 4.7 到 13.1 个月后,接受了第二次加强剂量的单价 Pfizer-BioNTech COVID-19 疫苗或 Pfizer-BioNTech 的研究性二价 COVID-19 疫苗(原始和 omicron BA.1) .在接受二价疫苗的研究参与者中,最常见的副作用包括注射部位疼痛、发红和肿胀、疲劳、头痛、肌肉疼痛、寒战、关节痛和发烧。
面向接受者和护理人员以及医疗保健提供者的二价 COVID-19 疫苗的情况说明书包括有关潜在副作用以及心肌炎和心包炎风险的信息。
在今天的授权下,FDA 还修订了 Moderna COVID-19 疫苗和 Pfizer-BioNTech COVID-19 疫苗的 EUA,取消使用单价 Moderna 和 Pfizer-BioNTech COVID-19疫苗分别对 18 岁和12岁的个人作为加强针。如授权书所述,这些单价疫苗继续被授权用于 6 个月及以上年龄个体的初级系列接种。
参考资料:
https://www.fda.gov/news-events/press-announcements/coronavirus-covid-19-update-fda-authorizes-moderna-pfizer-biontech-bivalent-covid-19-vaccines-use
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#FDA批准#
43
#紧急#
53
比较及时!
49
以后就象每年的#流感疫苗#一样,WHO预测一下可能流行的是什么毒株,然后让各个厂家开始制备疫苗,然后秋冬使用。不过,现在#mRNA疫苗#制备速度要比传统疫苗更快(3个月一个周期),因此,未来#奥密克戎#一旦稳定(出现一些稳定的变异株,不断反复流行),这样只需要把对应的#疫苗#放出来就行了。现在这个二价#奥密克戎疫苗#,几乎对从原始毒株,到最新的#BA.4/5#均具有较好的预防作用,防重症更不用说了。
108