阿斯利康公布新冠疫苗3期临床试验安全性和有效性
2021-03-26 生物探索 生物探索
当地时间3月25日,阿斯利康(AstraZeneca)官网宣布,新冠疫苗AZD1222的Ⅲ期临床试验的初步分析结果与3月22日公布的中期分析结果一致。

当地时间3月25日,阿斯利康(AstraZeneca)官网宣布,新冠疫苗AZD1222的Ⅲ期临床试验的初步分析结果与3月22日公布的中期分析结果一致。
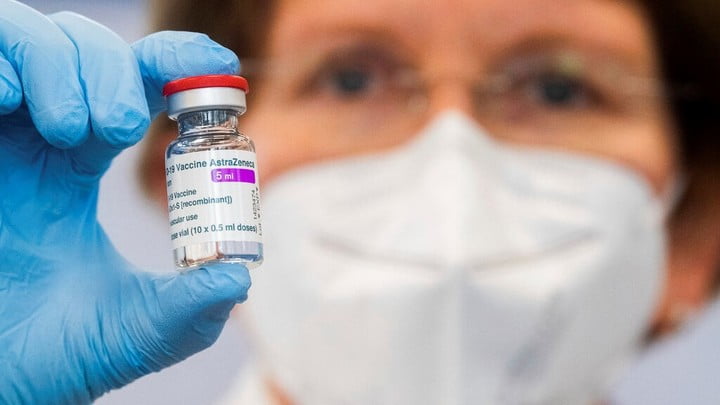
新冠疫苗AZD1222是由牛津大学与Vaccitech公司共同发明。它使用基于普通感冒腺病毒的弱化版本复制缺陷型黑猩猩病毒载体,该病毒在黑猩猩中引起感染,并包含SARS-CoV-2病毒刺突蛋白的遗传物质。接种疫苗后,会产生表面刺突蛋白,激发免疫系统攻击SARS-CoV-2病毒。AZD1222的Ⅲ期临床试验主要功效分析共纳入190名COVID-19患者,比中期分析增加了49例病例,其中有14例病例可能需要裁定,因此病例总数可能略有波动。
临床结果显示,该疫苗预防出现症状的COVID-19效力为76%(CI: 68%-82%);此外,各年龄组的结果相当,65岁及以上成人的疫苗的效力为85%(CI: 58%-95%);预防重度或危重疾病和住院的关键次要终点证实了100%的效力;这些数据进一步证明了阿斯利康疫苗是安全有效的。
这是AZD1222的安全性收到美国数据安全监测委员会(DSMB)质疑后公布的最新官方数据,据悉,AZD1222的Ⅲ期临床结果已提交给独立的数据安全监控委员会(DSMB)。主要分析已在试验方案中预先规定,并将成为未来几周向美国FDA提交紧急使用授权(EUA)的监管依据。
阿斯利康表示,未来几周内将会提交AZD1222的主要分析结果,以供同行评审发表。
迄今为止,全球已累计确诊人数超1亿,希望新冠疫苗能够尽快帮助终结疫情,结束这场噩梦。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#3期临床#
36
#安全性和有效性#
38
#3期临床试验#
44
新冠肺炎,疫情何时才能消失
59
了解
94