Bcl-2抑制剂最新研究进展
2023-06-10 精准药物 精准药物 发表于陕西省
在今年入选ASCO摘要的品种中,以亚盛医药、百济神州为代表的企业,公布了旗下Bcl-2抑制剂的最新研究数据。
2023年ASCO大会于6月2日至6日在美国伊利诺伊州芝加哥以线上线下混合会议形式举办,作为全球规模最大、学术水平最高、最具权威的临床肿瘤学会议,ASCO年会每年都会展示当前国际最前沿的临床肿瘤学科研成果和肿瘤治疗技术,被誉为是引领全球肿瘤诊疗方向的“风向标”。由于诸多重要的研究发现和临床数据会被选择在会上进行首次发布,这也让每年ASCO年会成为观察全球药企创新实力的最佳窗口。
在今年入选ASCO摘要的品种中,以亚盛医药、百济神州为代表的企业,公布了旗下Bcl-2抑制剂的最新研究数据。Bcl-2 蛋白家族于内源性细胞凋亡通路上发挥重要把关作用。Bcl-2 蛋白家族的成员可分为三个功能组别:抗凋亡蛋白(如Bcl-2 及Bcl-xL)、促凋亡效应因子及促凋亡活化因子。在肿瘤细胞中,科学家发现Bcl-2 常处于过表达状态,最终防止肿瘤细胞正常凋亡。就实体瘤而言,在前列腺癌、乳腺癌、小细胞肺癌和非小细胞肺癌等肿瘤均观察到Bcl-2 超表达,显示出Bcl-2 可能与此类肿瘤有关。除了实体瘤外,Bcl-2 超表达可能与血液肿瘤也有关系,如白血病与淋巴瘤。
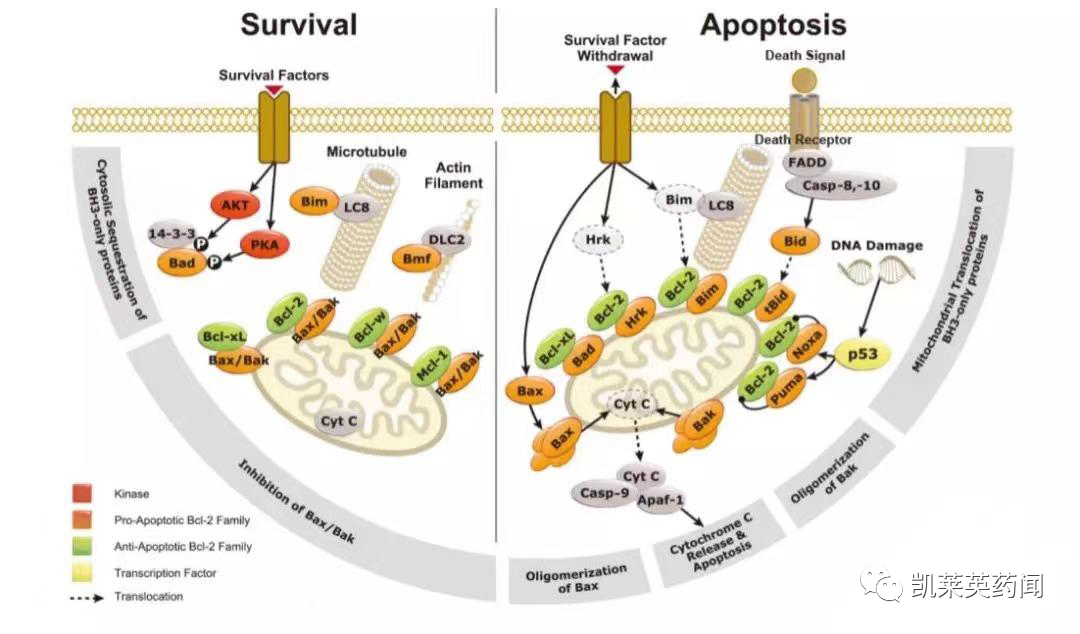
近年来,BcL-2领域药物开发进展缓慢,维奈克拉上市7年一直未有新药获批,在本次ASCO中,共更新了十余篇关于Bcl-2抑制剂的研究数据。下面我们具体看看产品的研发进展,尝试分析部分Bcl-2抑制剂的应用潜力与未来的前景。
2023 ASCO中Bcl-2抑制剂的研究更新
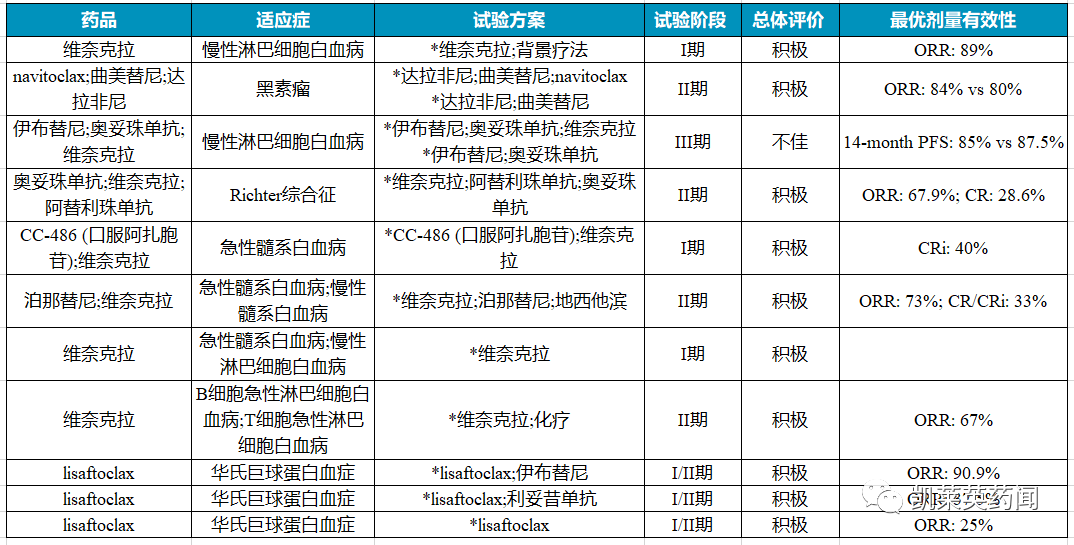
一 艾伯维:维奈克拉
维奈克拉(Venclexta)于2016 年获FDA 批准上市。自上市后,维奈克拉的销售额一路高歌猛进。2021 年,维奈克拉全球销售额达18.2 亿美元,同比增长36.1%;2022年销售额达20.1 亿美元,同比增长10.4%。据公司方预计,维奈克拉峰值销售有望在2026 年将达到60 亿美元。
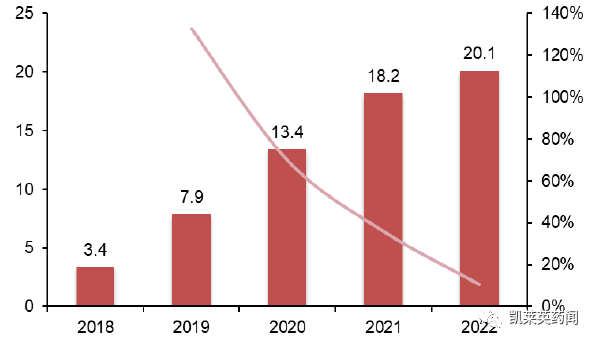
目前,维奈克拉共获批五个适应症,包括三个一线适应症与两个二线适应症,其中与阿扎胞苷或低剂量阿糖胞苷(LDAC)联合治疗因合并症不适合接受强诱导化疗,或者年龄75 岁及以上的新诊断的成人AML 患者于2020 年12 月在国内获批上市。维奈克拉于2022 年纳入国家医保目录,2021 年样本医院销售额达1268 万元,2022 年样本医院销售额达3087 万元。
维奈克拉获批适应症情况
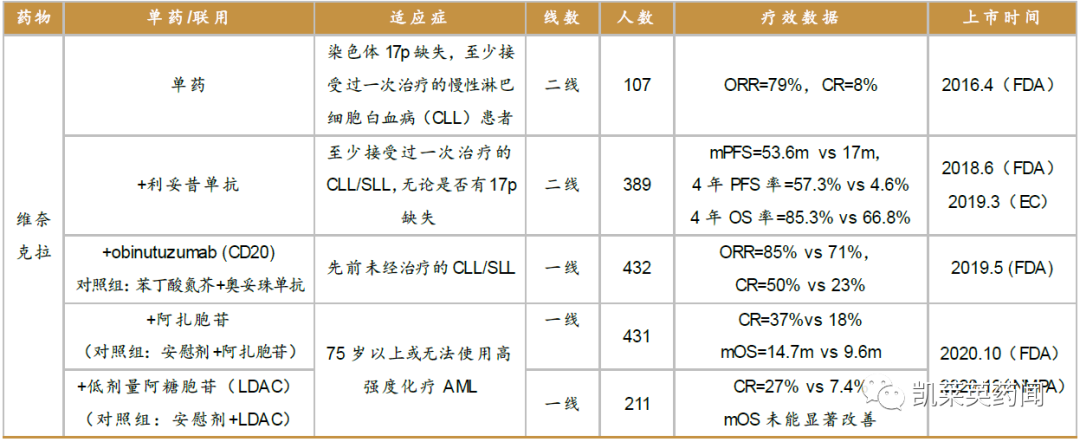
在本次会议中,浙江大学医学院附属第一医院尤良顺教授团队分享了一项II期、开放标签、单臂、多中心研究,创新性地将维奈克拉与阿扎胞苷和阿糖胞苷(VAA)联合使用治疗R/R AML患者,相关研究入选了2023 ASCO的壁报展示。研究的主要终点是复合完全缓解(CRc;包括CR和CRi)率、PR和MLFS,次要终点是OS和DOR。安全性终点为根据CTCAE分级的不良事件。
结果显示:
(1)所有患者的CRc率为62.1%(18/29),其中CR率为34.5%,CRi率为27.6%,PR率为13.8%。
(2)ELN中危/不良风险组、≥65岁组和基线骨髓计数≥30%组的CRc率分别为59.1%(13/22)、62.5%(5/8)和50.0%(7/14)。值得注意的是,M4/5患者的CRc率达72.7%(8/11)。
(3)中位随访6.95个月,中位OS和中位DOR尚未达到。预计12个月OS率为86%,预计12个月DOR率为62.6%。ELN中危/不良风险患者的中位DOR为7.5个月,预计12个月OS率和DOR率分别为84.3%和63.8%。既往骨髓计数低于30%且既往未接受过含HMA方案治疗的患者与良好的估计12个月DOR率相关。
(4)该方案在65岁以下患者和65岁以上患者中具有相似的疗效。(5)安全性方面,未观察到TLS事件。无治疗相关死亡发生。
此外,在一项多中心、开放标签、II期临床试验MOLTO研究结果,评价维奈克拉、阿替利珠单抗和奥妥珠单抗联合治疗Richter综合征的研究中,治疗包括35个周期的奥妥珠单抗(1000mg C1-8)、阿替利珠单抗(1200mg C1-18)和维奈克拉(400mg/d C1-35),q21。主要终点为C6时ORR≥67%。
结果显示:
(1)ORR为67.9%(19/28),达到主要终点。CR率为28.6%。中位随访11.6个月后,11/19例患者(57.9%)持续缓解,其中6例患者持续缓解≥24个月。其余8例患者中,7例在中位治疗周期14个周期后进展,1例在C9缓解期死于败血症。中位缓解持续时间、PFS和OS分别为11.7、16.2和31.6个月。在13例进展患者中,4例接受了挽救治疗,中位随访时间为24.3个月。巨大包块和ECOG PS>1影响患者PFS。uMRD率、突变影响和慢性淋巴细胞白血病-RS克隆关系对患者结局的影响将在会议上进行介绍。
(2)17例患者(60.7%)记录了43起3~4级不良事件(AE),主要是血液学相关AE(51.2%)。6例患者报告了任何级别的免疫相关AE(2例为3~4级),均未导致停药。未观察到肿瘤溶解综合征。6例患者发生≥3级感染,包括2例5级感染患者。1例患者发生MDS。
二 亚盛医药:lisaftoclax
Lisaftoclax (APG-2575)是首款进入Ⅱ期关键注册临床的国产Bcl-2 抑制剂,治疗复发难治CLL/SLL 适应症处于关键注册Ⅱ期临床,有望于2023 年上半年完成入组。APG-2575通过选择性抑制Bcl-2 蛋白恢复肿瘤细胞程序性死亡机制(细胞凋亡),从而诱导肿瘤细胞凋亡,达到治疗肿瘤的目的。APG-2575 采用每日剂量递增,对专业医护人员及病人更加友好,能够减少肿瘤溶解综合征(TLS)风险。与Venetoclax 相较,其半衰期更短,药物暴露量更少,潜在降低肿瘤溶解综合征风险,安全性更强。
目前,APG-2575正在中国、美国、澳大利亚及欧洲进行19 项Ⅰb/Ⅱ期临床研究,其中治疗复发/难治性慢性淋巴细胞白血病/小淋巴细胞淋巴瘤的中国关键Ⅱ期研究已于2022 年3 月完成首例患者入组。
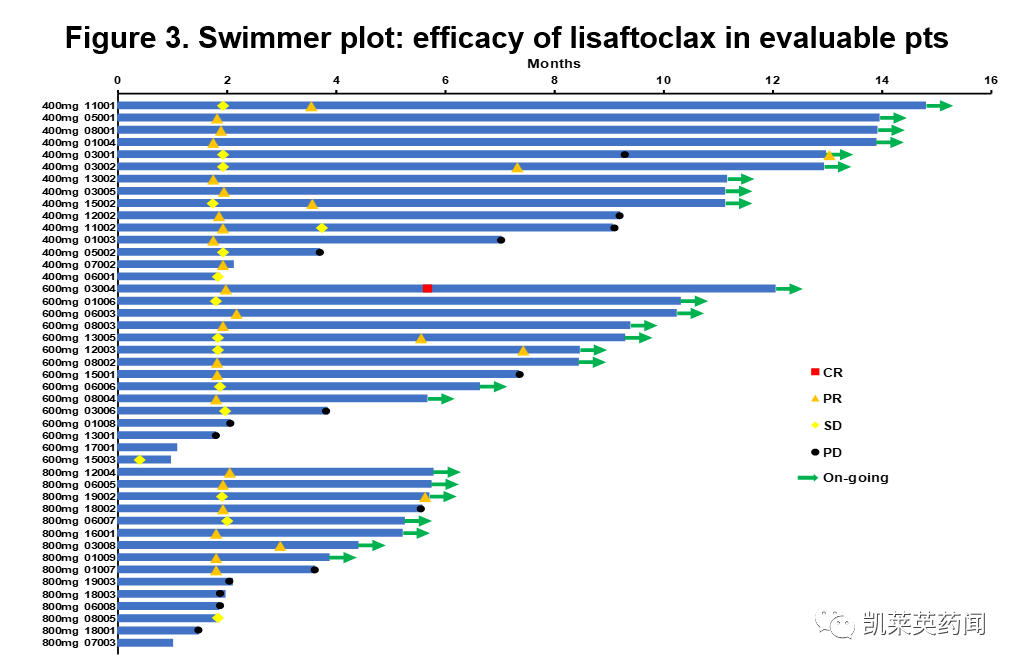
根据在2023 ASCO公布的数据,在一项开放性、多中心研究旨在评估APG-2575在中国R/R CLL/SLL患者中的安全性和抗肿瘤活性,以及药代动力学与药效学特征的试验中,将APG-2575每日口服一次,28天为一个周期,队列扩展在400mg、600mg、800mg 3个剂量水平进行,每个剂量组15个患者。
结果显示:APG-2575单药治疗在所有三个剂量组中均表现出良好安全性。从400mg到800mg剂量范围,都没有患者因为药物不耐受而降低剂量或退出治疗;仅有一例患者因为病情特殊发生TLS,暂停药物后TLS控制良好恢复继续治疗,其余所有患者(包括TLS高危患者)即使在每日剂量快速递增下也没有发生TLS。
每日剂量递增给药方式下TLS风险极低,和既往I期研究一致。中位治疗时长为7个疗程。在43例可评估R/R CLL/SLL患者中的ORR达到67.4%,其中1例完全缓解(CR),28例部分缓解(PR)。
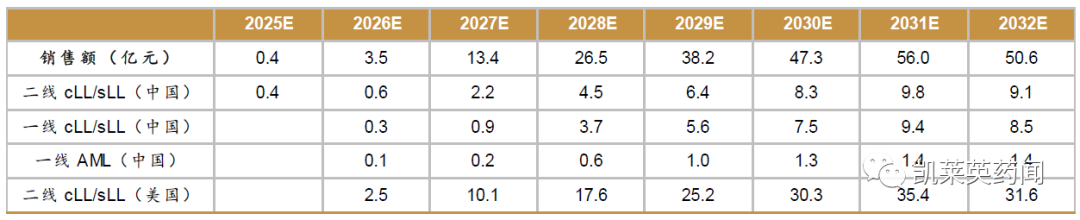
据西南证券推测,定价参考国内已上市维奈克拉价格,假设APG-2575 纳入医保前价格为25 万/年,纳入医保后降价40%,价格调整为15万元/年。销量有望高达56亿元。
三 百济神州:Sonrotoclax
Sonrotoclax (BGB-11417)的核心适应症为慢性淋巴细胞白血病/小淋巴细胞淋巴瘤(CLL/SLL),此外,其在急性髓系白血病(AML)、非霍奇金淋巴瘤(包括WM、MCL、MZL)、以及多发性骨髓瘤(MM)等多个适应症均有布局。
CLL/SLL:针对CLL/SLL 的初治和复发难治型患者,BGB-11417 单药或者联合BTK 抑制剂泽布替尼开展了名称为BGB-11417-202 和BGB-11417-101 的临床试验。预计联用泽布替尼针对初治的CLL/SLL 适应症今年能进入注册临床阶段。此外,单药也有针对BTK 抑制剂治疗失败的r/r CLL/SLL 的注册性研究潜力。
r/r MCL:BGB-11417 有望推进单药针对BTK 抑制剂治疗失败的r/r MCL 的注册性研究。
AML:BGB-11417 联合阿扎胞苷开展了针对AML 的Ib/II 期临床试验,对分子亚型的有效性分析、安全性拓展和高剂量的组评价正在进行中。目前在AML患者中耐受性良好。
r/r MM:BGB-11417 联合地塞米松的剂量递增试验正在进行,未达到RP2D。
在本次ASCO上,公司公布了一项关于“OX40激动剂BGB-A445与BCL-2抑制剂BGB-11417的早期研究结果”,剂量探索研究结果表明该试验性分子作为单药治疗B细胞恶性肿瘤患者中,在最高每日640 mg的所有试验剂量下耐受性均良好,且未出现剂量依赖性的毒性增加。BGB-11417单药治疗在R/R慢性淋巴细胞白血病/小淋巴细胞淋巴瘤中也显示出良好的初步疗效结果,患者能够在较低剂量水平下产生缓解。
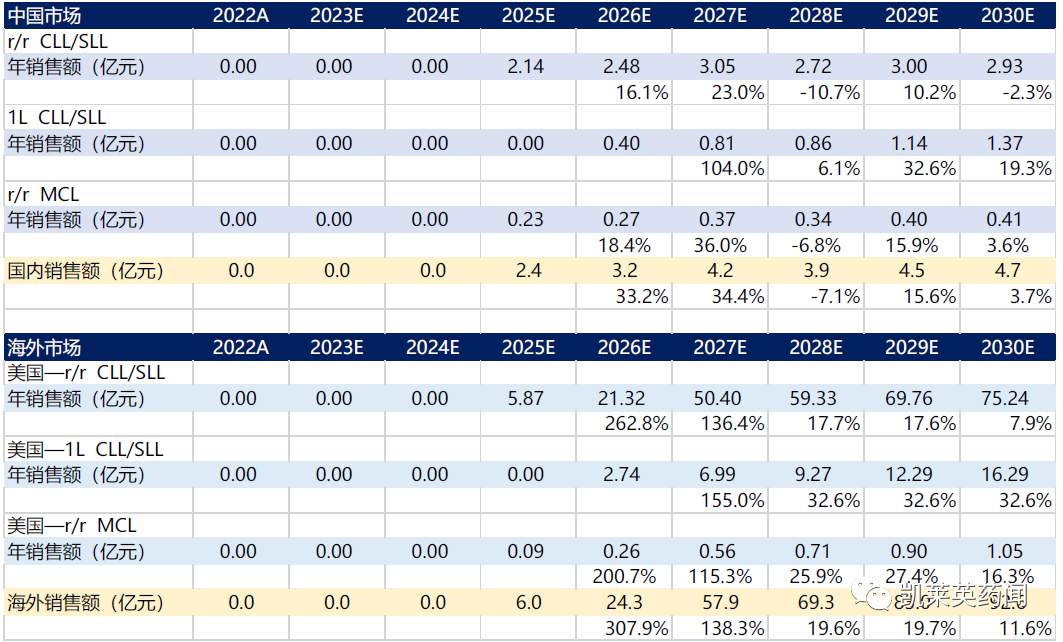
BGB-11417 在国内预计将于2025 年上市,2030 年达到销售峰值,峰值销售额约为5 亿元。预计在美国将于2025 年上市,预计2030 年达到销售额约为93 亿元。
四 维奈克拉、APG-2575、BGB-11417的比较
1、分子结构的比较
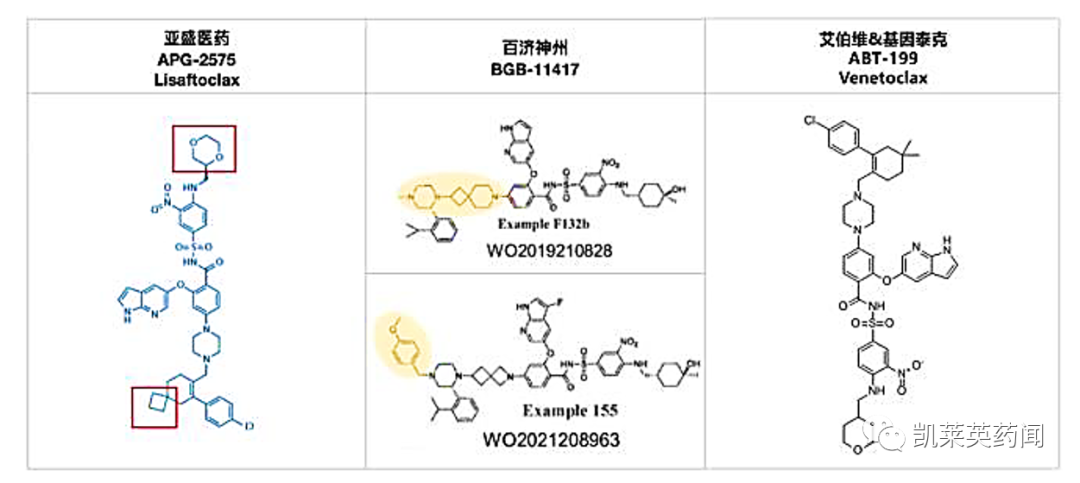
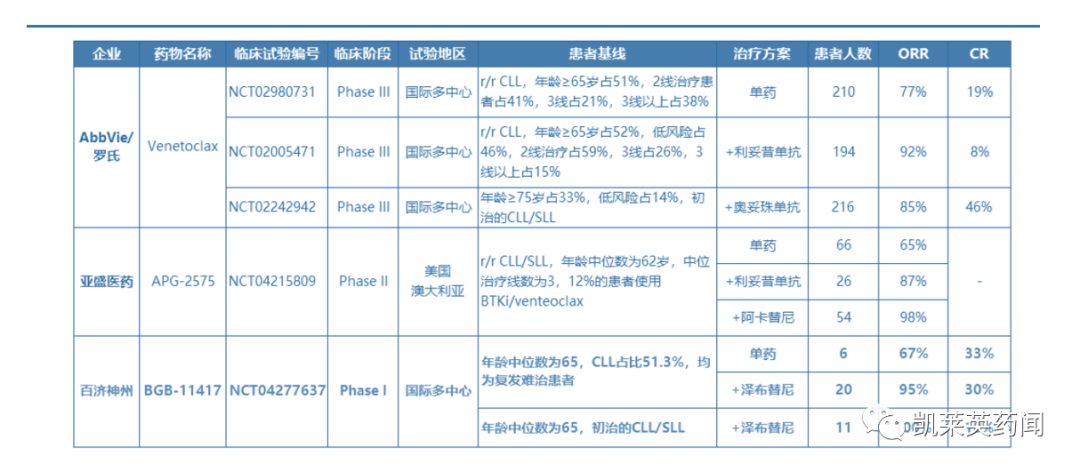
2、临床疗效数据比较
APG-2575、BGB-11417单药在r/r患者中疗效不算出色,但在联合用药探索中,都获得了富有潜力ORR或CR数据。
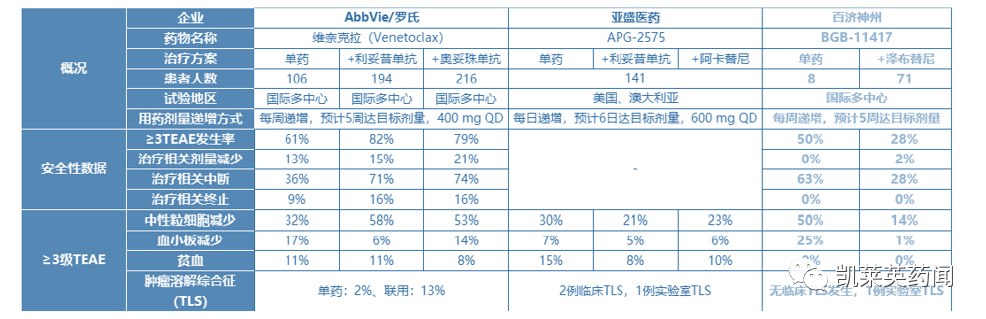
3、安全性比较
APG-2575为每日剂量递增的方案,BGB-11417是更为保守的每周剂量递增方案;此外,随访期间两药都没有患者因AE导致终止治疗。尤其是BGB-11417联用泽布替中先后服药方案的设计,整体≥3级AE率明显降低。
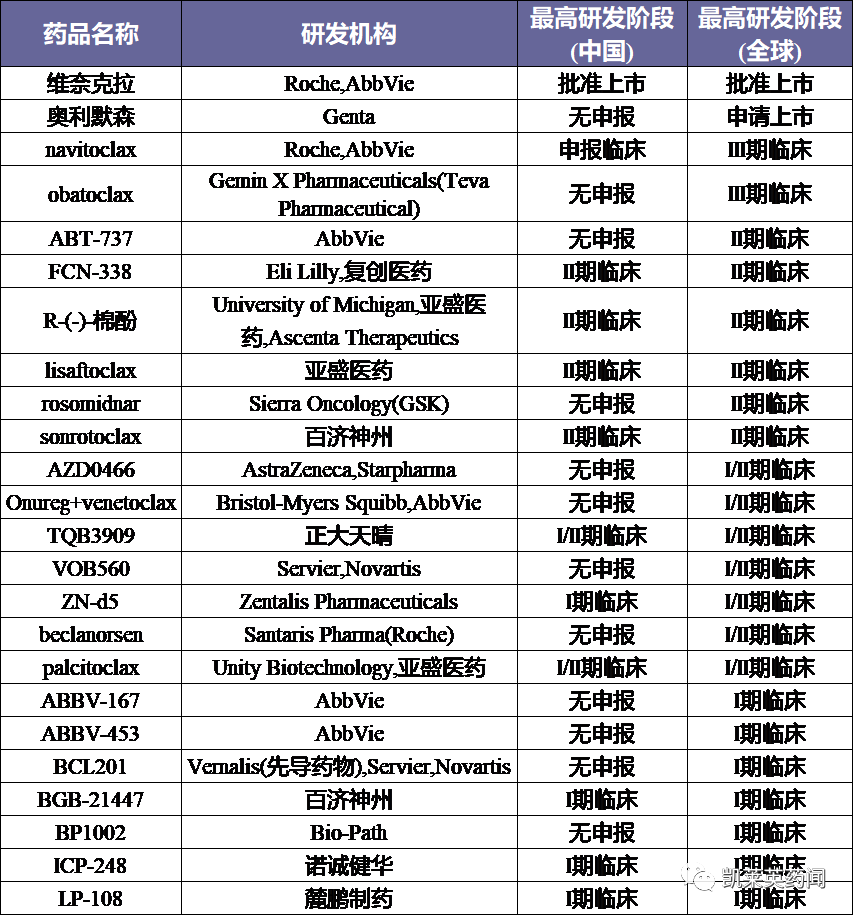
在研管线及总体规模预测
据不完全统计,目前在研的Bcl-2抑制剂近50余种,大多数公司都布局在血液瘤领域,联合用药是未来主要研发的方向。将目前处于临床阶段的在研药物统计如下:
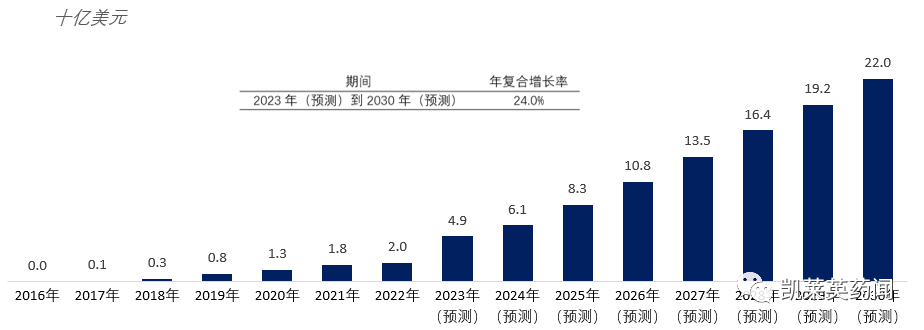
Bcl-2 家族蛋白是细胞凋亡机制新药研发最多的领域,根据弗若斯特沙利文分析,全球靶向细胞凋亡治疗市场未来前景广阔,预计2023 年-2030 年年复合增长率达24%,2030 年全球市场规模将达到220 亿美金。Bcl-2 蛋白作为细胞凋亡领域最重要的靶点之一,维奈克拉验证了此靶点的成药性,联合用药(与CD20 单抗,与BTK 抑制剂)拓宽了Bcl-2抑制剂的使用场景,未来市场空间有望逐步打开。
全球细胞凋亡靶标治疗市场规模(2016—2030 年)
参考资料
1、ASCO、各公司官网
2、西南证券、东吴证券
3、公众号:医脉通、血液肿瘤咨询
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








专业,深入,学到了,很好
34