PNAS:分子伴侣新疗法有望治疗代谢性疾病
2013-05-06 ZinFingerNase 生物谷
来自美国马萨诸塞大学阿姆赫斯特分校(University of Massachusetts Amherst)的研究人员鉴定出两种新的小分子伴侣可能用于治疗被称作辛德勒疾病(Schindler/Kanzaki disease, 也称作神崎病)的遗传性代谢疾病。这就为人们有史以来开发出治疗这种罕见疾病的药物提供希望。相关研究于近期刊登在PNAS期刊上。论文第一作者为Nathaniel Clark。

来自美国马萨诸塞大学阿姆赫斯特分校(University of Massachusetts Amherst)的研究人员鉴定出两种新的小分子伴侣可能用于治疗被称作辛德勒疾病(Schindler/Kanzaki disease, 也称作神崎病)的遗传性代谢疾病。这就为人们有史以来开发出治疗这种罕见疾病的药物提供希望。相关研究于近期刊登在PNAS期刊上。论文第一作者为Nathaniel Clark。
溶酶体贮积病(lysosomal storage disease, LSD)是非常罕见的,有50多种,辛德勒疾病是其中一种。这么多种溶酶体贮积病每年影响7千到8千的新生儿。迄今为止,人们还无法治疗这类疾病。
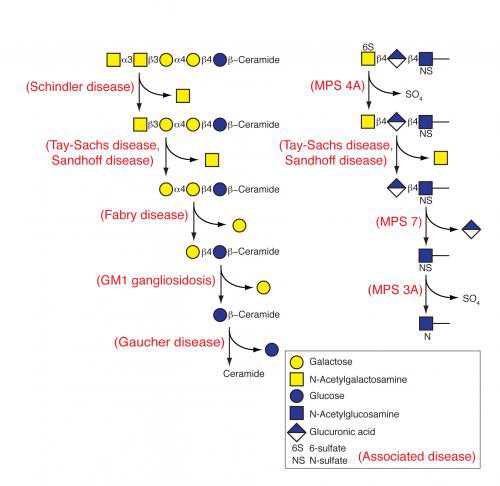
出生时患有辛德勒疾病的婴儿拥有单个编码α-N-乙酰半乳糖胺酶(alpha-N-acetylgalactosaminidase, alpha-NAGAL)的缺陷性基因拷贝。alpha-NAGAL是清除使用过的毒性底物的细胞回收装置的一部分。当alpha-NAGAL正常发挥作用,它降解被称作细胞回收中心---即溶酶体---内的含糖底物。如果alpha-NAGAL表现不佳或者不能发挥作用时,病人产生神经肌肉问题,如癫痫和肌无力。Garman说,“一些底物是非常有毒的,因而患有这些疾病的小孩确实病情严重,并且很多人只能存活较短的时间。”
这种缺陷性的基因导致酶alpha-NAGAL错误折叠,从而导致它不稳定并且发挥出较差的功能。治疗这种疾病的一种途径就是利用被称作药物分子伴侣(pharmacological chaperone)的小分子来稳定alpha-NAGAL。Garman和同事们鉴定出和测试过的两个小分子让种酶处于正确折叠的过程之中。
在这项研究中,研究人员证实这两种分子伴侣,即糖模拟物(亚胺糖)DGJ和DGJNAc,如何让缺陷性的酶alpha-NAGAL保持稳定。再者,Garman和同事们首次利用生物化学、晶体学和细胞实验来精确地证实这两种小分子如何结合到这种酶上并提供这种稳定性。
Garman说,“人们已假设利用酶DGJNAc来治疗辛德勒疾病将是有效的。如今,我们首次证实它确实如此。这些实验表明我们能够将DGJNAc加到细胞之中,并增加这种酶的数量。”
在当前这项研究中,研究人员开发出检测方法来测定这两种小分子伴侣如何结合到酶alpha-NAGAL上,并且它们如何影响这种酶的活性、稳定性和细胞内的位置。
人们已发现DGJ在人体内安全的,而且正在处于治疗法布瑞氏症(Fabry disease)的第三期临床试验,其中布瑞氏症是另一种溶酶体贮积病。多亏这项研究,DGJ和DGJNAc都可能被用来治疗患有辛德勒疾病的病人

Pharmacological chaperones for human α-N-acetylgalactosaminidase
Schindler/Kanzaki disease is an inherited metabolic disease with no current treatment options. This neurologic disease results from a defect in the lysosomal α-N-acetylgalactosaminidase (α-NAGAL) enzyme. In this report, we show evidence that the iminosugar DGJNAc can inhibit, stabilize, and chaperone human α-NAGAL both in vitro and in vivo. We demonstrate that a related iminosugar DGJ (currently in phase III clinical trials for another metabolic disorder, Fabry disease) can also chaperone human α-NAGAL in Schindler/Kanzaki disease. The 1.4- and 1.5-Å crystal structures of human α-NAGAL complexes reveal the different binding modes of iminosugars compared with glycosides. We show how differences in two functional groups result in >9 kcal/mol of additional binding energy and explain the molecular interactions responsible for the unexpectedly high affinity of the pharmacological chaperones. These results open two avenues for treatment of Schindler/Kanzaki disease and elucidate the atomic basis for pharmacological chaperoning in the entire family of lysosomal storage diseases.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







#分子伴侣#
34
#PNAS#
0
#代谢性#
38
#新疗法#
46
#伴侣#
35