急性冠脉综合征ACS合并上消化道出血的诊治
2020-11-30 《门诊》杂志 门诊新视野
抗栓治疗作为急性冠脉综合征(ACS)药物治疗的基石,对于ACS及其接受介入治疗的患者,双联抗血小板治疗能够显着降低早期和长期不良心血管事件的发生率。然而,与抗栓治疗相关的各种出血并发症也日渐增加。
抗栓治疗作为急性冠脉综合征(ACS)药物治疗的基石,对于ACS及其接受介入治疗的患者,双联抗血小板治疗能够显着降低早期和长期不良心血管事件的发生率。然而,与抗栓治疗相关的各种出血并发症也日渐增加。谈及ACS出血并发症,消化道出血不仅发生率较高,且严重影响患者预后,值得特别关注!当ACS“遇到”“上消化道出血”,临床应采取何种策略?
ACS合并消化道出血的流行病学
GRACE[1]、HORIZONS-AMI[2]、ACUITY[3]研究显示,ACS患者院内30 d大出血发生率高达3.0%-8.3%;同时,2014年发表于《中国心血管病研究杂志》的一项研究[4]显示,行急诊PCI的STEMI患者严重出血(BARC分型≥3型)发生率高达6.4%。
与穿刺部位出血相比,非穿刺部位相关出血所占的比率较高,且以消化道出血为主。NCDR Cath PCI注册研究[5]显示,在PCI术后患者中,非穿刺部位出血占57.9%,消化道出血为16.6%;一项瑞士PCI注册研究[6]显示,PCI患者1年抗血小板治疗期间不同部位出血中,消化道出血比例约30%,占比最高。
消化道出血可显着增加ACS患者短期和长期死亡率;对于ACS患者,积极预防消化道出血尤为重要。一项基于ACUITY研究的事后分析[7]显示,消化道出血是ACS患者30天和1年死亡的独立预测因素,易引起患者临床结局的恶化。
ACS合并消化道出血的发生机制
在抗栓药物导致的出血中,以消化道出血最为常见。抗栓药物包括抗血小板药物和抗凝药物两大类,导致消化道出血的机制较为复杂,往往可分成4种情况:
阿司匹林通过局部和全身作用引起消化道黏膜损伤、出血;
氯吡格雷通过影响胃肠道黏膜损伤愈合,导致修复受损、出血;
血小板糖蛋白Ⅱb/Ⅲa抑制剂(GPI)阻断血小板聚集的终末途径,通过强效抑制血小板聚集而导致出血;
新型抗凝药物(达比加群、利伐沙班、阿哌沙班等)所致出血往往与用药剂量过大、患者高龄、心力衰竭、既往有消化道出血病史等相关。
阿司匹林所致消化道损伤的特点[8]:
服药后12个月内为消化道损伤的多发阶段,3个月时达高峰;
阿司匹林的抗血栓作用并不随剂量增加而增加,而消化道损伤风险随剂量增大而明显增加。阿司匹林高剂量、低剂量均可增加上消化道溃疡出血风险;
老年患者是抗血小板药物消化道损伤的高危人群,年龄越大,危险越大;
幽门螺杆菌(HP)感染可加重阿司匹林的消化道损伤作用,在开始长期抗血小板治疗之前,建议有条件患者应检测并根除HP;
阿司匹林与其他抗血小板或抗凝药物联用明显增加严重出血发生危险,主要以消化道出血为主;
阿司匹林剂型改良并不能避免消化道损伤风险,不同剂型阿司匹林发生消化性溃疡及消化道出血危险的差异无统计学意义。
“全身作用”对阿司匹林致消化道损伤贡献较大,对于阿司匹林肠溶片,局部直接刺激作用减少,但COX-2环氧化酶活性抑制的全身作用依然存在[9]。(图1)
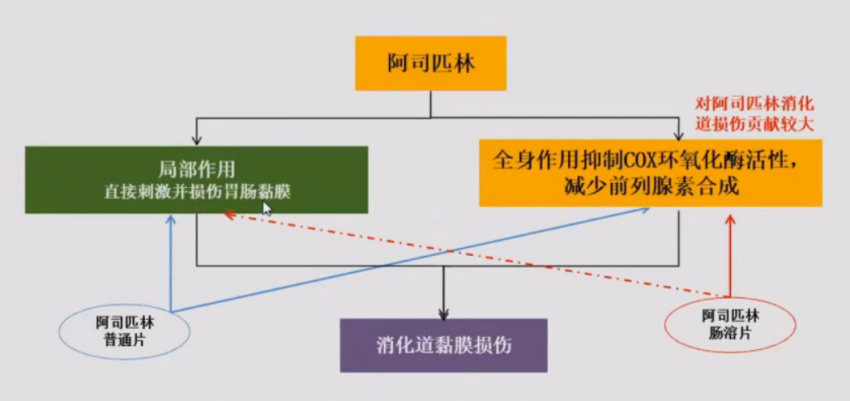
图1. 阿司匹林致消化道损伤的机制
ACS合并上消化道出血的风险评估及预防
PCI术前应常规采用CRUSADE评分预测ACS患者出血风险。CRUSADE评分包括入院时的8个指标:基线血细胞比容、肌酐清除率、心率、收缩压、性别(女性)、症状中有充血性心力衰竭的征象、既往外周血管疾病史或卒中史、糖尿病。根据CRUSADE评分,患者可分为五级:极低危≤20分;低危21-30分;中危31-40分;高危41-50分;很高危>50分。
《ACS抗栓治疗合并出血防治多学科专家共识 2016》[10]推荐,ACS患者上消化道出血预防策略包括:1.合理选择和使用抗栓药物;2.使用口服抗凝剂的患者减少联合用药;3.特殊ACS患者的抗凝治疗;4.应用质子泵抑制剂(PPI)预防消化道出血。
抗血小板药物应如何选择?
1)阿司匹林:长期服用宜选择肠溶制剂;2)P2Y12受体抑制剂:若出血风险不高(如CRUSADE≤30分),NSTE-ACS患者、直接PCI的STEMI患者,建议优先选择替格瑞洛[10]。PLATO研究[11]结果显示,与氯吡格雷相比,替格瑞洛双抗治疗1年显着降低患者主要心血管事件风险,且不增加主要出血风险。2016年发表在《临床军医杂志》的一项研究[12]显示,对于行药物洗脱支架植入的ACS患者,替格瑞洛与氯吡格雷相比可显着降低1年心血管事件和死亡风险,且不增加致命性大出血事件。
非口服抗凝药物应如何选择[10]?
1)对于NSTE-ACS患者,若出血风险较高(如CRUSADE≥31分),PCI术前建议选用磺达肝癸纳(2.5 mg皮下注射,1次/d);2)对于拟行PCI且出血风险为中、高危的患者(如CRUSADE≥31分),PCI术中抗凝建议选用比伐芦定;3)对于拟行PCI的患者,若存在高出血风险(如CRUSADE≥41分),PCI术中亦推荐使用比伐芦定,但术后不强调高剂量维持应用;4)出血风险低(如CRUSADE≤30分)且无肝素诱导的血小板减少症(HIT)的患者,可使用普通肝素(UFH),尽量不与GPI联合使用,以降低出血发生风险。
抗栓药物联合使用原则[10]?
1)常规上游(如急救车和急诊室)使用GPI增加出血风险,不宜推荐;2)高危患者(如血清肌钙蛋白阳性)、造影提示血栓负荷较重或未给予适当负荷量P2Y12受体抑制剂的患者可考虑静脉使用GPI。如需联用GPI,PCI术中使用UFH的剂量应调整为50-70 u/kg;3)PCI围术期交叉使用UFH和低分子肝素(LMWH)增加出血风险,应尽量避免。ACUITY研究[13]显示,常规上游GPI治疗显着增加中高危ACS患者出血风险;SYNERGY研究[14]显示,PCI围术期交叉使用UFH和LMWH,患者出血风险显着增加。
特殊ACS患者抗栓治疗[15]:
1.长期使用口服抗凝剂(OAC)患者:长期使用OAC是溶栓治疗的相对禁忌症;急诊PCI前无需停用OAC,同时加用双联抗血小板治疗;术中推荐患者继续接受肝素抗凝治疗,无需考虑患者末次口服抗凝药的时间;避免使用GP IIb/IIIa受体拮抗剂;术后推荐三联抗栓治疗4-6 W后改为双联抗栓(P2Y12受体抑制剂+OAC),建议使用新型口服抗凝药(NOAC);若患者存在无法纠正的高出血风险,且低血栓风险,则可在出院后改为双联抗栓治疗;2.合并肾功能不全患者:ACS合并CKD需要根据肾功能水平调整抗栓药物的选择和剂量。
《ACS抗栓治疗合并出血防治多学科专家共识 2016》[10]推荐,对于胃肠出血风险较高者,如合并胃肠道溃疡或出血病史;长期使用非甾体类抗炎药(NASIDs)或波尼松;具有下列两项或更多危险因素:年龄≥65岁;消化不良;胃食管反流病;HP感染;长期饮酒,建议在DAPT基础上合用PPI(3-6个月),6个月后可考虑继续或间断服用,以预防或降低消化道出血。
《ACS抗栓治疗合并出血防治多学科专家共识 2016》[10]强调:部分PPI可通过CYP2C19竞争抑制氯吡格雷的抗血小板作用,对于服用氯吡格雷的患者,仍建议尽可能选择泮托拉唑、雷贝拉唑等影响较小的药物。ADAPT-DES研究[16]显示,氯吡格雷与PPI联用可降低血小板抑制效果,增加心血管事件风险;PLATO亚组分析[11]显示,替格瑞洛与PPI联用不影响其降低心血管事件的临床疗效,不增加主要出血。
ACS抗栓治疗合并上消化道出血的救治
对于ACS抗栓治疗合并出血的患者,应尽快完成出血与缺血双评估,在选择合理止血方案(压迫止血、药物治疗、内镜治疗、外科手术等)的基础上,决定后续抗栓治疗策略。在出血的评估与处理、缺血风险的评估和抗栓策略调整等过程中,心血管医师应整合多学科意见做出最佳临床决策[10](图2)。
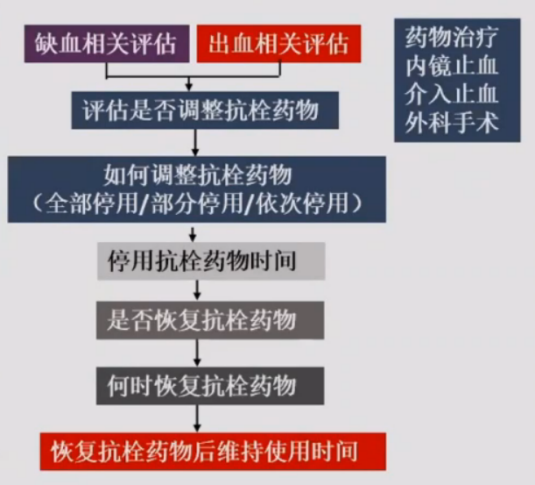
图2. ACS患者抗栓治疗合并出血的临床决策路径
ACS患者在抗栓治疗过程中一旦发生上消化道出血,应首先评估血流动力学是否稳定,决定是否需要采取输血及血管活性药物使用;同时应综合评估缺血与出血风险,调整抗栓治疗策略。小出血(如BARC出血分型<3型)患者,可在充分止血及监测下继续服用抗栓药物;严重出血(如BARC出血分型≥3型)患者,应考虑药物种类及剂量。当出血无法控制或可能威胁生命时,应立即停药,并予新鲜血小板输注等治疗;对于血栓事件高风险的患者(如BMS置入≤1个月或DES置入≤3个月),应积极采用内镜下止血治疗,并尽可能保留DAPT;对于溃疡性出血复发危险较高的患者,不建议使用氯吡格雷替代阿司匹林联合PPI治疗。需注意,当满足以下条件考虑出血已经得到控制,5 d后可恢复使用抗血小板药物:1.血流动力学稳定;2.不输血情况下,血红蛋白稳定;3.血尿素氮(BUN)不继续升高;4.肠鸣音不活跃;5.便潜血转阴(非必需条件)[10]。
临床实践中,“再出血”本身也可导致病死率增高。内镜是ACS抗栓治疗合并出血处理的重要方法,内镜止血后在“再发出血”的预测因素包括血流动力学不稳定、内镜下活动性出血、溃疡大于2 cm、溃疡位于胃小弯上部或十二指肠后部、血红蛋白低于100 g/L和需要输血等[10]。
总结
ACS合并非穿刺部位出血中,以消化道出血发生率最高;消化道出血可显着增加ACS患者死亡风险,合理评估、识别消化道出血的高危人群至关重要。除此之外,临床实践中,应积极采取策略预防ACS患者上消化道出血;如果预防不佳,一旦发生上消化道出血,首先需评估血流动力学是否稳定,同时应综合评估缺血与出血风险,调整抗栓治疗策略。如需止血,往往首先考虑静脉PPI等药物治疗、内镜、介入止血,但如果仍无法止血可考虑外科手术。
原始出处:
[1]Moscucci M,et al.Eur Heart J.2003;24(20):1815-1823.
[2]Stone GW,et al.N Eng J Med.2008;351(21):2218-2230.
[3]Stone GW,et al.N Eng J Med.2006;355(21):2203-2216.
[4]何培源等.中国心血管病研究,2014;12(7):577-582.
[5]Subherwal S,et al.J AM Coll Cardial.2012;59(21):1861-1869.
[6]Konstantinos C.Koskinas,et al.Circ Cardiovasc Interv.2015;8:e002053.
[7]Eugenia Nikoisky,et al.J Am Coll Cardiol.2009;54:1293-302.
[8]抗血小板药物消化道损伤的预防和治疗中国专家共识组.中华内科杂志,2013;52(3):264-270.
[9]Abajo FJ,et al.BMC Clin Pharm.2001;1:1.
[10]中国医师协会心血管内科医师分会,等.中华内科杂志,2016;55(10):813-824.
[11]Wallentin L,et al.N Engl J Med.2009;361:1045-1057.
[12]刘然,聂绍平等.临床军医杂志,2016;44(5):454-495.
[13]Stone GW,et al.JAMA.2007;297:591-602.
[14]White HD,et al.Am Heart J.2006;152:1042250.
[15]中华心血管病杂志编辑委员会.中华心血管病杂志(网络版),2019;2(1):1-9.
[16]Weisz G,et al.Circ Cardiovasc Interv.2015;8:e001952.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#上消化道#
50
#ACS#
41
#综合征#
50
#消化道#
32
ACS合并非穿刺部位出血中,以消化道出血发生率最高;消化道出血可显着增加ACS患者死亡风险,合理评估、识别消化道出血的高危人群至关重要。除此之外,临床实践中,应积极采取策略预防ACS患者上消化道出血;如果预防不佳,一旦发生上消化道出血,首先需评估血流动力学是否稳定,同时应综合评估缺血与出血风险,调整抗栓治疗策略。如需止血,往往首先考虑静脉PPI等药物治疗、内镜、介入止血,但如果仍无法止血可考虑外科手术。
101